Clear Sky Science · es
Sintilimab neoadyuvante, paclitaxel ligado a albúmina y carboplatino para carcinoma escamoso de esófago localmente avanzado y resecable: estudio clínico y exploración mecanicista
Cambiando la marea contra un letal cáncer de la garganta
El cáncer de esófago es uno de los más mortales a nivel mundial y a menudo se descubre cuando ya ha avanzado profundamente en el tórax. Muchos pacientes aún son candidatos a cirugía, pero incluso con la mejor quimioterapia y radioterapia actuales, el riesgo de recurrencia sigue siendo alto. Este estudio prueba una nueva forma de potenciar las defensas del propio cuerpo antes de la cirugía y examina microscópicamente cómo cambian los tumores y las células circundantes en respuesta. Los hallazgos apuntan a tratamientos más eficaces y a un camino hacia una atención verdaderamente personalizada.
Un nuevo plan de tres fármacos antes de la cirugía
Los investigadores reclutaron a 24 personas en China con una forma común y agresiva de cáncer de esófago llamada carcinoma de células escamosas. Todos tenían tumores avanzados pero aún resecables. Antes de pasar al quirófano, cada paciente recibió tres ciclos de un tratamiento combinado: sintilimab, un anticuerpo que activa el sistema inmunitario y facilita que las células T reconozcan el cáncer; además de dos fármacos quimioterápicos estándar, paclitaxel ligado a albúmina y carboplatino. Tras esta fase neoadyuvante, los pacientes se sometieron a cirugía para extirpar el tumor esofágico y la mayoría continuó con sintilimab después.
Mayor reducción tumoral y supervivencia alentadora
Cuando cirujanos y patólogos examinaron los tumores extirpados, encontraron que este régimen previo a la cirugía produjo reducciones profundas en muchos pacientes. Aproximadamente el 42 % mostró lo que los médicos llaman una respuesta patológica mayor, es decir, que solo quedaba una fracción pequeña de células tumorales vivas. Uno de cada tres pacientes no presentó células cancerosas detectables en el tumor principal. En las pruebas de imagen y el seguimiento clínico, los resultados también fueron prometedores: tres años después del tratamiento, alrededor de tres de cada cuatro pacientes estaban vivos sin signos de recurrencia, y casi cuatro de cada cinco seguían vivos. Es importante destacar que los efectos secundarios de este plan intensificado fueron manejables, sin muertes relacionadas con el tratamiento y con la cirugía manteniéndose segura y factible.
Cómo el vecindario tumoral moldea la respuesta
No todos los pacientes se beneficiaron por igual, así que el equipo investigó por qué. Se centraron en el microambiente tumoral: el complejo vecindario de células cancerosas, células inmunitarias y moléculas señalizadoras. Usando mediciones proteicas dirigidas en muestras tumorales cuidadosamente diseccionadas, compararon quienes respondieron bien con quienes no. Antes del tratamiento, hallaron 14 proteínas que diferían entre ambos grupos. Una proteína de superficie, CD44, destacó: los tumores con niveles más altos de CD44 tendían a responder mejor a la terapia basada en sintilimab. Tras el tratamiento, muchas proteínas implicadas en la actividad inmune y en la reparación del ADN se redujeron en los respondedores, lo que sugiere que la terapia combinada había alterado con éxito los sistemas de soporte del cáncer y remodelado el paisaje inmune local.
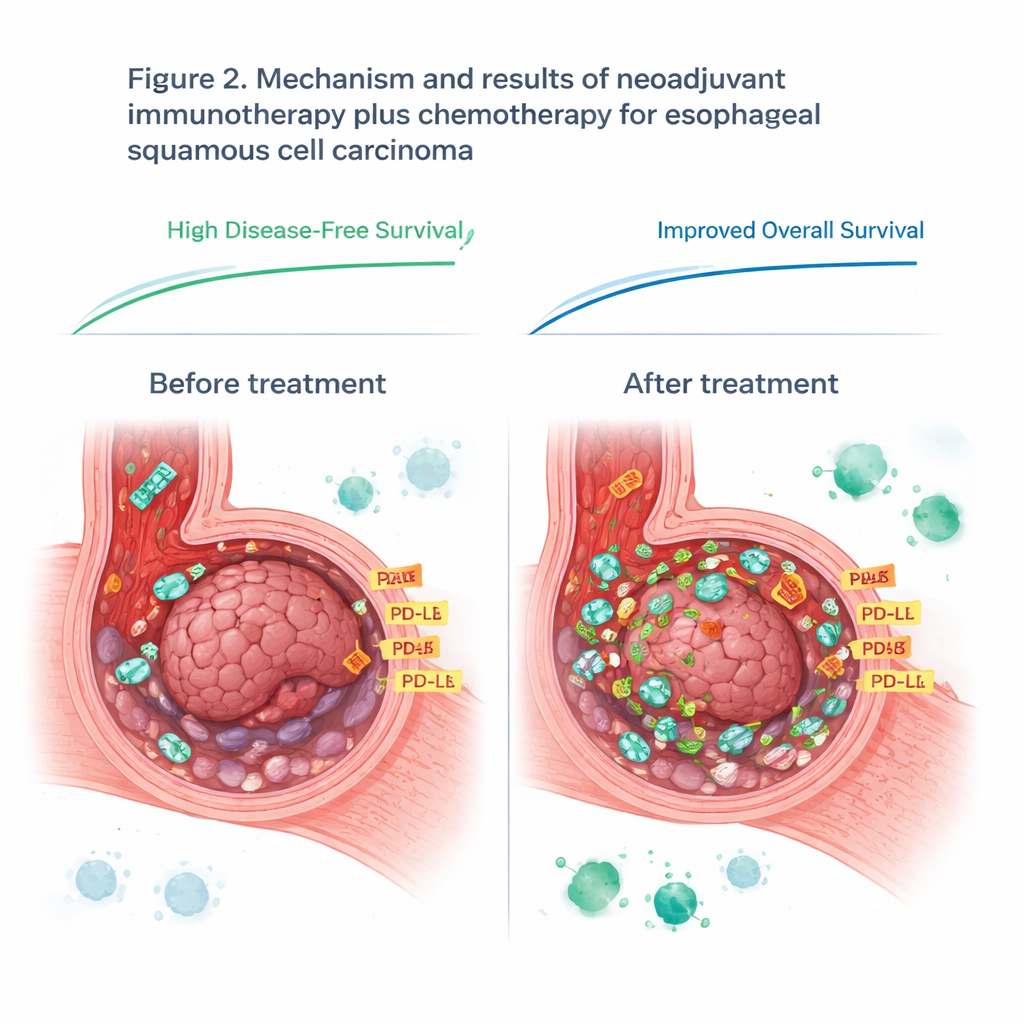
Repensando un marcador inmune popular
El estudio también examinó PD-L1, una proteína frecuentemente usada como guía para decidir quién puede beneficiarse de los inhibidores del punto de control inmunitario. Antes del tratamiento, los niveles de PD-L1 en las muestras tumorales no predijeron quién tendría un buen resultado, lo que pone en cuestión la práctica actual en este tipo de cáncer. Sin embargo, los niveles de PD-L1 aumentaron en todos los pacientes durante el tratamiento, probablemente porque el sistema inmunitario activado inundó el tumor con señales inflamatorias. Tras la terapia, niveles más altos de PD-L1 en el tejido tumoral remanente se asociaron mejor con la eficacia de la inmunoterapia. Esto sugiere que el momento importa: una única medición de PD-L1 antes del tratamiento puede perder cambios cruciales que se desarrollan una vez que el sistema inmunitario se activa.
Qué significa esto para los pacientes y el futuro
Para las personas que afrontan una cirugía por un cáncer de esófago avanzado, este estudio ofrece dos mensajes esperanzadores. Primero, combinar sintilimab con quimioterapia antes de la cirugía parece reducir los tumores más profundamente y podría mejorar las probabilidades de supervivencia a largo plazo, sin añadir efectos secundarios peligrosos. Segundo, el trabajo demuestra que el tumor y su microambiente no son fijos; son remodelados por el tratamiento de formas que pueden seguirse mediante proteínas como PD-L1 y CD44. En el futuro, esas huellas moleculares podrían ayudar a los médicos a seleccionar y ajustar terapias en tiempo real, convirtiendo más tumores “fríos” que ignoran al sistema inmunitario en tumores “calientes” que permiten un ataque inmunitario potente y duradero.
Cita: Wu, H., Jiang, Q., Li, X. et al. Neoadjuvant sintilimab, albumin-bound paclitaxel, and carboplatin for locally advanced, resectable esophageal squamous cell carcinoma: clinical study and mechanistic exploration. npj Precis. Onc. 10, 82 (2026). https://doi.org/10.1038/s41698-025-01248-2
Palabras clave: cáncer de esófago, inmunoterapia, terapia neoadyuvante, inhibidores de PD-1, microambiente tumoral