Clear Sky Science · es
La transcriptómica espacial revela heterogeneidad molecular y dianas terapéuticas específicas por subtipo en el cáncer de pulmón de células pequeñas
Por qué importa este estudio sobre el cáncer de pulmón
El cáncer de pulmón de células pequeñas es una de las formas más letales de cáncer, afecta sobre todo a personas con historial de tabaquismo y con frecuencia reaparece rápidamente tras la quimioterapia. Los médicos saben que no todos los tumores de este tipo se comportan igual, pero hasta ahora carecían de herramientas para ver cómo se disponen en el interior de cada tumor los distintos tipos de células cancerosas y las células inmunitarias. Este estudio empleó una tecnología nueva que lee la actividad génica en miles de puntos diminutos a lo largo de un corte tumoral, creando un “mapa molecular” de cada muestra. Al combinarlo con análisis informáticos a medida, los investigadores descubrieron patrones ocultos que podrían señalar tratamientos más precisos y específicos por subtipo.
Mapeando los tumores in situ
El equipo analizó muestras tumorales de 21 pacientes con enfermedad limitada de cáncer de pulmón de células pequeñas que se sometieron a cirugía antes de recibir cualquier fármaco. En lugar de triturar el tejido y perder toda la información espacial, aplicaron transcriptómica espacial: una técnica que mide qué genes están activados en muchos puntos definidos a lo largo de una sección tisular. Cada punto conserva su posición original, lo que permite a los científicos vincular la actividad génica con el lugar físico donde residen las células cancerosas, las células normales y las células inmunitarias. Añadieron dos herramientas clave: un nuevo índice “Edgeindex” para cuantificar hasta qué punto las células tumorales infiltran el tejido vecino, y una red neuronal artificial —una forma de aprendizaje automático— para marcar automáticamente qué puntos son tumorales y cuáles no.
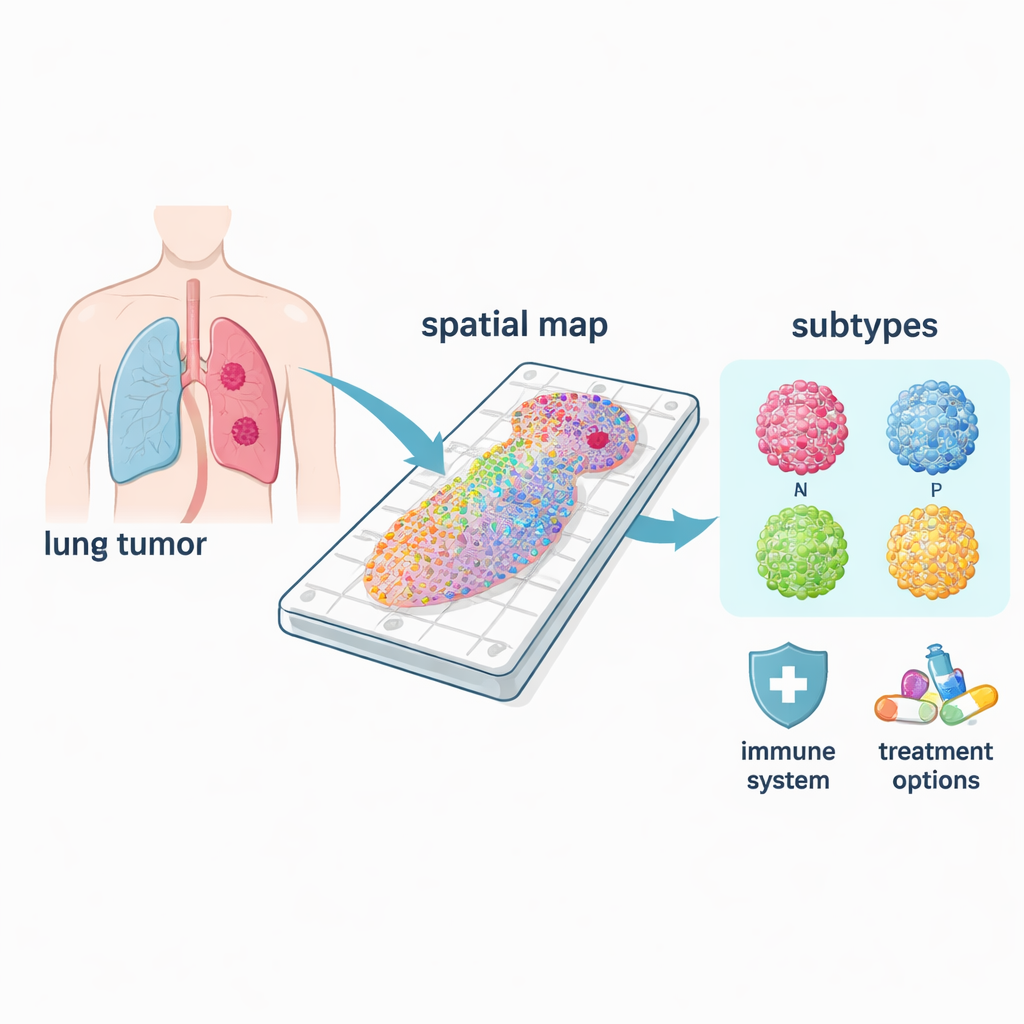
Diferentes tipos de cáncer en una misma enfermedad
El cáncer de pulmón de células pequeñas no es una sola enfermedad, sino que incluye al menos cuatro subtipos moleculares principales, a menudo llamados ASCL1, NEUROD1, POU2F3 y YAP1, por los genes reguladores que los definen. Con sus mapas espaciales, los investigadores pudieron ver dónde dominaba cada subtipo dentro de los tumores y cómo difería su biología. Las formas comunes ASCL1 y NEUROD1 se asociaron fuertemente a programas de división celular, coherentes con su reputación de alta proliferación. En contraste, las regiones POU2F3 se relacionaron con vías inmunitarias, mientras que las áreas YAP1 mostraron señales vinculadas al metabolismo y la remodelación tisular, rasgos que pueden conectar con la diseminación y la resistencia al tratamiento. Como estos patrones se resuelven en el espacio, el método puede identificar el verdadero subtipo “conductor” dentro de un tumor mixto, algo que las pruebas de conjunto suelen pasar por alto.
El borde invasivo y el cambio inmunitario
Una de las innovaciones centrales del estudio, el Edgeindex, captura cuánto se entremezclan las células tumorales con el tejido no tumoral circundante. Las puntuaciones bajas reflejan tumores compactos y bien delimitados, mientras que las altas indican islotes dispersos y bordes irregulares e invasivos. Los tumores con Edgeindex alto estaban enriquecidos en programas génicos relacionados con la matriz extracelular, la metástasis y la muerte celular. También mostraron un paisaje inmunitario notablemente alterado: menos linfocitos T colaboradores y otros actores de la inmunidad adaptativa, pero más células innatas como ciertos linfocitos NK y monocitos. Los autores interpretan esto como una “remodelación del nicho inmunológico”, en la que el tumor aleja las respuestas inmunitarias precisas y dirigidas y deja un defensa mayoritariamente innata, menos efectiva para controlar el cáncer.
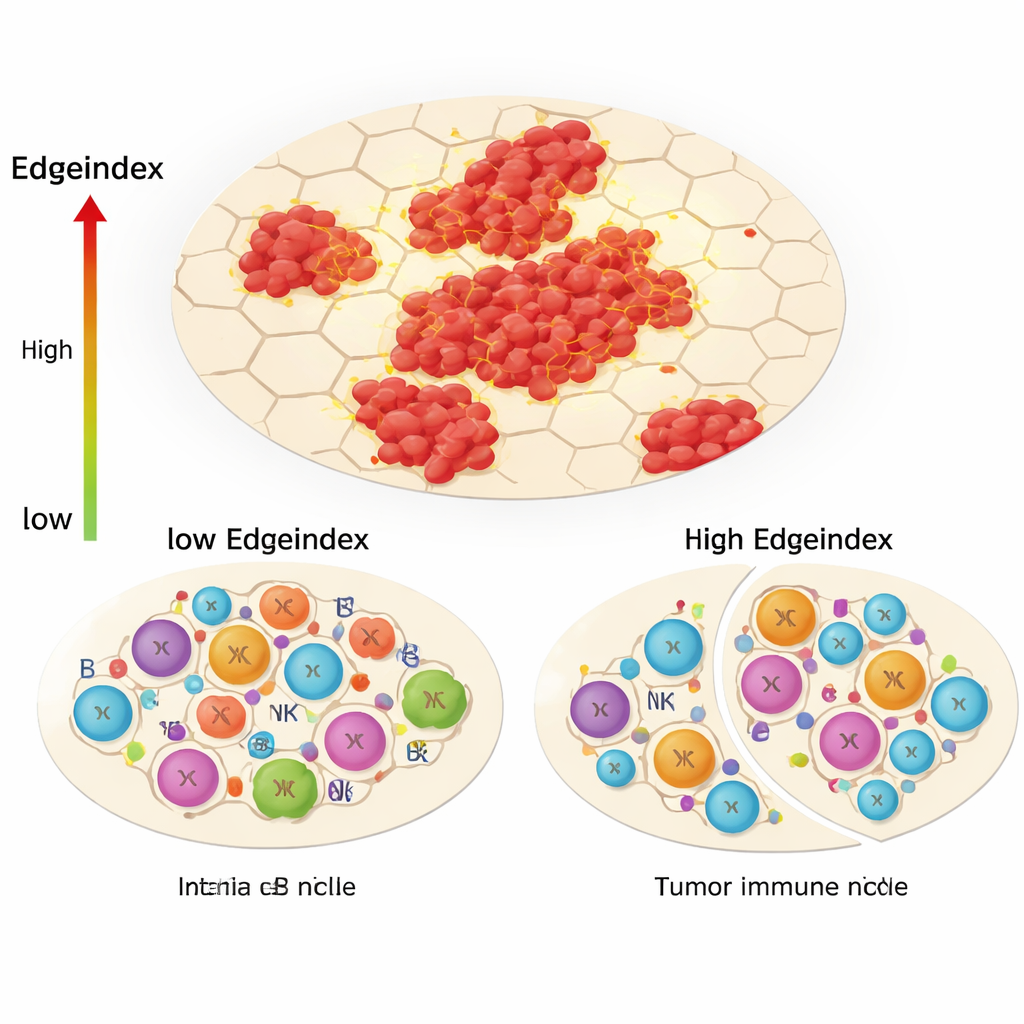
Diversidad oculta dentro y alrededor de los tumores
Más allá del subtipo y los patrones de invasión, los datos espaciales revelaron que tanto las poblaciones de células tumorales como sus microambientes circundantes eran internamente diversas. Al agrupar puntos dentro de cada tumor, el equipo contó cuántos vecindarios de expresión génica distintos existían en las regiones tumorales y en el tejido no tumoral cercano. Una mayor diversidad dentro del tumor se asoció a vías relacionadas con la inmunidad, mientras que ciertos patrones en el tejido circundante se vincularon a la actividad del ciclo celular y a la regulación genética. Los investigadores también examinaron con qué intensidad distintas regiones “se comunicaban” usando moléculas de señalización conocidas. Los tumores con comunicación más intensa entre regiones tendían a mostrar señales inmunitarias más fuertes, lo que refuerza la idea de que la actividad inmune y el crecimiento tumoral están estrechamente entrelazados en el espacio.
Siguiendo el desarrollo tumoral a lo largo del tiempo
Para aproximar cómo cambian las células tumorales a medida que progresa la enfermedad, el equipo realizó un análisis de “pseudotiempo” que ordena las células a lo largo de un trayecto de desarrollo según su actividad génica. A través de las muestras, identificaron recurrentemente un gen, UCHL1, como central en estas trayectorias. Niveles altos de UCHL1 coincidieron con fuerte actividad del ciclo celular en los puntos tumorales, mientras que niveles más bajos se alinearon con vías relacionadas con la inmunidad y la muerte celular. Dado que UCHL1 es una proteína de tipo neuronal previamente asociada a cánceres pulmonares agresivos, estos hallazgos refuerzan la hipótesis de que podría ser una diana farmacológica útil, en particular para las células de tipo neuroendocrino que impulsan el cáncer de pulmón de células pequeñas.
Qué significa esto para los pacientes
En términos sencillos, este estudio convierte cortes planos al microscopio de cáncer de pulmón de células pequeñas en mapas ricos y en capas que muestran dónde se localizan los distintos subtipos, con qué agresividad invaden, cómo se comunican con su entorno y cómo responde o fracasa el sistema inmunitario. El nuevo índice Edgeindex y el enfoque de mapeo señalan qué tumores son especialmente infiltrativos y qué células inmunitarias están presentes o ausentes en el borde. Al vincular estos patrones espaciales con debilidades específicas por subtipo —como fármacos dirigidos a DLL3, BCL‑2, AURKA, IGF‑1R/PARP o puntos de control inmunitario— el trabajo acerca el campo a emparejar a cada paciente con una estrategia de tratamiento más personalizada. Aunque estas herramientas aún deben validarse en estudios mayores, ofrecen un plano para terapias más precisas y potencialmente más eficaces en un tipo de cáncer que necesita urgentemente mejores opciones.
Cita: Xie, T., Tang, L., Fan, G. et al. Spatial transcriptomics reveals molecular heterogeneity and subtype-specific therapeutic targets in small cell lung cancer. npj Precis. Onc. 10, 81 (2026). https://doi.org/10.1038/s41698-025-01243-7
Palabras clave: cáncer de pulmón de células pequeñas, transcriptómica espacial, heterogeneidad tumoral, microambiente inmunitario tumoral, oncología de precisión