Clear Sky Science · es
Características de patología computacional de la arquitectura inmune predicen resultados clínicamente relevantes en el cáncer de pulmón de células pequeñas (CPCP)
Por qué importan los defensores del cuerpo en el cáncer de pulmón
El cáncer de pulmón de células pequeñas es una de las formas más agresivas de cáncer de pulmón, que a menudo se disemina con rapidez y reaparece tras el tratamiento. Los médicos pueden ver los tumores al microscopio, pero los patrones finos de cómo se disponen las células cancerosas y las inmunitarias son demasiado complejos para evaluarlos a simple vista. Este estudio presenta un método informático llamado PhenopyCell que lee esos patrones ocultos en las muestras de biopsia de rutina y los usa para predecir cuánto tiempo es probable que vivan los pacientes y qué tan bien podrían responder a la quimioterapia. Para pacientes y familias, ese conocimiento podría en el futuro ayudar a personalizar el tratamiento en lugar de recurrir a un enfoque único para todos.
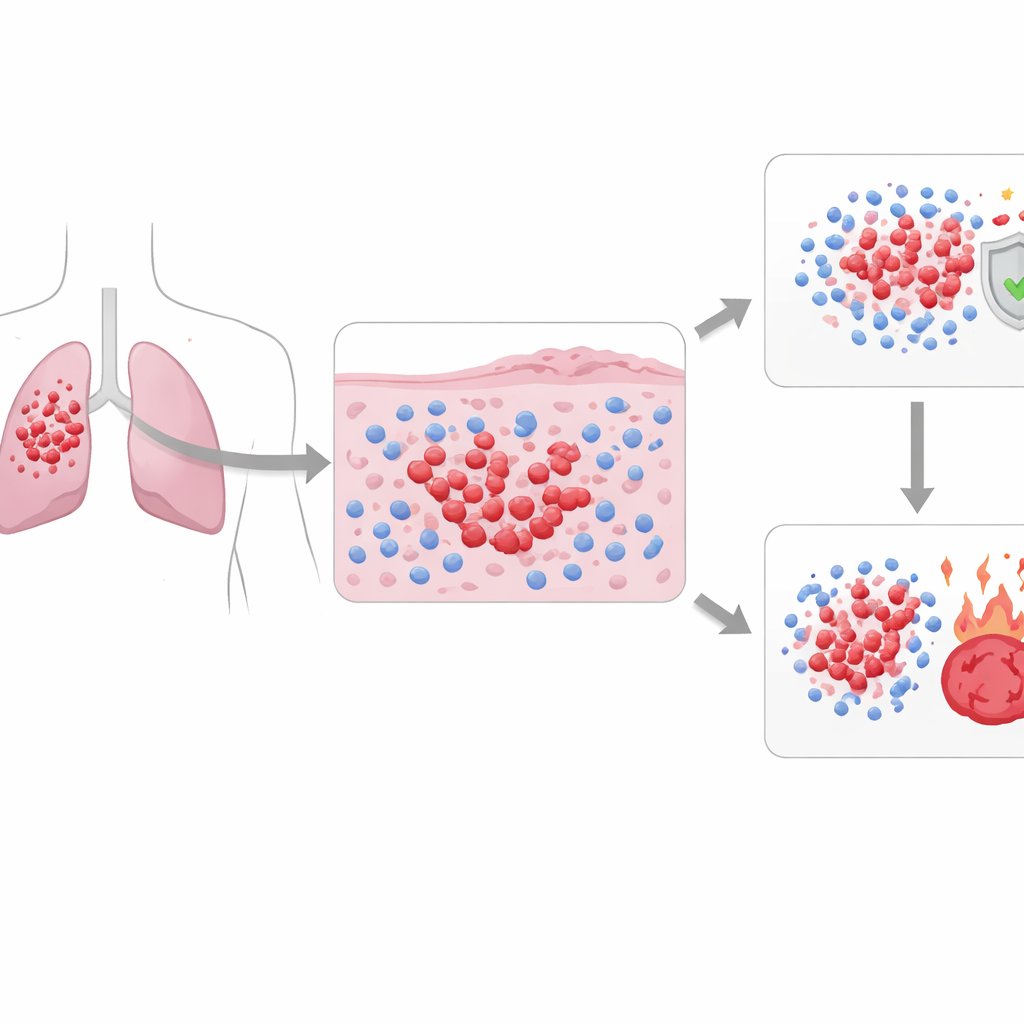
Mirando más de cerca un cáncer de pulmón letal
El cáncer de pulmón de células pequeñas representa alrededor del 15 % de los cánceres de pulmón, pero provoca una gran proporción de las muertes porque crece y se disemina rápidamente. Suele dividirse en enfermedad “limitada”, que puede abarcarse en un único campo de radiación, y enfermedad “extensa”, que se ha diseminado más ampliamente. El tratamiento inicial estándar incluye quimioterapia potente a base de platino, a veces combinada con inmunoterapia. Muchos tumores parecen desaparecer al principio, pero el cáncer suele volver en menos de un año, y menos de uno de cada diez pacientes sobrevive a largo plazo. Las pruebas actuales basadas en el tamaño tumoral, la diseminación y el aspecto microscópico básico no capturan por qué algunos pacientes responden mejor que otros a los mismos fármacos.
Enseñar a los ordenadores a leer los vecindarios tumorales
Los investigadores desarrollaron PhenopyCell para convertir las láminas de tejido teñido estándar en un mapa detallado de “vecindarios” celulares. Usando herramientas de aprendizaje profundo ya existentes, enseñaron primero a un ordenador a localizar y marcar células tumorales individuales y células inmunitarias en imágenes digitales de biopsias de 281 pacientes tratados en tres centros de EE. UU. A continuación, dividieron cada lámina en regiones tumorales, tejido cercano y zonas no tumorales distantes, y calcularon más de cien características numéricas. Estas características describen, por ejemplo, cuán densamente se agrupan las células inmunitarias alrededor de los racimos tumorales, a qué distancia se sitúan las células inmunitarias de las células cancerosas, cuán diversa es la mezcla de células y con qué regularidad están dispuestas a lo largo de la lámina.
Patrones ocultos vinculados a supervivencia y respuesta a fármacos
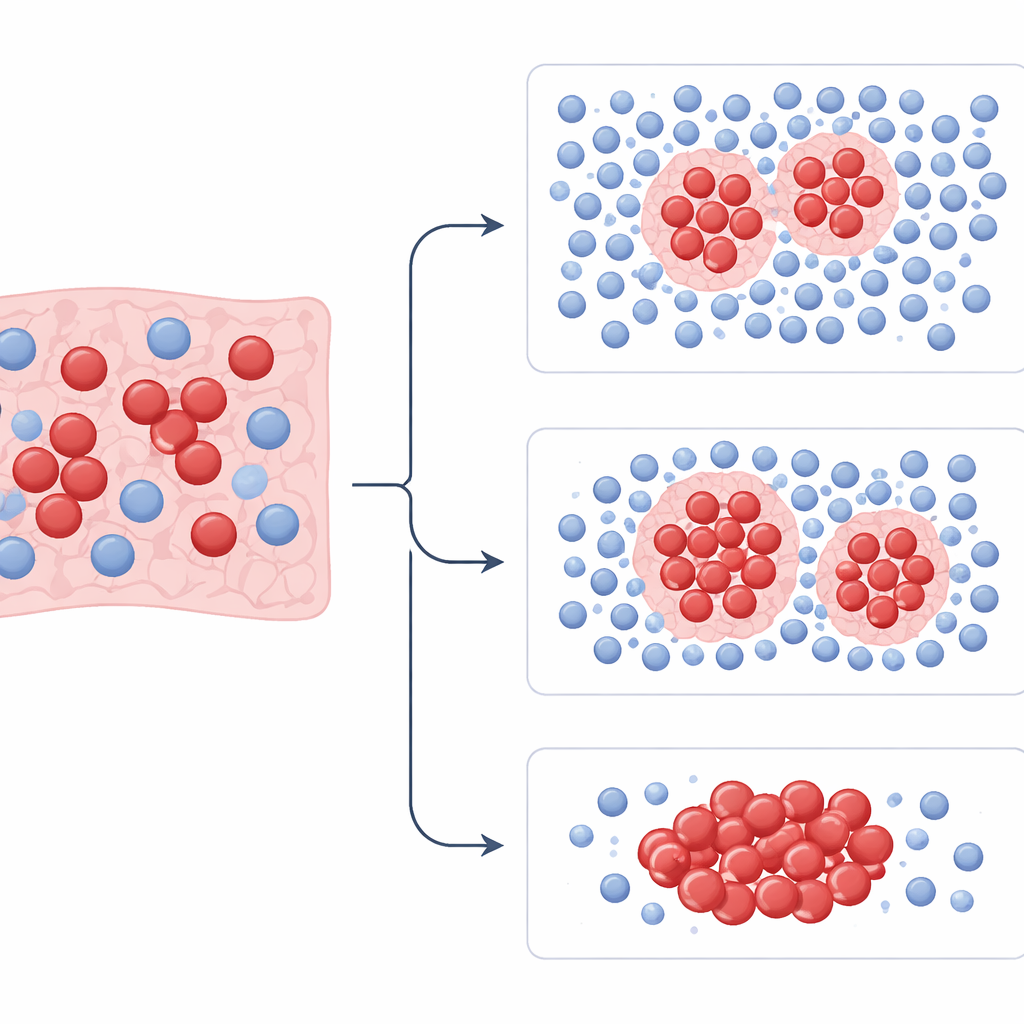
Con estas mediciones en mano, el equipo entrenó modelos para separar a los pacientes en grupos de mayor y menor riesgo y para predecir quién respondería a la quimioterapia con platino. Entrenaron los modelos con los casos de un hospital y luego los probaron en pacientes de los otros dos centros. En todos los conjuntos de datos, los patrones capturados por PhenopyCell se asociaron de forma significativa con la supervivencia global y con la eficacia de la quimioterapia. Los pacientes cuyos tumores mostraban muchos focos organizados de células inmunitarias rodeando de forma compacta los racimos tumorales tendían a vivir más. Aquellos con células inmunitarias dispersas o escasas y una distribución tumoral muy desigual eran más propensos a tener una enfermedad agresiva y malos resultados. Estos vínculos se mantenían aun al controlar la edad, el sexo y otros factores clínicos, y se observaron tanto en estadios limitados como extensos de la enfermedad.
Más allá de las cajas negras y las revisiones rutinarias al microscopio
El estudio también comparó a PhenopyCell con modelos de inteligencia artificial “foundation” más recientes y con medidas tradicionales de células inmunitarias llamadas linfocitos infiltrantes de tumor. Algunos modelos grandes de aprendizaje profundo alcanzaron alta precisión en el grupo de entrenamiento original, pero rindieron de forma inconsistente cuando se probaron con pacientes externos, lo que plantea dudas sobre su estabilidad. Los recuentos sencillos de células inmunitarias, ya sea estimados por ordenador o valorados por un patólogo, tampoco predecían la supervivencia de forma fiable. En contraste, el enfoque de PhenopyCell en cómo se disponen espacialmente las células inmunes y tumorales, no solo en cuántas hay, proporcionó señales más fiables y más fáciles de interpretar. Las características que utiliza pueden relacionarse directamente con conceptos biológicos como la exclusión inmune, áreas de tejido necrótico y formas tumorales variables.
Qué podría significar esto para los pacientes
Para un público no especializado, el mensaje principal es que la “arquitectura” de un tumor —cómo se distribuyen las células cancerosas y los defensores del organismo en el campo de batalla— contiene pistas importantes sobre cómo se comportará la enfermedad y cómo responderá al tratamiento. PhenopyCell demuestra que esas pistas pueden extraerse de las mismas láminas de biopsia de rutina que ya se obtienen en la atención estándar, sin procedimientos adicionales. Aunque el estudio es retrospectivo y se basa principalmente en pacientes que recibieron solo quimioterapia, sugiere que en el futuro estas herramientas podrían ayudar a los médicos a identificar qué pacientes tienen mayor riesgo, quién podría beneficiarse de tratamientos más agresivos o novedosos y quién podría evitar efectos secundarios innecesarios. Serán necesarios estudios prospectivos y de mayor tamaño, especialmente en pacientes que reciben inmunoterapias modernas, antes de que un sistema así pueda guiar decisiones cotidianas, pero este trabajo traza un camino claro hacia una atención más personalizada en el cáncer de pulmón de células pequeñas.
Cita: Barrera, C., Jain, P., Corredor, G. et al. Computational pathology features of immune architecture predict clinically relevant outcomes in small-cell lung cancer (SCLC). npj Precis. Onc. 10, 119 (2026). https://doi.org/10.1038/s41698-025-01225-9
Palabras clave: cáncer de pulmón de células pequeñas, patología computacional, microambiente tumoral, arquitectura de células inmunitarias, predicción de respuesta al tratamiento