Clear Sky Science · es
Métodos para la evaluación aleatorizada, ciega y controlada de supuestas intervenciones contra la enfermedad en redes multilaboratorio de evaluación preclínica
Por qué importa esto para la salud cotidiana
Muchos tratamientos médicos prometedores parecen eficaces en estudios con animales, pero luego fracasan en costosos ensayos clínicos a gran escala. Este artículo muestra, con detalle concreto, cómo los científicos pueden rediseñar esas primeras pruebas en animales para que sus resultados sean más fiables y más capaces de predecir lo que ocurrirá en pacientes reales: tomando el ictus como caso de prueba. 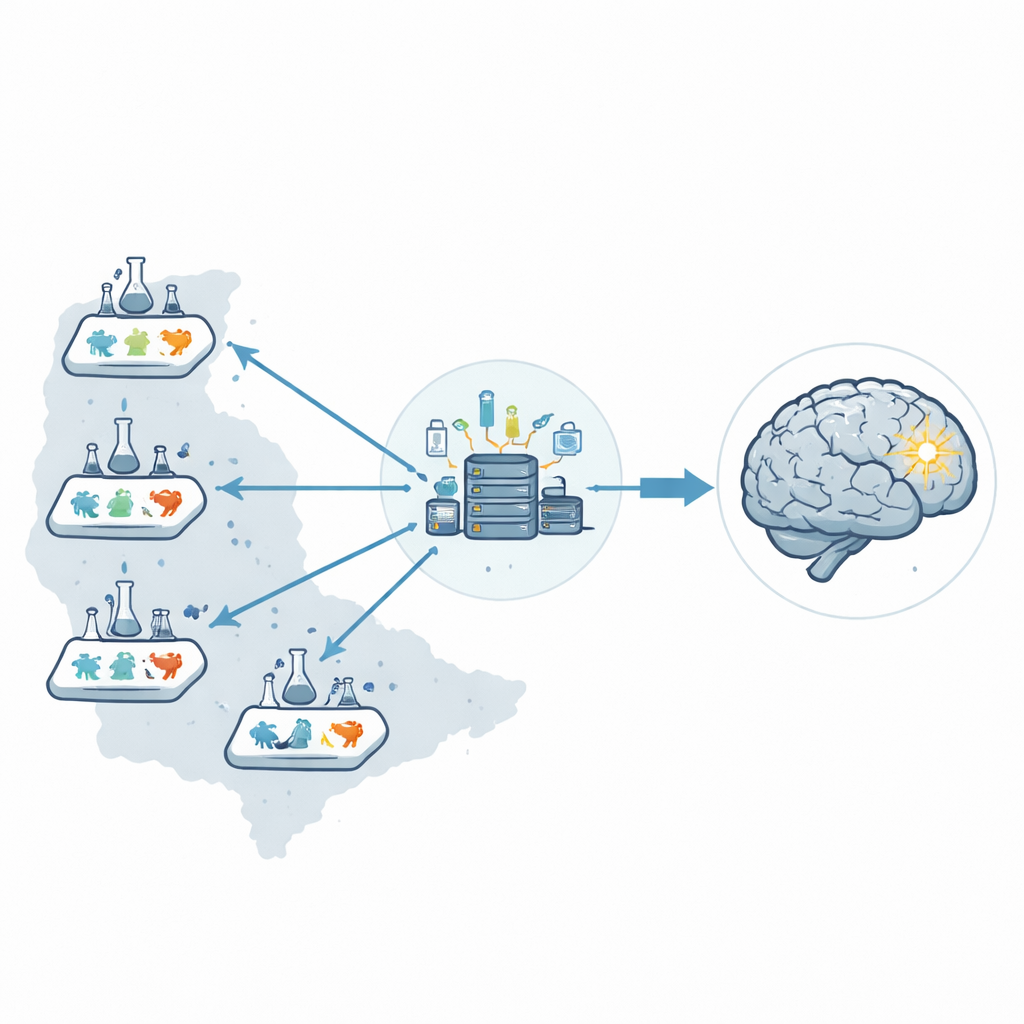
Construir una red en vez de depender de un solo laboratorio
En lugar de confiar en un único laboratorio, los investigadores crearon una red preclínica de seis laboratorios en Estados Unidos, denominada Stroke Preclinical Assessment Network. Un centro coordinador central gestionó toda la operación: enviar viales codificados de fármaco, asignar los tratamientos al azar, recibir todos los datos y ejecutar los análisis estadísticos. Al separar esas funciones de quienes realizaban las cirugías o evaluaban los resultados, redujeron la posibilidad de que las expectativas humanas influyeran sutilmente en los resultados.
Implementar imparcialidad y ocultamiento
Para imitar las normas de un buen ensayo clínico, cada animal fue inscrito, etiquetado y seguido desde el momento en que llegó al laboratorio. Los tratamientos se ocultaron en viales idénticos para que los cirujanos no pudieran distinguir los fármacos reales de los placebos mientras inducían el ictus y administraban la terapia. Un plan de aleatorización estructurado garantizó que machos y hembras, distintos modelos de ictus y los seis centros contribuyeran de forma equilibrada a cada grupo de tratamiento. Incluso si un animal murió o un procedimiento falló, permanecía en el registro para que las pérdidas no pudieran ignorarse discretamente, ayudando a evitar sesgos ocultos.
Probar tratamientos en modelos de ictus realistas
La red empleó cinco modelos diferentes de roedores que, en conjunto, capturaron aspectos importantes del ictus humano, incluidos la edad, la hipertensión y la obesidad inducida por la dieta. El ictus se produjo de la misma manera en todos los sitios, bloqueando brevemente una arteria cerebral principal y luego restaurando el flujo sanguíneo—similar a los procedimientos modernos de extracción de coágulos en personas. Los animales recibieron uno de seis tratamientos protectores candidatos o un control coincidente. El equipo los siguió con pruebas simples de movimiento, como cómo giraban en una esquina o caminaban sobre una rejilla, y con exploraciones cerebrales para medir el tamaño de la lesión durante 30 días.
Calificación a ciegas, datos compartidos y estadística inteligente
Para mantener los juicios imparciales, las pruebas de comportamiento se grabaron en vídeo y se cargaron en un archivo central. Estos vídeos, despojados de cualquier información identificativa, se enviaron a calificadores entrenados en otros laboratorios, que los puntuaron sin saber qué tratamiento había recibido el animal ni dónde se había probado. Las imágenes por resonancia magnética se procesaron mediante una canalización de análisis automatizada que segmentó el cerebro y el área lesionada con intervención humana mínima. Todos los resultados se integraron en un diseño estadístico multi brazo y multi etapa que permitió evaluar varios tratamientos en paralelo: los candidatos débiles o claramente ineficaces podían descartarse tempranamente, mientras que los prometedores avanzaban a etapas posteriores. 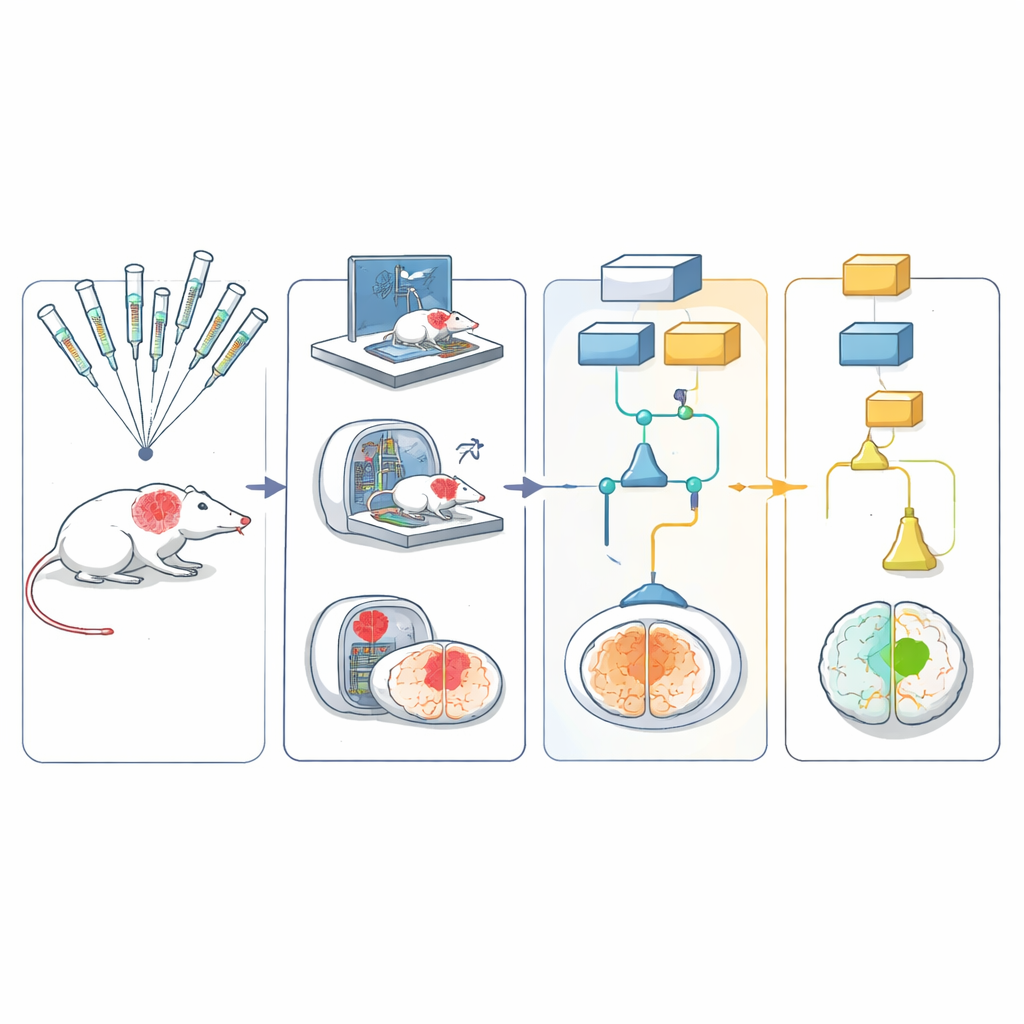
Qué mostraron los resultados sobre las terapias para el ictus
A lo largo de cuatro etapas y 2.615 animales, el sistema demostró ser operativo incluso durante las disrupciones por la pandemia de COVID-19. Los métodos mantuvieron consistentemente el equilibrio entre los grupos de tratamiento, minimizaron los errores en la dosificación y mostraron una mejora en la calidad de los datos a medida que los centros progresaban en la curva de aprendizaje. Al final, cinco de los seis tratamientos fueron descartados, mientras que uno—ácido úrico, un captador de radicales libres—cumplió el umbral preestablecido de beneficio. Al mismo tiempo, el trabajo expuso limitaciones de algunos modelos populares, como tasas de mortalidad muy altas en ratones envejecidos, lo que sugiere que pueden no ser prácticos ni realistas para estudios futuros.
Panorama general: un modelo para una ciencia preclínica más fiable
Para un lector no especializado, el mensaje clave es que cómo probamos tratamientos en animales importa tanto como qué probamos. Al incorporar las salvaguardias de los ensayos clínicos modernos—aleatorización, enmascaramiento, contabilización completa de cada sujeto y estadísticas cuidadosas—en la investigación con animales, esta red demuestra que los estudios iniciales pueden ser a la vez más rigurosos y más eficientes. El manual detallado que proporcionan puede adaptarse a otras enfermedades, ofreciendo un camino hacia hallazgos de laboratorio que resistan la replicación y den a médicos, pacientes y financiadores mayor confianza de que una terapia realmente tiene opciones de funcionar en la clínica.
Cita: Lamb, J., Nagarkatti, K., Diniz, M.A. et al. Methods for randomized, blinded, controlled evaluation of putative disease interventions in multilaboratory, preclinical assessment networks. Lab Anim 55, 74–82 (2026). https://doi.org/10.1038/s41684-026-01683-z
Palabras clave: ictus, ensayos preclínicos, modelos animales, rigor de la investigación, estudios multicéntricos