Clear Sky Science · es
Transgénesis mediada por PiggyBac y eliminación por CRISPR–Cas9 en la polilla de la cera mayor, Galleria mellonella
Una pequeña oruga con gran potencial médico
Imagínese testar nuevos antibióticos o estudiar infecciones peligrosas sin usar ratones u otros mamíferos. Las larvas de la polilla de la cera mayor, Galleria mellonella, están emergiendo como un sustituto de bajo coste y éticamente atractivo para esos experimentos. Este estudio muestra cómo los científicos han dado un paso importante al dotar a estas orugas de las mismas herramientas genéticas que convirtieron a la mosca de la fruta y al pez cebra en modelos tan potentes para la investigación biomédica.
Por qué este insecto importa para la salud humana
Las larvas de Galleria mellonella imitan sorprendentemente bien cómo responde el cuerpo humano a los gérmenes. Pueden mantenerse a 37 °C —nuestra temperatura corporal— y pueden infectarse con una amplia gama de bacterias y hongos de importancia médica. Cuando se enferman, su cuerpo se oscurece mediante un proceso llamado melanización, lo que proporciona a los investigadores una lectura visible del estado de salud. Al ser invertebrados, evitan muchos de los obstáculos legales y éticos asociados al trabajo con vertebrados, y son económicos de criar en gran número. Incluso se ha observado que las larvas degradan plásticos comunes, lo que sugiere aplicaciones también en investigación ambiental.
La caja de herramientas genética que faltaba
A pesar de estas ventajas, a las larvas de la polilla de la cera les han faltado los trucos genéticos sofisticados disponibles en animales de laboratorio clásicos. En la última década, varios equipos han secuenciado el genoma de la polilla y catalogado sus genes y proteínas activos, pero los investigadores aún no podían activar o desactivar genes con facilidad ni añadir marcadores útiles. Esa carencia ha limitado lo que se podía hacer con el modelo —por ejemplo, crear animales que se iluminen al infectarse o eliminar genes específicos para probar cómo afectan a la inmunidad. El artículo actual afronta este problema adaptando dos potentes sistemas de ingeniería genética, conocidos como PiggyBac y CRISPR–Cas9, para su uso en Galleria mellonella.
Construir larvas informadoras que brillen en la oscuridad
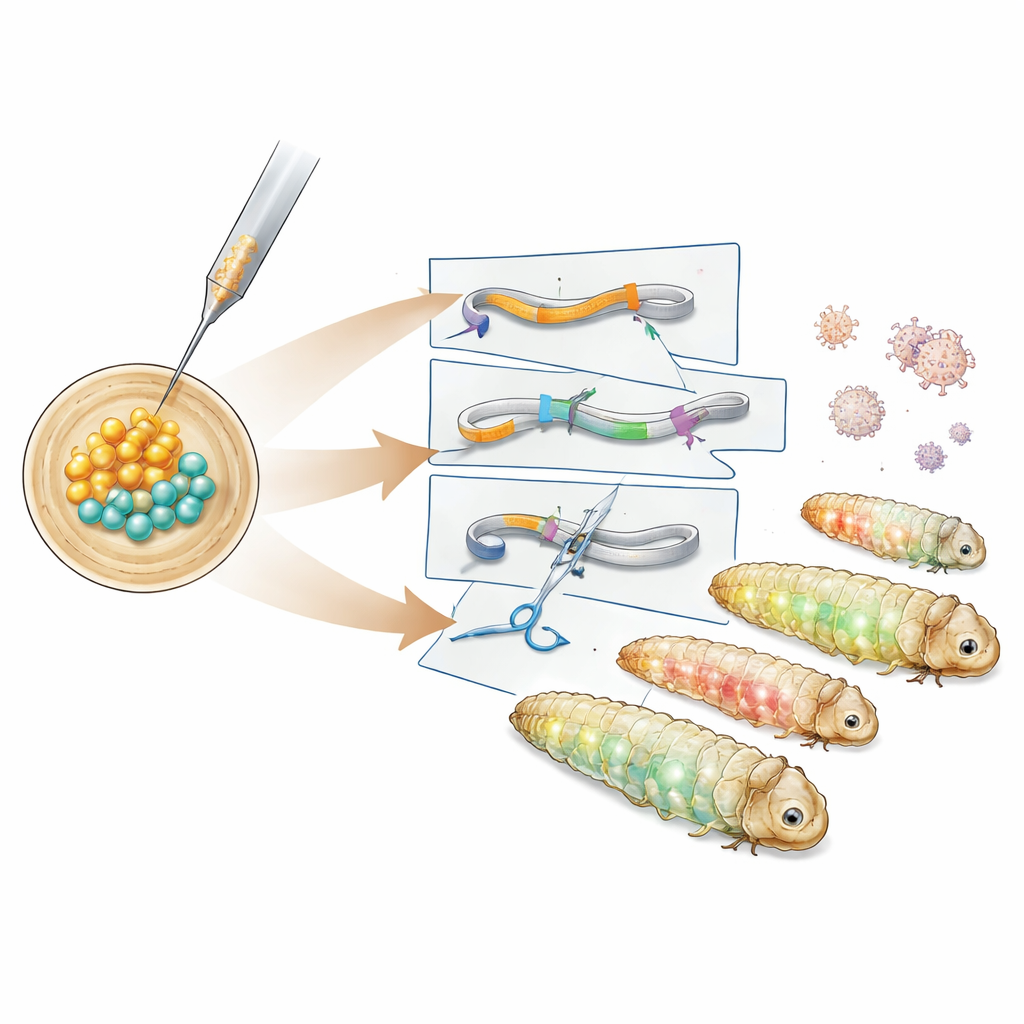
El equipo estudió primero el momento del desarrollo embrionario temprano de la polilla y encontró una ventana de aproximadamente seis horas tras la puesta de los huevos en la que todos los núcleos en división aún comparten un citoplasma común. Inyectar ADN durante ese periodo permite que el material genético nuevo se distribuya a todos los tejidos posteriores, incluidos los futuros espermatozoides y óvulos. Utilizando esta ventana, los investigadores introdujeron constructos de ADN basados en el transposón PiggyBac, un elemento “cortar‑y‑pegar” que inserta fragmentos grandes de ADN en el genoma. Tras probar distintos plasmidios ayudantes, identificaron una versión que llevaba una enzima PiggyBac hiperactiva y que produjo líneas transgénicas con éxito. Estas larvas expresaron proteínas fluorescentes verdes y rojas en tejidos corporales distintos, y el análisis del ADN mostró que la casete genética se insertó en un tramo inocuo entre genes nativos.
Observar células y eliminar genes
A continuación, los autores crearon líneas informadoras más especializadas. Un constructo etiquetó una proteína estructural llamada tubulina con fluorescencia verde para resaltar el armazón interno de la célula, mientras que otro fusionó un marcador rojo con una histona, proteína que empaqueta el ADN en el núcleo. Estas líneas brillaron en patrones característicos a lo largo del intestino, el tejido adiposo, las glándulas de seda y otros tejidos, permitiendo a los investigadores visualizar estructuras celulares en larvas vivas o fijadas. Para ir más allá de añadir genes y realmente desactivarlos, el equipo recurrió a CRISPR–Cas9. Inyectaron complejos proteína‑ARN de CRISPR preensamblados dirigidos al marcador verde fluorescente en embriones que ya portaban la casete informadora. Muchos descendientes mostraron pérdida parcial o total de la señal verde mientras conservaban la fluorescencia roja en los ojos, y la secuenciación del ADN confirmó pequeñas inserciones y deleciones en el sitio de corte previsto por CRISPR.
De un avance técnico a un impacto práctico
Aunque la eficiencia tanto de PiggyBac como de CRISPR en estas polillas sigue siendo modesta en comparación con algunos otros insectos, los autores describen vías claras de mejora ajustando promotores, variantes enzimáticas y estrategias de inyección. Incluso en su forma actual, la caja de herramientas es lo bastante potente para generar líneas estables que visualicen componentes celulares clave o que porten eliminaciones génicas dirigidas. Para los no especialistas, lo esencial es que Galleria mellonella puede ahora ser manipulado casi con la misma flexibilidad que animales de laboratorio mejor conocidos. Eso significa que los investigadores pueden crear orugas que informen sobre la infección, modelar aspectos de enfermedades humanas o testar nuevos fármacos de maneras más rápidas, baratas y humanas, lo que podría reducir la dependencia de modelos mamíferos en la biología de la infección y campos relacionados.
Cita: Pearce, J.C., Campbell, J.S., Prior, J.L. et al. PiggyBac-mediated transgenesis and CRISPR–Cas9 knockout in the greater wax moth, Galleria mellonella. Lab Anim 55, 95–102 (2026). https://doi.org/10.1038/s41684-025-01665-7
Palabras clave: Galleria mellonella, modelo de infección de invertebrados, ingeniería genética, transgénesis PiggyBac, eliminaciones CRISPR