Clear Sky Science · es
Formación multifásica mejorada de nitrato y sulfato particulado impulsada por NO2 en condiciones de alta humedad
Por qué el aire húmedo puede seguir estando sucio
Mucha gente imagina que el tiempo húmedo y brumoso ayuda a limpiar el aire, lavando la contaminación del cielo. Pero en el sur de China ocurre a menudo lo contrario: cuando el aire cálido y húmedo del océano se encuentra con aire continental más frío, se forman neblinas densas aunque los limpiadores atmosféricos tradicionales sean débiles. Este estudio explica por qué, revelando cómo un contaminante común del tráfico, el dióxido de nitrógeno, impulsa de forma silenciosa la rápida formación de partículas finas nocivas cuando el aire es muy húmedo.
Aire pegajoso sobre una ciudad costera
Los investigadores se centraron en Xiamen, una ciudad costera del sur de China, durante dos semanas a principios de la primavera de 2024. En esa época del año, el aire cálido y húmedo del océano con frecuencia choca con el aire continental más frío y seco y se queda estacionario, creando frentes meteorológicos cuasiestacionarios. Durante estos episodios de alta humedad, el aire se vuelve estancado, la velocidad del viento disminuye y una capa de aire poco profunda se asienta sobre la ciudad. Las mediciones desde una estación en la azotea mostraron que los niveles de partículas finas (PM2,5) aumentaron, la visibilidad empeoró y con frecuencia se formó niebla a medida que subía la humedad. Dentro de estos periodos brumosos, la composición química de las partículas cambió en dos etapas claras: primero dominó el nitrato y luego se disparó el sulfato.
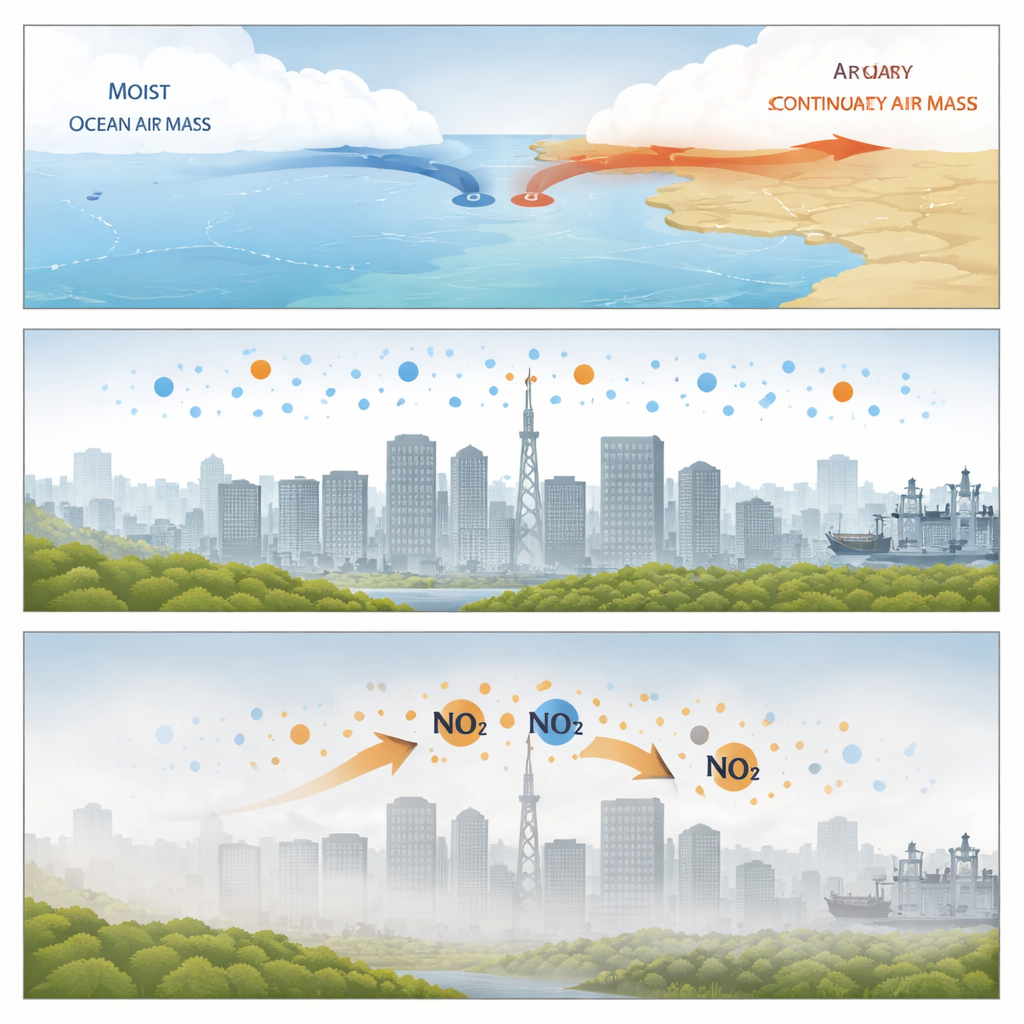
Dos fases de química oculta
En las primeras horas, muy húmedas, de estos episodios, las partículas se enriquecieron en nitrato, aunque la química habitual impulsada por la luz solar era débil y los niveles de ozono eran bajos. El equipo encontró que la mejor explicación era que el dióxido de nitrógeno procedente del tráfico y otras fuentes se estaba incorporando directamente en las superficies húmedas de las partículas y en las finas películas de agua sobre el suelo. En estas gotas concentradas, el dióxido de nitrógeno reacciona más rápido que en agua ordinaria, produciendo tanto nitrato como otra forma reactiva de nitrógeno que puede volver a escapar al aire. El vínculo estrecho entre el dióxido de nitrógeno, el agua en los aerosoles, el área superficial de las partículas y el aumento del nitrato sugirió que estos procesos superficiales dominaban la producción de nitrato durante la noche.
Cuando la niebla convierte el nitrógeno en partículas de azufre
A medida que la humedad aumentó aún más y se formó niebla, la química cambió. El sulfato, formado a partir del dióxido de azufre, comenzó a crecer rápidamente e incluso pudo superar al nitrato. De nuevo, el dióxido de nitrógeno desempeñó un papel central, pero de una manera diferente. Dentro de la niebla y de las gotas grandes, el dióxido de nitrógeno y sus productos de reacción oxidaron el azufre disuelto en una serie de reacciones en fase acuosa. Un intermedio clave, una especie reactiva de nitrógeno que mantiene un equilibrio con el ácido nitroso, se encontró que permanece más tiempo dentro de gotas más grandes y menos ácidas que en partículas diminutas y más ácidas. Este mayor tiempo de permanencia le permitió atacar repetidamente al azufre disuelto, impulsando la rápida producción de sulfato precisamente cuando estaban presentes niebla densa y bruma.
Poner cifras a lo invisible
Para probar estas ideas, los autores construyeron un detallado “modelo de caja” por ordenador que combinó la química en fase gaseosa, las reacciones en agua líquida y los intercambios entre el aire y las partículas. Cuando permitieron la captación de dióxido de nitrógeno por partículas húmedas y gotas de niebla, el modelo reprodujo de forma cercana los aumentos observados de nitrato y sulfato. Durante los episodios húmedos, la incorporación directa de dióxido de nitrógeno representó casi la mitad de todo el nitrato formado, y los oxidantes a base de nitrógeno (dióxido de nitrógeno más sus productos acuosos) produjeron casi dos tercios del sulfato. Durante la noche, la vía del dióxido de nitrógeno superó con creces a la ruta más familiar que implica a otro oxidante nocturno, el pentóxido de dinitrógeno. El modelo también mostró que las gotas de niebla, con su mayor tamaño y pH más alto, son reactores especialmente favorables para la química nitrógeno–azufre que genera sulfato.
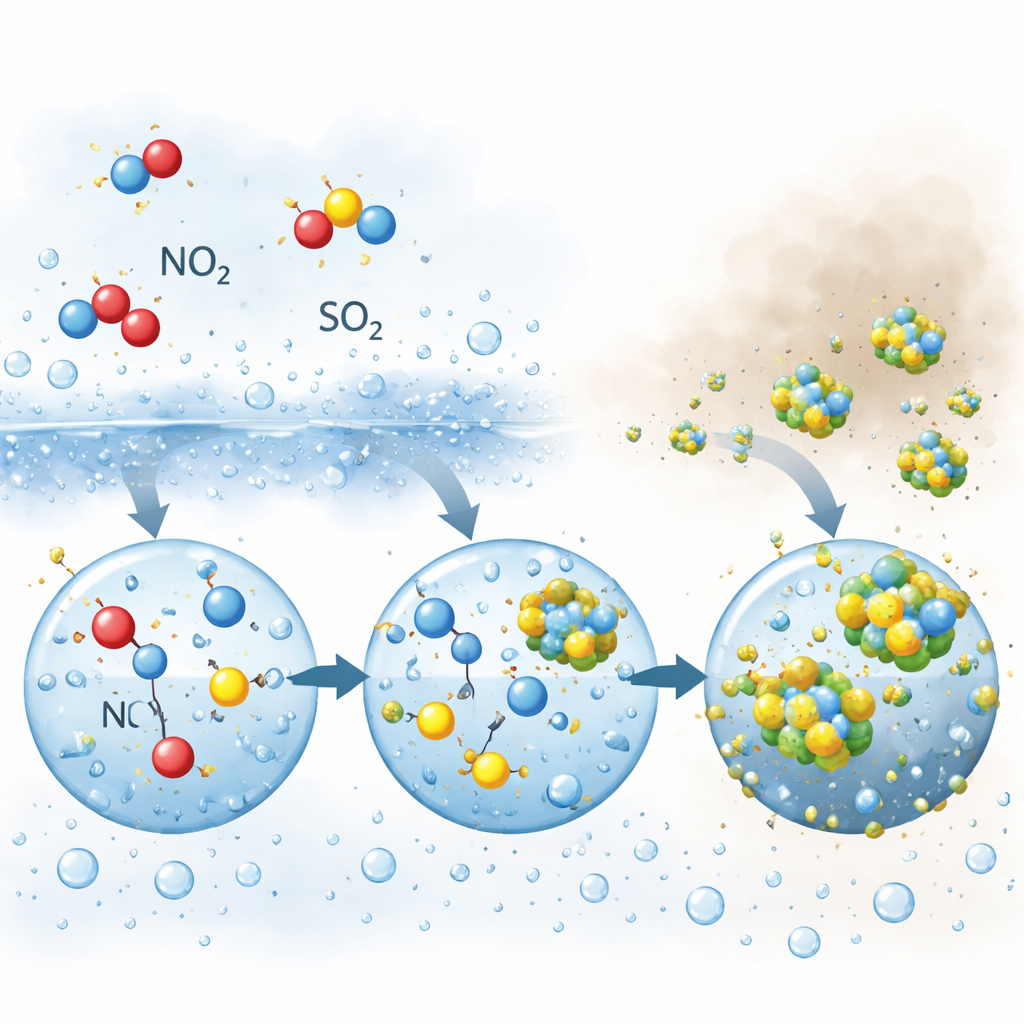
Qué significa esto para un aire más limpio
El estudio concluye que el dióxido de nitrógeno hace mucho más que servir como un gas indicador de la contaminación del tráfico: en condiciones muy húmedas y estancadas se convierte en un potente impulsor de la formación de partículas finas. Al acelerar la conversión del nitrógeno y el azufre gaseosos en partículas de nitrato y sulfato, estas reacciones ocultas en agua ayudan a explicar por qué los niveles de partículas no han disminuido tan rápido como las emisiones de gases de nitrógeno y azufre en China. Los hallazgos sugieren que el control efectivo del smog en regiones costeras y húmedas debe considerar no solo cuánto dióxido de nitrógeno se emite, sino también con qué frecuencia la atmósfera entra en estos estados pegajosos y brumosos que lo convierten en una fábrica química microscópica.
Cita: Lin, Z., Ji, X., Xu, L. et al. Enhanced NO2-driven multiphase formation of particulate nitrate and sulfate under high-humidity conditions. npj Clim Atmos Sci 9, 76 (2026). https://doi.org/10.1038/s41612-026-01352-5
Palabras clave: contaminación del aire, dióxido de nitrógeno, partículas finas, alta humedad, química de la niebla