Clear Sky Science · es
Apuntar al EGFR expresado en el cáncer con un anticuerpo monoclonal humanizado
Encontrar las banderas ocultas del cáncer
Los tratamientos contra el cáncer a menudo tienen dificultades para equilibrar el ataque a las células tumorales con la protección del tejido sano. Este artículo describe un nuevo anticuerpo diseñado en laboratorio, llamado A10, que puede distinguir las células cancerosas que portan una forma particular de un receptor de señal de crecimiento de las células normales. Al dirigirse a una conformación que aparece principalmente cuando este receptor está alterado o sobrerrepresentado en las células tumorales, A10 abre la puerta a terapias que son tanto poderosas como más selectivas que muchas opciones actuales.
Por qué importa este interruptor de crecimiento
Muchos tumores, incluidos los agresivos de cerebro, pulmón, mama y colon, dependen de una proteína de superficie llamada receptor del factor de crecimiento epidérmico (EGFR) para crecer y sobrevivir. Las células tumorales pueden aumentar este receptor amplificando su gen, mutándolo o produciendo una versión truncada y permanentemente activa conocida como EGFRvIII. Los fármacos estándar que bloquean EGFR a menudo afectan tanto a las células cancerosas como a los tejidos normales, porque reconocen partes del receptor que están presentes en todas partes. El equipo detrás de este estudio se centró, en cambio, en un pequeño lazo de EGFR que queda claramente expuesto principalmente en las células cancerosas—ya sea porque EGFR está presente en números anormalmente altos o porque el receptor está truncado en EGFRvIII. Ese lazo actúa como una “bandera” específica del cáncer que, en principio, puede atacarse con mayor seguridad.
Convertir un anticuerpo de ratón en un medicamento humano
Los investigadores habían descubierto previamente un anticuerpo de ratón, 40H3, que reconocía este lazo expuesto en el EGFR expresado por el cáncer. Sin embargo, los anticuerpos de ratón pueden desencadenar reacciones inmunitarias si se administran repetidamente a pacientes. Para superar esto, el equipo utilizó métodos de ingeniería de proteínas para injertar los segmentos clave de unión de 40H3 en andamiajes de anticuerpos humanos, generando catorce candidatos “humanizados” más una molécula de referencia quimérica. Cuando probaron estas variantes en células cancerosas que sobreproducen EGFR, tres versiones se unieron especialmente bien, y una—A10—sobresalió como la que más unía al tiempo que ignoraba las células normales con niveles modestos de EGFR. A lo largo de un amplio panel de líneas celulares tumorales con distintas mutaciones y números de copias de EGFR, A10 mostró de forma consistente una mayor unión que el anticuerpo original de ratón y mantuvo una fuerte preferencia por las células malignas.
Ver cómo el anticuerpo sujeta su objetivo
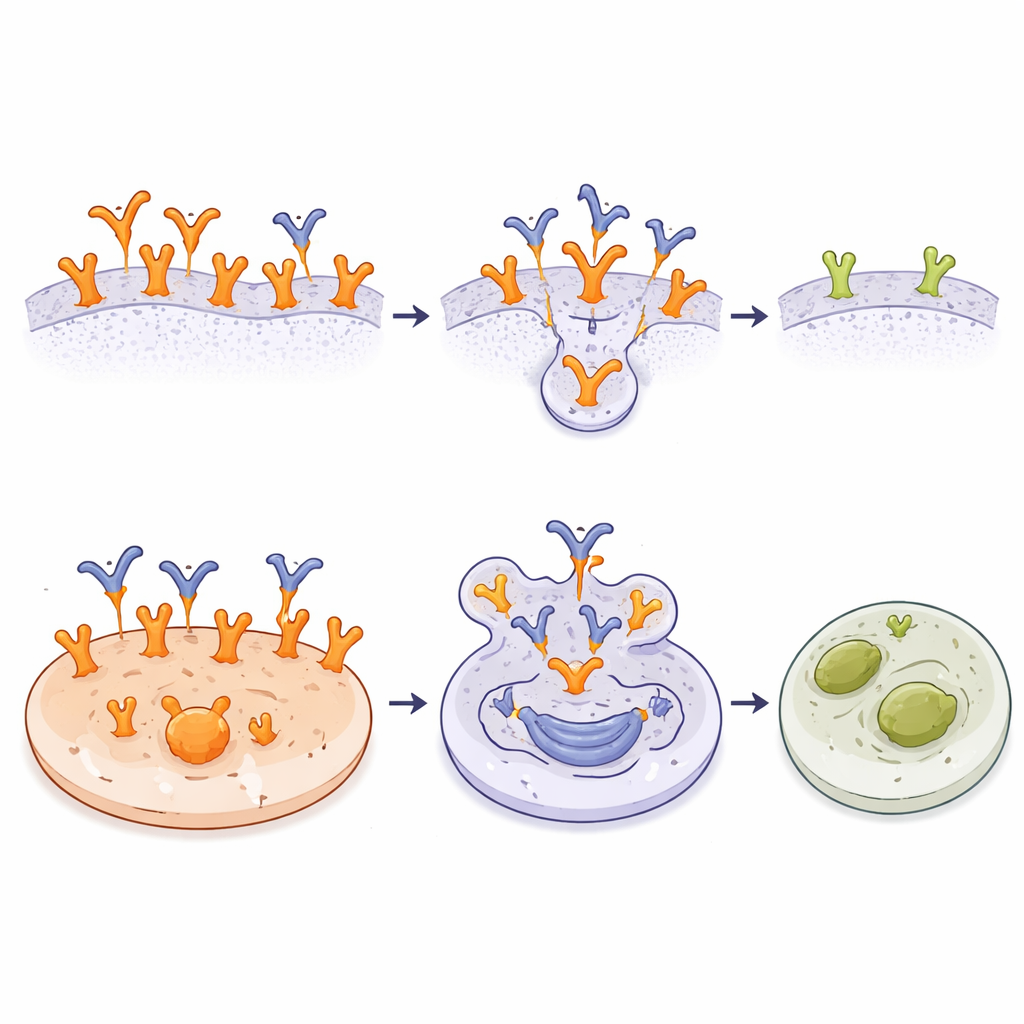
Para entender por qué A10 es tan selectivo, el equipo resolvió una estructura 3D de alta resolución de la parte activa del anticuerpo unida al lazo de EGFR. El lazo se pliega en una horquilla apretada estabilizada por un puente disulfuro, y A10 acuna esa conformación en una ranura formada entre sus dos brazos, con numerosos contactos cargados que la bloquean en su lugar. Comparar esta estructura con las formas conocidas de la molécula completa de EGFR reveló una idea clave: tanto en la forma inactiva “atada” como en el dímero activo del EGFR normal, el lazo está en gran medida enterrado o parcialmente protegido por dominios vecinos. Esto significa que A10 no puede alcanzar fácilmente su sitio de unión en receptores típicos expresados a niveles modestos. En contraste, en la variante específica del cáncer EGFRvIII falta la parte frontal del receptor, lo que deja el lazo altamente expuesto y accesible. Los datos sugieren que A10 reconoce principalmente a EGFR durante ciertas conformaciones transitorias y en formas sobresaturadas o truncadas que ocurren preferentemente en células tumorales.
Armar el anticuerpo para matar células tumorales
Reconocer una bandera específica del tumor es útil por sí solo, pero los investigadores fueron más allá al convertir A10 en un conjugado anticuerpo‑fármaco (ADC). Unieron químicamente un potente compuesto citotóxico, monometil auristatina E (MMAE), a A10 usando un enlazador que puede cortarse dentro de las células. Este ADC A10‑MMAE se unió a las células cancerosas igual de bien que el anticuerpo no conjugado. En pruebas de laboratorio en muchas líneas celulares, el ADC fue más eficaz contra tumores con niveles muy altos de EGFR o con EGFRvIII, donde A10 tenía abundantes sitios de unión. En estas células, cantidades minúsculas del conjugado fueron suficientes para desencadenar la muerte celular. Las líneas tumorales con menos blancos para A10 o con resistencia inherente a MMAE se vieron menos afectadas, y las células fibroblásticas normales con EGFR silvestre permanecieron indemnes a pesar de ser sensibles a MMAE libre. Los resultados muestran que la combinación de unión selectiva y liberación interna del fármaco puede enfocar de manera marcada la toxicidad sobre las células cancerosas.
Qué podría significar esto para la atención oncológica futura
En términos sencillos, este trabajo muestra que es posible construir un anticuerpo que “vea” EGFR solo cuando se parece y actúa como un receptor impulsor del cáncer, mientras que en gran medida ignora su forma cotidiana en los tejidos sanos. Al mapear exactamente cómo A10 sujeta un lazo oculto en EGFR y demostrar que un conjugado farmacológico basado en A10 puede matar de forma eficiente a células tumorales ricas en receptor y, al mismo tiempo, preservar las células normales, el estudio proporciona una base sólida para desarrollar terapias más seguras y altamente dirigidas. Si estos hallazgos se traducen a pacientes, los tratamientos futuros basados en A10 podrían llevar fármacos potentes directamente a los cánceres dependientes de EGFR dejando el resto del organismo en gran medida intacto.
Cita: Costa, T.G.F., Sarnovsky, R., Zhan, J. et al. Targeting cancer expressed EGFR with a humanized monoclonal antibody. Sci Rep 16, 10814 (2026). https://doi.org/10.1038/s41598-026-46245-y
Palabras clave: EGFR, conjugado anticuerpo‑fármaco, terapia oncológica dirigida, glioblastoma, EGFRvIII