Clear Sky Science · es
Perspectivas estructurales y mecanísticas sobre la diana de integrinas α2β1 y α5β1 por vesículas extracelulares bioingenierizadas procedentes de células de cáncer de pulmón
Los mensajeros ocultos del cáncer
El cáncer de pulmón suele detectarse en etapas avanzadas, cuando las opciones de tratamiento son limitadas. Una estrategia prometedora es administrar fármacos solo a las células tumorales, preservando el tejido sano. Este estudio explora un sistema de entrega natural y diminuto —las vesículas extracelulares, o VE— que las células cancerosas ya utilizan para enviar señales. Al reingenierizar estas vesículas con una corta etiqueta de direccionamiento, los investigadores demuestran cómo pueden anclarse a sitios de unión específicos en las células tumorales, sentando las bases para terapias contra el cáncer más precisas y menos tóxicas.
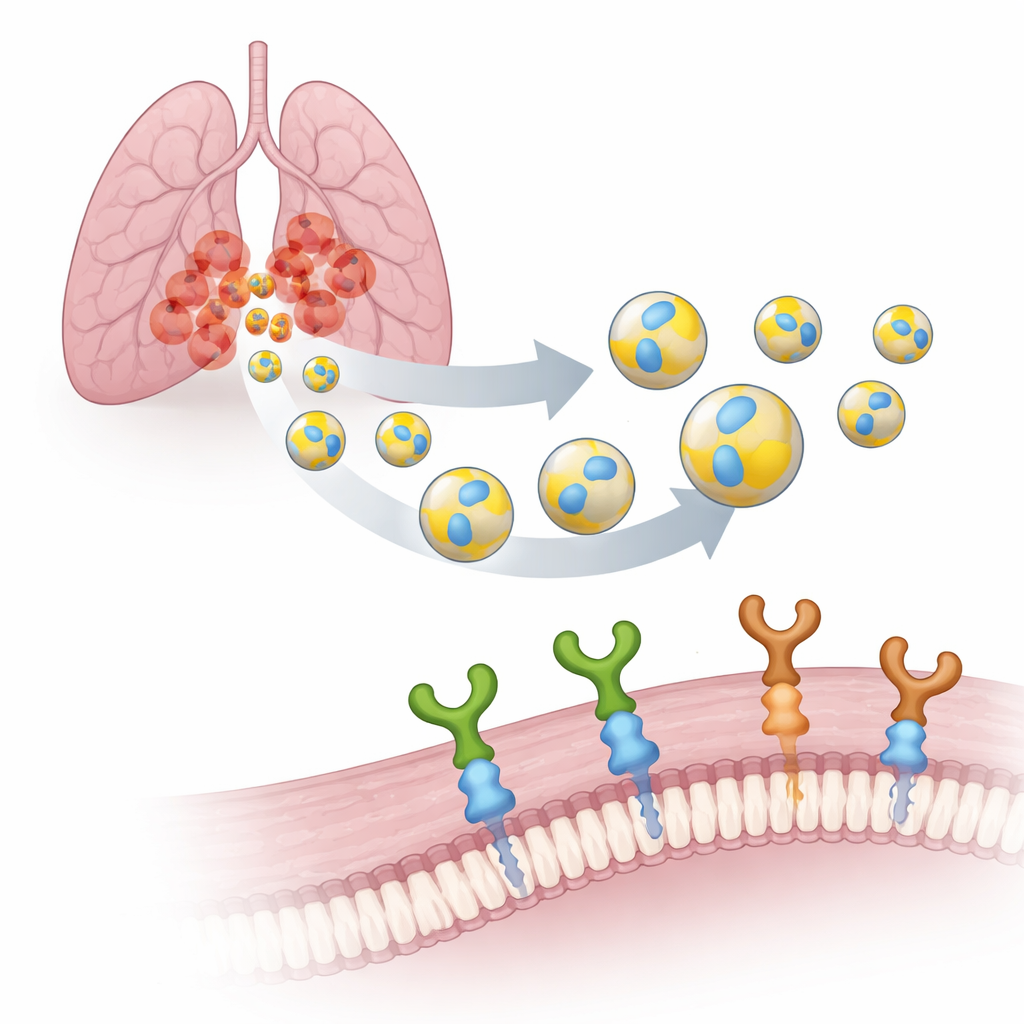
Convertir paquetes naturales en mensajeros inteligentes
Todas las células de nuestro cuerpo liberan VE: burbujas a escala nanométrica rodeadas por una membrana, algo así como pequeñas pompas de jabón microscópicas. Al estar fabricadas por nuestras propias células, las VE son biodegradables, atraviesan con facilidad barreras biológicas y son menos propensas a provocar efectos adversos que los transportadores sintéticos. El equipo se centró en VE producidas por células humanas de cáncer de pulmón (A549) y decoró su superficie con una pequeña etiqueta de siete bloques constructivos llamada PTHTRWA. Experimentos anteriores mostraron que esta etiqueta dirige las VE hacia las células de cáncer de pulmón en ratones, uniéndose con mucha más fuerza a las células tumorales que a las células pulmonares normales y manteniendo una toxicidad solo débil.
Encontrar los puertos de acoplamiento adecuados en las células tumorales
Para convertir estas vesículas etiquetadas en herramientas verdaderamente selectivas, los investigadores necesitaban identificar qué “puertos” en las células cancerosas reconocen. Analizaron dos receptores de superficie relacionados, las integrinas α2β1 y α5β1. Son ganchos moleculares que ayudan a las células a adherirse al entorno y a transmitir señales hacia el interior. En los tumores pulmonares, α5β1 se asocia fuertemente con comportamiento agresivo, diseminación y mal pronóstico, mientras que α2β1 se ha vinculado con resistencia a la quimioterapia. Usando una técnica sensible llamada resonancia de plasmones de superficie, el equipo comparó la fuerza con la que las VE decoradas con PTHTRWA se unen a ambas integrinas. Encontraron que las vesículas sin la etiqueta apenas interactuaban, mientras que las VE etiquetadas formaban complejos firmes y estables con ambos receptores en condiciones cercanas a las fisiológicas.
Acercándose al abrazo molecular
Para entender lo que ocurre átomo por átomo cuando la etiqueta encuentra las integrinas, los investigadores recurrieron a simulaciones por ordenador. Construyeron modelos tridimensionales de la etiqueta unida a regiones clave de las integrinas y permitieron que estos sistemas evolucionaran en agua virtual durante cientos de nanosegundos. Los cálculos mostraron que PTHTRWA encaja con precisión en una ranura poco profunda del receptor α2β1, formando una red de enlaces de hidrógeno y contactos hidrofóbicos que estabilizan el complejo. De manera crucial, la unión favoreció una conformación más “abierta” del receptor —su forma de alta afinidad y activada para señalizar— frente al estado “cerrado” de reposo. Cuando probaron versiones ligeramente modificadas de la etiqueta, observaron que pequeños ajustes químicos en un extremo pueden remodelar sutilmente cómo se acomoda el péptido en la ranura y cómo proclive es a preferir una integrina sobre la otra.
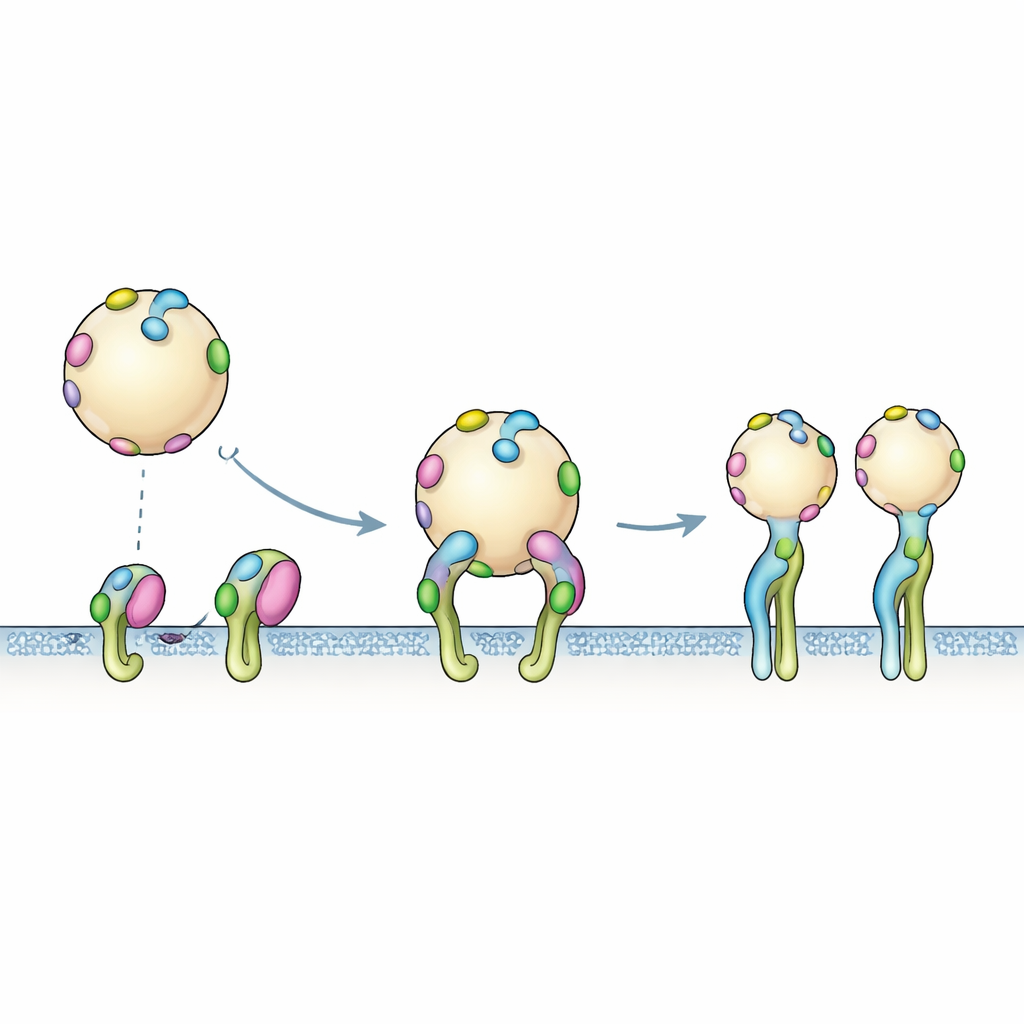
De etiquetas individuales a agarres multivalentes
Los modelos computacionales capturan una etiqueta tocando un receptor a la vez, pero la superficie real de las VE está cubierta por muchas copias de PTHTRWA. Los experimentos de unión reflejaron esta realidad multivalente: una vez que una vesícula etiquetada se acerca a un parche de integrinas, varias etiquetas pueden comprometerse simultáneamente. Los datos del sensor encajaron mejor con un proceso en dos pasos. Primero, la vesícula se acopla brevemente mediante encuentros rápidos y reversibles. Luego tiene lugar una reorganización más lenta en la que las integrinas pasan a su conformación abierta y el agarre global se estrecha. Este abrazo cooperativo de muchas manos explica por qué la fuerza aparente de unión de las vesículas completas es mayor que la que cabría predecir a partir de una sola etiqueta.
Qué podría significar esto para futuros tratamientos
En pocas palabras, el estudio muestra que las VE armadas con la etiqueta PTHTRWA pueden reconocer selectivamente integrinas que están sobreactivas en el cáncer de pulmón y que lo hacen empujando a estos receptores hacia una forma abierta y fuertemente unida. Al mapear estas interacciones en detalle, los investigadores ofrecen reglas de diseño para la próxima generación de transportadores basados en vesículas que podrían entregar fármacos, agentes de imagen u otras cargas directamente a células malignas mientras ignoran en gran medida el tejido sano. Aunque será necesario más trabajo en animales y en humanos, esta estrategia de direccionamiento de integrinas acerca un paso más la visión de una medicina personalizada contra el cáncer basada en VE.
Cita: Nowicka, A.M., Żołek, T., Kowalczyk, A. et al. Structural and mechanistic insights into α2β1 and α5β1 integrin targeting by bioengineered extracellular vesicles originating from lung cancer cells. Sci Rep 16, 10833 (2026). https://doi.org/10.1038/s41598-026-46071-2
Palabras clave: cáncer de pulmón, vesículas extracelulares, integrinas, administración dirigida de fármacos, simulaciones moleculares