Clear Sky Science · es
El compuesto fluoroquinolínico ejerce efectos anti-eritroleucémicos mediante la doble diana GLUT1 y la vía de señalización PI3K/AKT
Un nuevo ángulo sobre un cáncer sanguíneo peligroso
La eritroleucemia es una forma rara pero muy agresiva de cáncer de la sangre con pocas opciones de tratamiento más allá del trasplante de células madre. Para muchos pacientes, en su mayoría de edad avanzada, esto implica terapias duras, costes elevados y pronósticos sombríos. Este estudio explora un compuesto diseñado en laboratorio llamado FKL-137 que ataca las células de eritroleucemia de una manera inesperada: cortándoles su combustible preferido, el azúcar, y desencadenando su autodestrucción. El trabajo sugiere una posible nueva clase de fármacos dirigidos que explotan la dependencia de las células cancerosas de un uso energético alterado, al tiempo que preservan más del tejido sano.
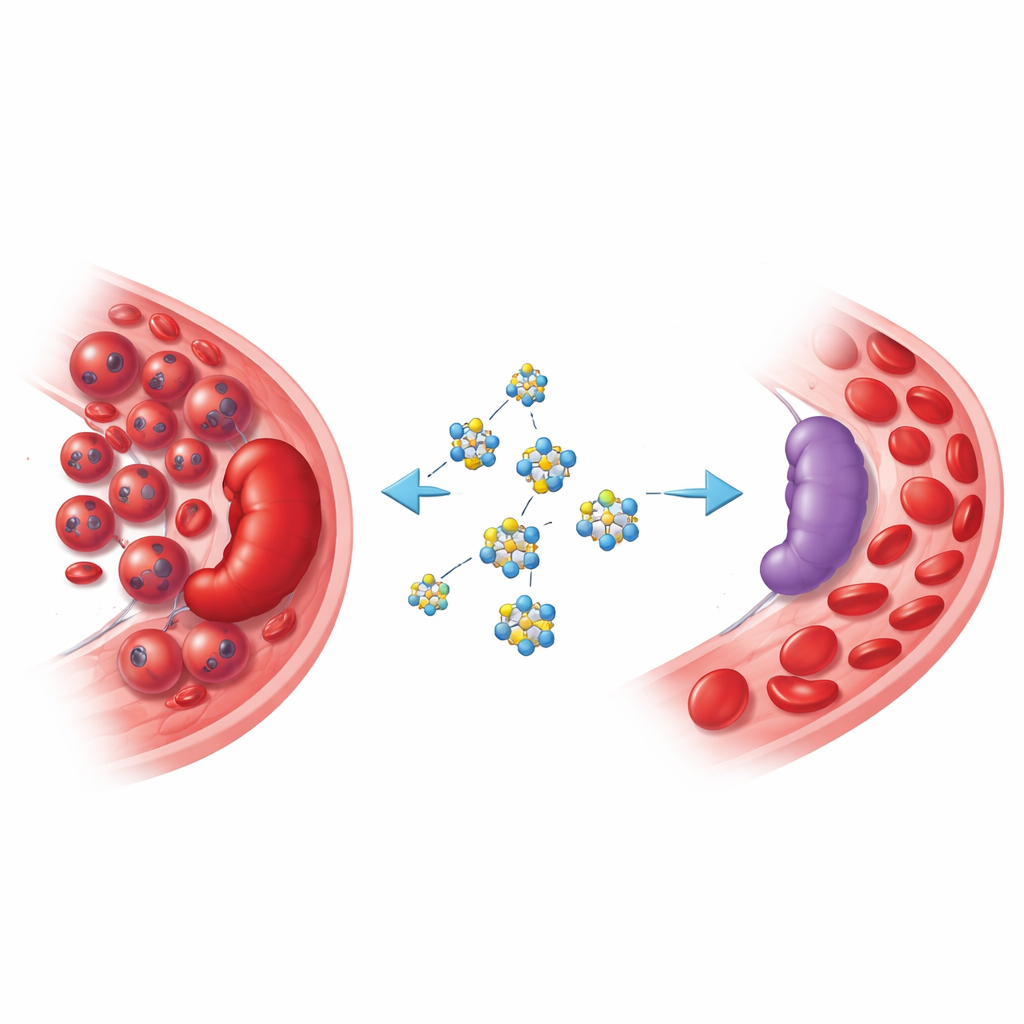
Cuando las células sanguíneas se rebelan
En la eritroleucemia, los precursores inmaduros de los glóbulos rojos proliferan sin control en la médula ósea y el bazo. Los pacientes pueden desarrollar anemia severa, bazo agrandado con riesgo de ruptura y un deterioro rápido de la salud. Las terapias actuales son limitadas y muchas personas son demasiado frágiles para tratamientos agresivos. Al mismo tiempo, los científicos han descubierto que muchos cánceres hematológicos dependen de un uso reprogramado de la glucosa: captan glucosa a altas tasas y la convierten rápidamente en energía y bloques de construcción, lo que les ayuda a multiplicarse y evadir al sistema inmune. Apuntar a esta “adicción” metabólica se ha convertido en una estrategia atractiva para nuevos fármacos.
Privar a las células cancerosas del azúcar
Los investigadores se centraron en una pequeña molécula sintética, FKL-137, derivada de una familia química ya conocida por su actividad anticancerígena. En experimentos de laboratorio, expusieron dos líneas celulares humanas de eritroleucemia a dosis crecientes de FKL-137. El compuesto ralentizó marcadamente el crecimiento celular con el tiempo y empujó a las células hacia la muerte programada, observada por cambios clásicos en la morfología celular y la activación de la maquinaria interna de muerte. De forma importante, FKL-137 fue mucho más potente contra las células leucémicas que frente a células hepáticas normales, y las medidas de seguridad farmacológica sugirieron una toxicidad relativamente baja a dosis eficaces.
Golpear las puertas del azúcar del cáncer
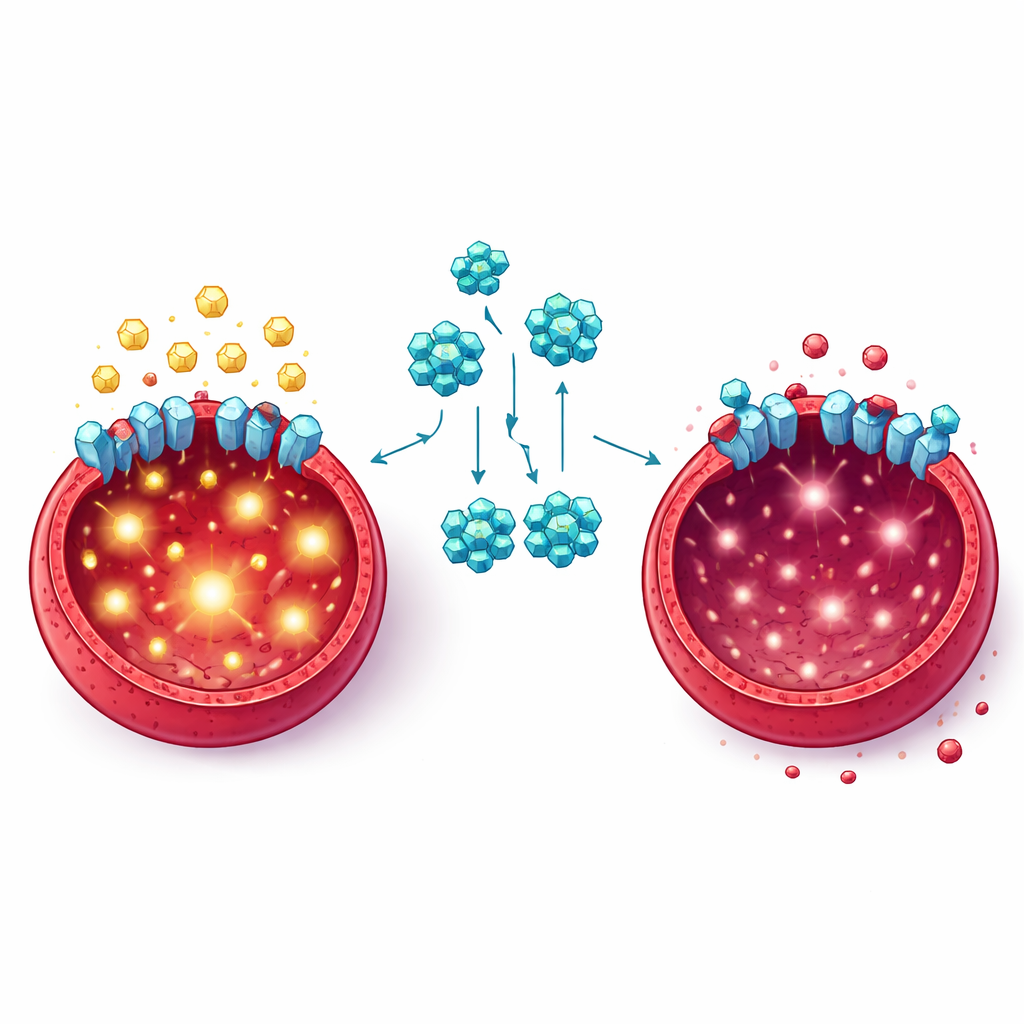
Profundizando en el mecanismo, el equipo investigó cómo FKL-137 interfiere con el metabolismo canceroso. Encontraron que las células leucémicas tratadas captaban menos glucosa y liberaban menos lactato, un subproducto de la intensa quema de azúcar. Proteínas clave que normalmente ayudan a convertir la glucosa en energía y componentes celulares estaban reducidas. Mediante modelado computacional, pruebas de estabilidad térmica e imagenología, los investigadores demostraron que FKL-137 se une a GLUT1, una de las principales “puertas” en la superficie celular que introduce glucosa al interior. Cuando los niveles de GLUT1 se redujeron por medios genéticos, las células leucémicas crecieron más despacio y usaron menos azúcar, además de volverse aún más sensibles a FKL-137. Esto confirmó que GLUT1 es tanto un impulsor del crecimiento de las células de eritroleucemia como un objetivo importante del fármaco.
Interrumpir un bucle de señalización de crecimiento
El estudio también reveló efectos más allá de la propia puerta de la glucosa. Las células de eritroleucemia normalmente emplean una vía de señalización conocida como PI3K/AKT para fomentar la supervivencia, el crecimiento y el alto consumo de glucosa, en parte apoyando a GLUT1. El tratamiento con FKL-137 redujo las formas activas de proteínas clave en esta vía, rompiendo un bucle reforzador entre el transporte de glucosa y las señales de crecimiento. En ratones infectados con un virus que provoca de forma fiable eritroleucemia, el tratamiento con FKL-137 mejoró los niveles de glóbulos rojos, redujo el tamaño del bazo, disminuyó la invasión de células cancerosas en órganos y corrigió el metabolismo anómalo de la glucosa en tejido esplénico —todo ello sin daño evidente en corazón, hígado, pulmones o riñones.
Promesa, límites y siguientes pasos
En conjunto, el trabajo presenta a FKL-137 como un candidato farmacológico de doble acción que bloquea la principal puerta de entrada de glucosa en las células de eritroleucemia y atenúa una potente vía de crecimiento que depende de ese combustible. Al privar primero a las células cancerosas de nutrientes y luego empujarlas hacia la muerte, el compuesto ofrece una forma conceptualmente elegante de explotar una vulnerabilidad que las células normales no comparten en la misma medida. Los autores advierten, sin embargo, que FKL-137 aún requiere refinamiento: tiene una ventana terapéutica relativamente estrecha, las células cancerosas pueden encontrar formas de compensar redirigiendo su metabolismo, y los hallazgos en líneas celulares y modelos murinos deben confirmarse en tejidos humanos. Aun así, el estudio refuerza la idea de que apuntar con precisión a cómo las células cancerosas se nutren y crecen podría abrir un nuevo frente en el tratamiento de este cáncer sanguíneo, por lo demás difícil de controlar.
Cita: Cheng, S., Zhao, W., Yu, J. et al. The fluoroquinoline compound exerts anti-erythroleukemic effects by dual-targeting GLUT1 and the PI3K/AKT signaling pathway. Sci Rep 16, 10916 (2026). https://doi.org/10.1038/s41598-026-45597-9
Palabras clave: eritroleucemia, metabolismo del cáncer, inhibidor de GLUT1, vía PI3K AKT, terapia dirigida