Clear Sky Science · es
Prueba de concepto de extracción de ADN libre de células de plasma basada en un sistema acuoso de dos fases para aplicaciones de biopsia líquida
Por qué importa una prueba de sangre para el cáncer y otras enfermedades
Muchas pruebas médicas modernas buscan pequeños fragmentos de ADN que flotan libremente en nuestra sangre. Estos fragmentos, conocidos como ADN libre de células, pueden revelar si un tumor está liberando material genético, si un órgano trasplantado está siendo rechazado o cómo progresa un embarazo. Pero, dado que estos fragmentos son escasos, cortos y están mezclados con una sopa de proteínas y otras moléculas, extraerlos de forma limpia y rápida resulta sorprendentemente difícil. Este estudio presenta una forma nueva y más sencilla de extraer esos fragmentos del plasma sanguíneo usando un método de separación acuoso y suave, lo que podría hacer que las pruebas avanzadas de “biopsia líquida” sean más accesibles y asequibles.
El desafío de pescar piezas diminutas de ADN
Los médicos e investigadores usan biopsias líquidas para leer pistas genéticas mediante una simple extracción de sangre en lugar de extirpar tejido. El problema es que el ADN libre de células en el plasma suele existir solo en unas pocas decenas de nanogramos por mililitro y está fragmentado en piezas cortas. Una pequeña fracción de este material puede provenir de un tumor o de un órgano trasplantado, por lo que cada fragmento cuenta. Los kits de extracción estándar capturan ADN haciendo que se adhiera a superficies de sílice en presencia de sales fuertes, seguidos de varios lavados y centrifugados. Estos kits funcionan bien, pero requieren tiempo, equipo especial y pueden ser costosos. Además, pueden tener dificultades para recuperar los fragmentos más cortos y pueden arrastrar largas cadenas de ADN genómico normal, que enmascaran señales raras relacionadas con enfermedades.
Un truco de dos capas de agua para atrapar ADN
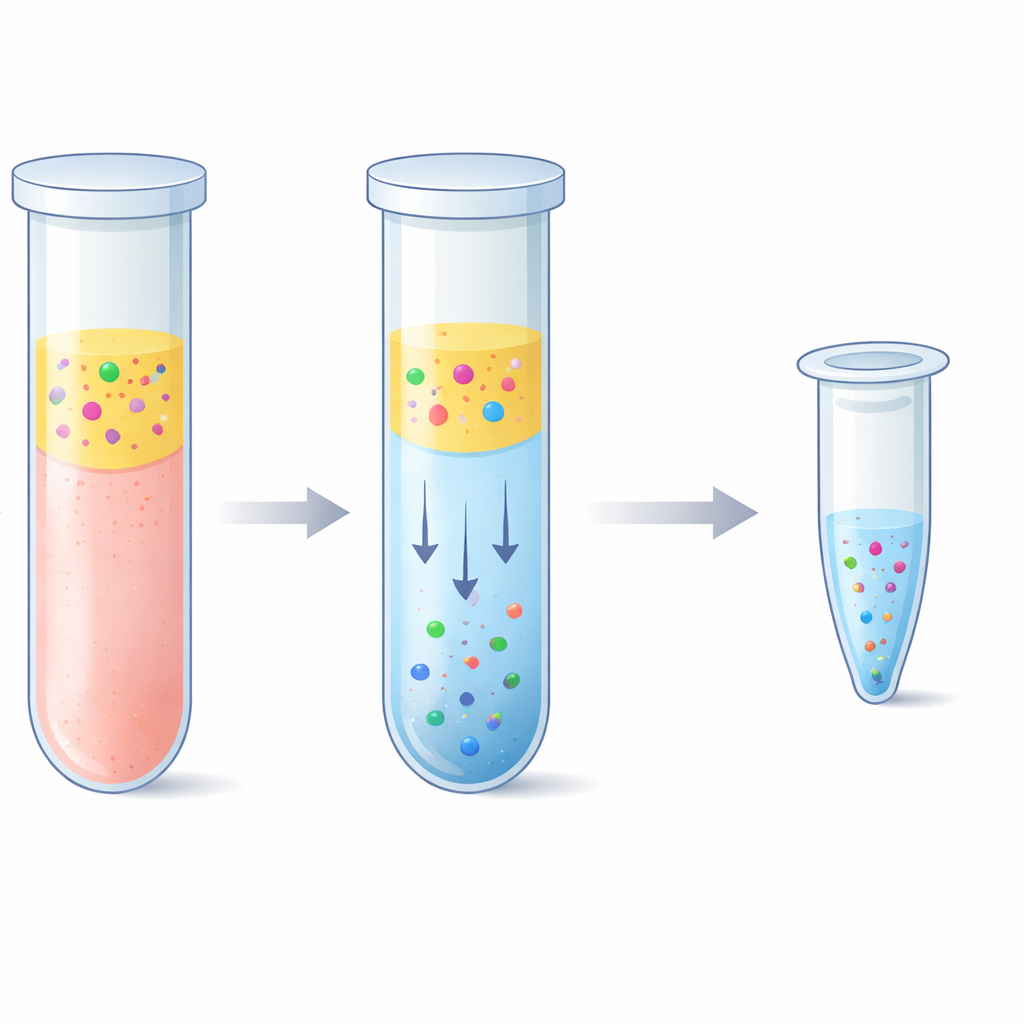
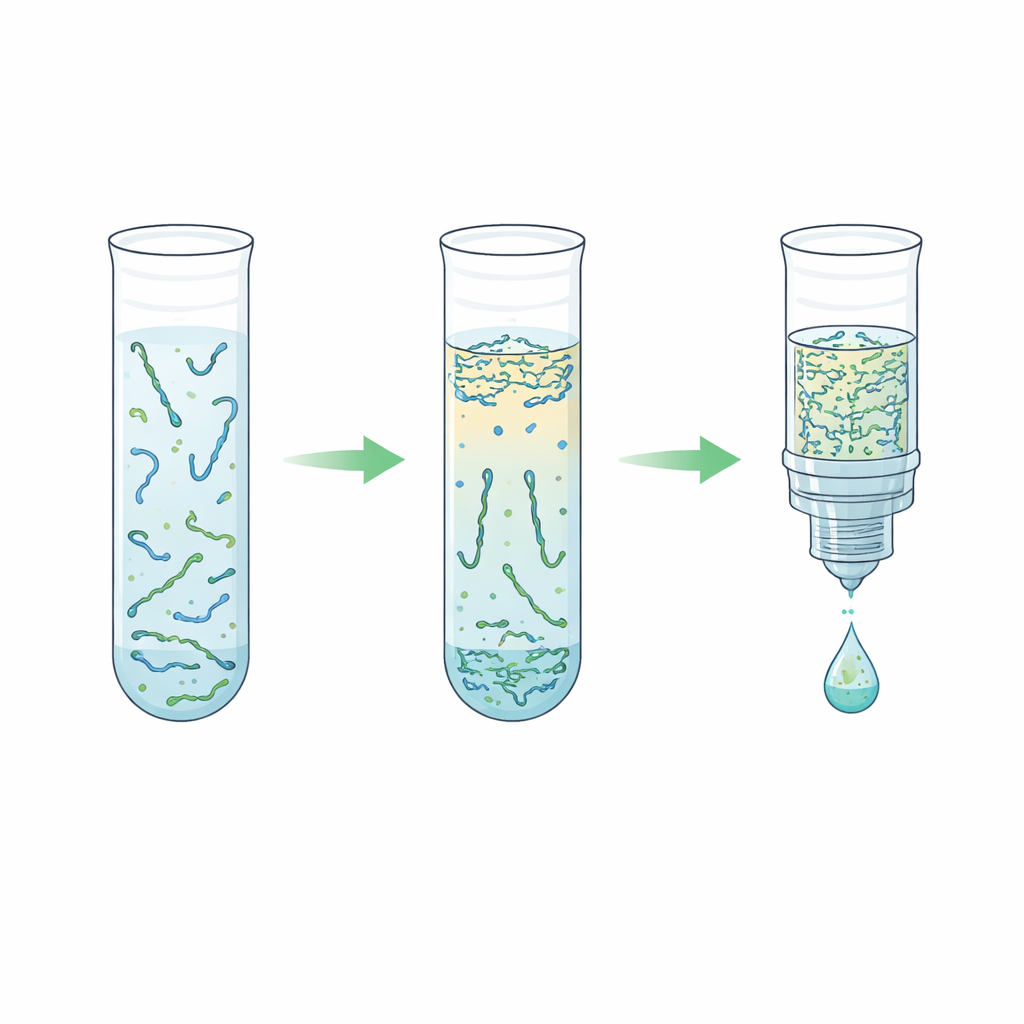
El equipo exploró una alternativa basada en un “sistema acuoso de dos fases”: en términos sencillos, dos líquidos ricos en agua que no se mezclan por completo, como aceite y vinagre, pero ambos compuestos mayormente por agua. Al combinar plasma con un polímero llamado polietilenglicol y sales fosfato simples, la mezcla se separó naturalmente en una capa superior y otra inferior. De manera notable, los fragmentos cortos de ADN prefirieron fuertemente la capa inferior rica en sal, mientras que la mayor parte de las proteínas sanguíneas y las cadenas largas de ADN permanecieron en la capa superior o en la interfaz. Los investigadores ajustaron cuidadosamente la receta para que la capa inferior permaneciera lo bastante pequeña como para concentrar el ADN pero lo bastante suave como para no dañarlo. Luego emparejaron este paso con una purificación por “elución inversa”, que empuja la capa inferior salina a través de una matriz porosa para eliminar la sal y reducir el volumen final, obteniendo al final una solución de ADN más limpia y concentrada.
Refinar el proceso para uso en el mundo real
A través de numerosas rondas de ensayo, los autores ajustaron el equilibrio de polímero y sal, las velocidades de centrifugado, los volúmenes y los pasos opcionales de lisis que rompen los complejos proteína–ADN. Encontraron que aumentar el contenido de polímero a lo largo de ciertas líneas de composición duplicaba la concentración de ADN sin perjudicar la recuperación, y que un condicionamiento más fuerte en el paso de elución inversa aproximadamente cuadruplicaba la concentración en comparación con su trabajo anterior. Sorprendentemente, descubrieron que omitir la lisis agresiva antes de la separación en dos capas a menudo funcionaba mejor; la lisis tendía a perturbar las fases y reducir el rendimiento. Un flujo de trabajo simplificado, en gran parte sin lisis, eliminó alrededor del 99,7 % de las proteínas plasmáticas mientras recuperaba hasta aproximadamente dos tercios del ADN corto de entrada en un volumen cuatro veces menor, todo en cerca de diez minutos de procesamiento total y sólo un par de minutos de trabajo manual.
Cómo se compara el nuevo método
Los investigadores compararon su enfoque con un kit comercial de sílice ampliamente usado. El kit estándar produjo rendimientos totales de ADN algo mayores y una mayor concentración porque eluye en volúmenes muy pequeños. Sin embargo, el método de dos fases mostró recuperaciones consistentes por encima del 60 % en un rango de entradas de ADN, incluso al empezar con cantidades muy pequeñas, y requirió muchos menos pasos manuales y menos equipo. Es importante que el nuevo proceso actuara como un filtro integrado por longitud de fragmento: enriqueció ADN corto, similar al ADN libre de células, mientras excluía en gran medida las cadenas largas que pueden proceder de células sanguíneas rotas. Las pruebas usando PCR cuantitativa mostraron que los extractos limpiados no inhibían la amplificación posterior. Cuando el equipo usó una muestra de referencia comercial que contenía mutaciones relacionadas con el cáncer conocidas, el ADN recuperado con su método pudo convertirse en bibliotecas de secuenciación, correrse en un secuenciador de alto rendimiento y usarse para detectar todas las variantes esperadas en las frecuencias correctas.
Qué podría significar esto para futuras pruebas de sangre
En términos sencillos, este trabajo demuestra que una separación relativamente simple y basada en agua puede reemplazar la química más compleja de superficies sólidas para preparar ADN libre de células a partir de plasma. Aunque el nuevo método actualmente rinde ligeramente menos ADN que los kits comerciales de primer nivel, ofrece un procesamiento rápido, una fuerte eliminación de proteínas no deseadas y de ADN largo, y compatibilidad lista para PCR y secuenciación de próxima generación. Si se valida más ampliamente en muestras de pacientes y se optimiza para automatización, este enfoque podría reducir costes y simplificar los flujos de trabajo de laboratorio, ayudando a que las pruebas de sangre basadas en genética para cáncer, trasplantes y otras condiciones lleguen a un uso más generalizado en la práctica cotidiana.
Cita: Meutelet, R., Buerfent, B.C., Hess, T. et al. Proof of concept for aqueous two-phase system-based extraction of cell-free DNA from plasma for liquid biopsy applications. Sci Rep 16, 11232 (2026). https://doi.org/10.1038/s41598-026-45585-z
Palabras clave: biopsia líquida, ADN libre de células, prueba de sangre para cáncer, extracción de ADN, secuenciación de próxima generación