Clear Sky Science · es
Interferón-β y FTY720 amelioran la inflamación progresiva del SNC mediante la señalización astrocitaria asociada a SOCS1
Por qué esta investigación importa a las personas con esclerosis múltiple
Para muchas personas con esclerosis múltiple (EM), el mayor temor no son las primeras recaídas, sino la pérdida lenta y sostenida de funciones que puede seguirlas. En esta fase tardía y progresiva, el daño dentro del cerebro y la médula espinal continúa incluso cuando los fármacos habituales que actúan sobre el sistema inmunitario en la sangre cumplen su función. Este estudio explora una forma de alcanzar esa inflamación «oculta» combinando una pastilla de EM ya existente con una forma de un fármaco de uso prolongado administrada directamente hacia el cerebro.
Una enfermedad cerebral a largo plazo con pocas opciones
La EM es una enfermedad autoinmune en la que las propias células inmunitarias del cuerpo atacan el aislamiento de las fibras nerviosas, causando problemas visuales, debilidad y otros síntomas neurológicos. En las primeras etapas, los síntomas tienden a aparecer y desaparecer. Con el tiempo, muchos pacientes pasan a una fase progresiva caracterizada por una discapacidad gradual y a menudo irreversible. Durante esta etapa, la barrera hematoencefálica se vuelve más difícil de atravesar para los fármacos, y la actividad nociva de las células residentes del cerebro llamadas glía—especialmente astrocitos y microglía—toma un papel creciente. Los tratamientos actuales, que en su mayoría actúan bloqueando células inmunitarias en la sangre, ofrecen solo una ayuda limitada una vez establecida esta fase.
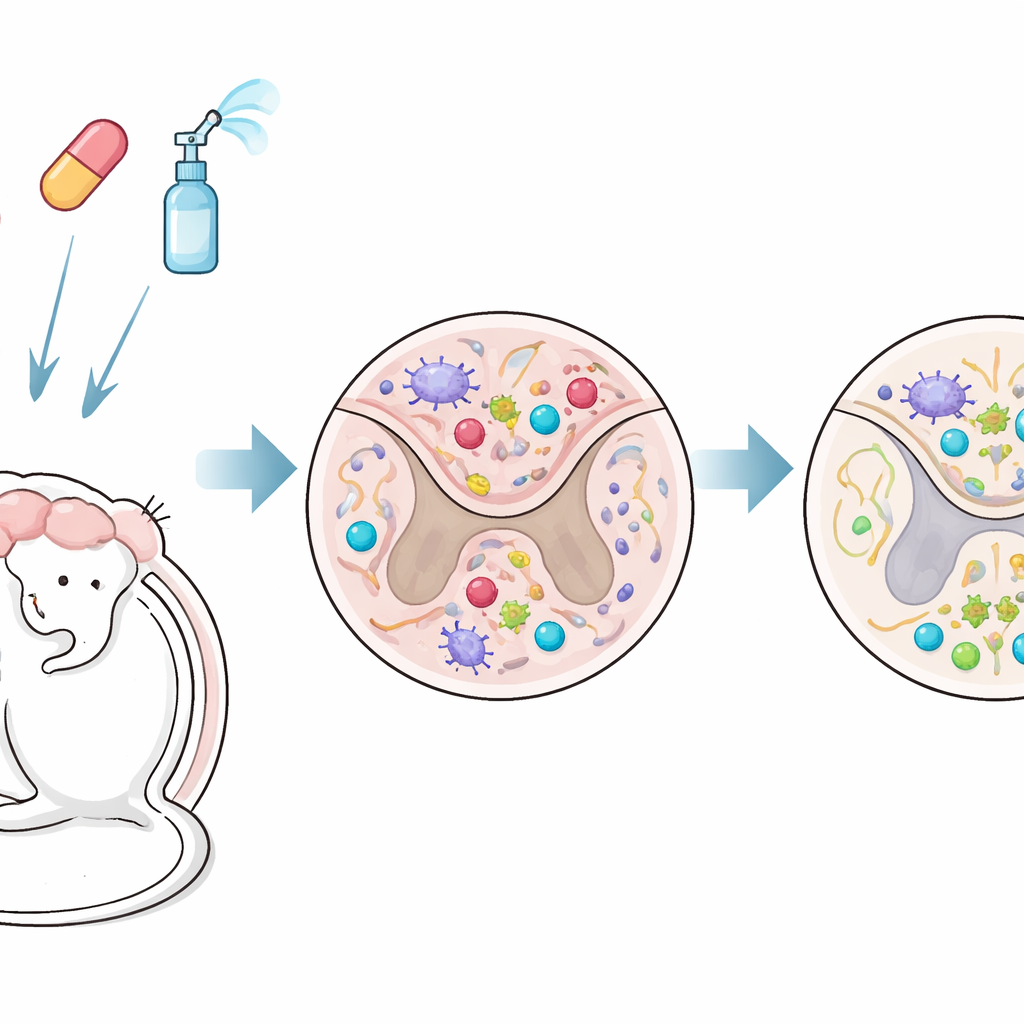
Combinar dos fármacos para alcanzar sangre y cerebro
Los investigadores probaron un tratamiento combinado en un modelo murino que reproduce de forma cercana la EM progresiva. Un fármaco, fingolimod (FTY720), es una pastilla que atrapa células inmunitarias en los ganglios linfáticos y que también puede entrar al cerebro. El otro, interferón‑beta, es una terapia clásica para la EM que normalmente actúa fuera del cerebro porque no atraviesa con facilidad la barrera hematoencefálica. En este estudio, el interferón‑beta se administró por vía intranasal—a través de la nariz—para eludir esa barrera y alcanzar el sistema nervioso central de forma más directa. El tratamiento comenzó después de que los ratones ya hubieran desarrollado problemas neurológicos crónicos, reflejando una etapa en la que el daño suele ser más difícil de revertir.
Menos daño y actividad inmune más contenida
Los ratones que recibieron el tratamiento combinado de fingolimod más interferón‑beta intranasal evolucionaron mejor que los que recibieron solo fingolimod. Sus puntuaciones de enfermedad mejoraron más y algunos déficits neurológicos existentes se redujeron. Al examinar las médulas espinales, los científicos hallaron más mielina preservada, menos signos de lesión axonal y menos células inmunitarias infiltradas. Se redujeron las células T y los monocitos proinflamatorios, y las T restantes produjeron menos de las moléculas mensajeras dañinas interferón‑gamma e IL‑17. Es importante que la terapia combinada también atenuó las señales perjudiciales procedentes de astrocitos y microglía, las células gliales que ayudan a modelar el entorno local dentro del cerebro y la médula espinal.
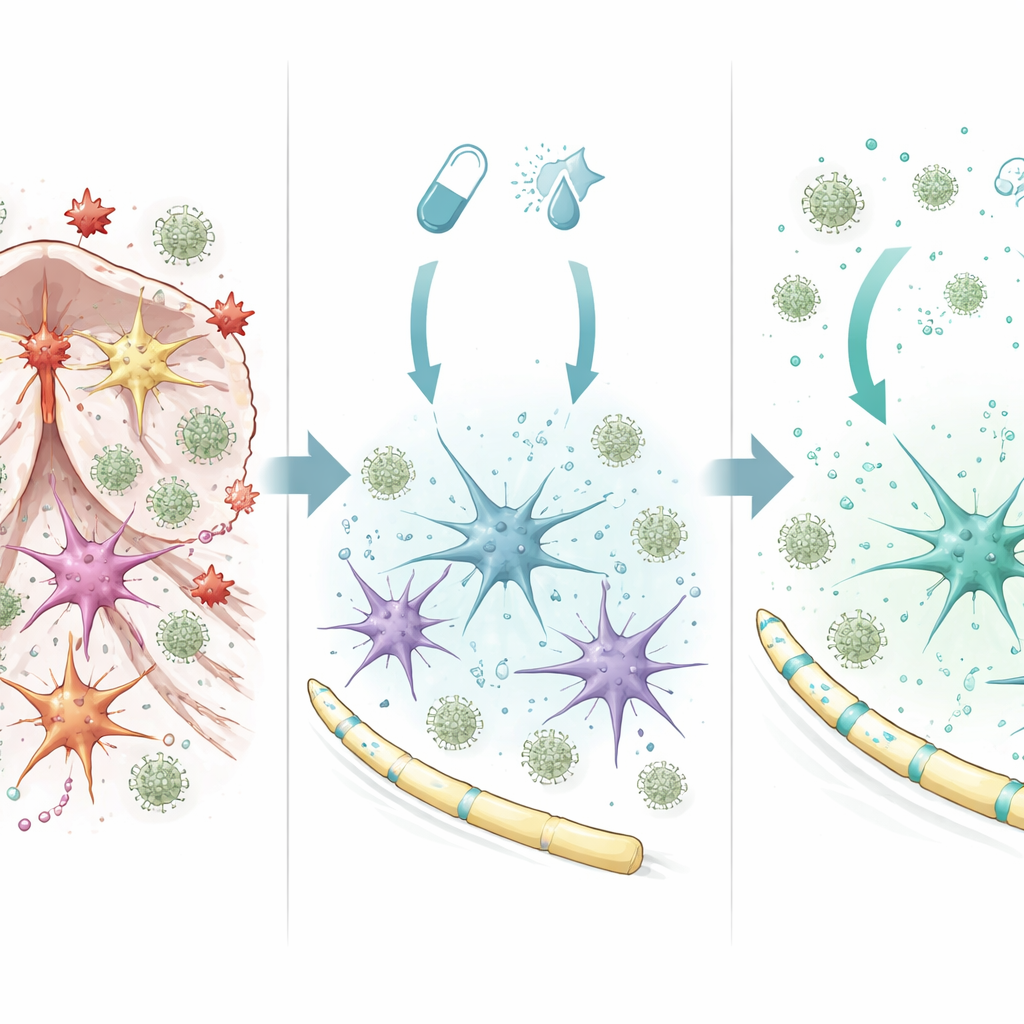
Los astrocitos pasan de comportarse de forma nociva a protectora
Para entender cómo actúa el tratamiento combinado dentro del cerebro, el equipo estudió astrocitos purificados en cultivo. Cuando se expusieron a fingolimod más interferón‑beta, los astrocitos activaron un amplio conjunto de genes vinculados a la supervivencia celular, la reducción de la inflamación y un aislamiento nervioso más saludable. Un actor clave fue un regulador llamado SOCS1, que actúa como freno sobre la señalización inflamatoria. Bloquear SOCS1 en astrocitos borró gran parte del patrón génico protector y provocó que estas células liberaran más factores inflamatorios que atraían a células inmunitarias. En contraste, cuando SOCS1 estaba activo, los astrocitos producían más señales de crecimiento y reparación y liberaban una mezcla de moléculas que reducían la migración de monocitos inflamatorios. Cambios protectores similares se observaron en líneas celulares humanas de astrocitos y microglía tratadas con la combinación de fármacos, lo que sugiere que el mecanismo es relevante más allá de los ratones.
Qué podría significar esto para futuras terapias de la EM
Este estudio muestra que combinar fingolimod con interferón‑beta administrado por la nariz puede hacer más que bloquear células inmunitarias en la sangre. También puede reprogramar astrocitos dentro del sistema nervioso central hacia un estado más calmado y protector, con SOCS1 actuando como un nodo central de control. Si bien el trabajo se realizó en ratones y en cultivos celulares, y el interferón‑beta por sí solo no se probó en paralelo en todos los experimentos, los resultados apuntan a una estrategia prometedora: dirigirse tanto al sistema inmunitario periférico como a las propias células de soporte del cerebro al mismo tiempo. Si se pueden lograr efectos similares y demostrarse seguros en humanos, enfoques combinados y focalizados en el cerebro podrían ayudar a frenar o revertir en parte el daño silencioso que impulsa la EM progresiva.
Cita: Tsaktanis, T., Beyer, T., Nirschl, L. et al. Interferon-β and FTY720 ameliorate progressive CNS inflammation via SOCS1-associated astrocyte signaling. Sci Rep 16, 9851 (2026). https://doi.org/10.1038/s41598-026-45303-9
Palabras clave: esclerosis múltiple progresiva, fingolimod, interferón beta, astrocitos, neuroinflamación