Clear Sky Science · es
Datos cristalográficos de la dolifosfato manosa sintetasa de Pyrococcus furiosus sugieren que la enzima podría voltear su producto glicolipídico
Cómo los microbios termófilos mantienen en forma su capa celular
Muchos microbios que prosperan en ambientes hirvientes sobreviven gracias a una capa protectora de azúcares en su superficie celular. Construir esta capa requiere moléculas especiales grasa–azúcar que deben sintetizarse en un lado de la membrana celular y luego desplazarse al otro. Este estudio analiza una enzima que fabrica una de esas moléculas en un microbio termófilo y sugiere que, de manera notable, la misma proteína podría también ayudar a voltear su producto a través de la membrana, cumpliendo dos funciones a la vez.
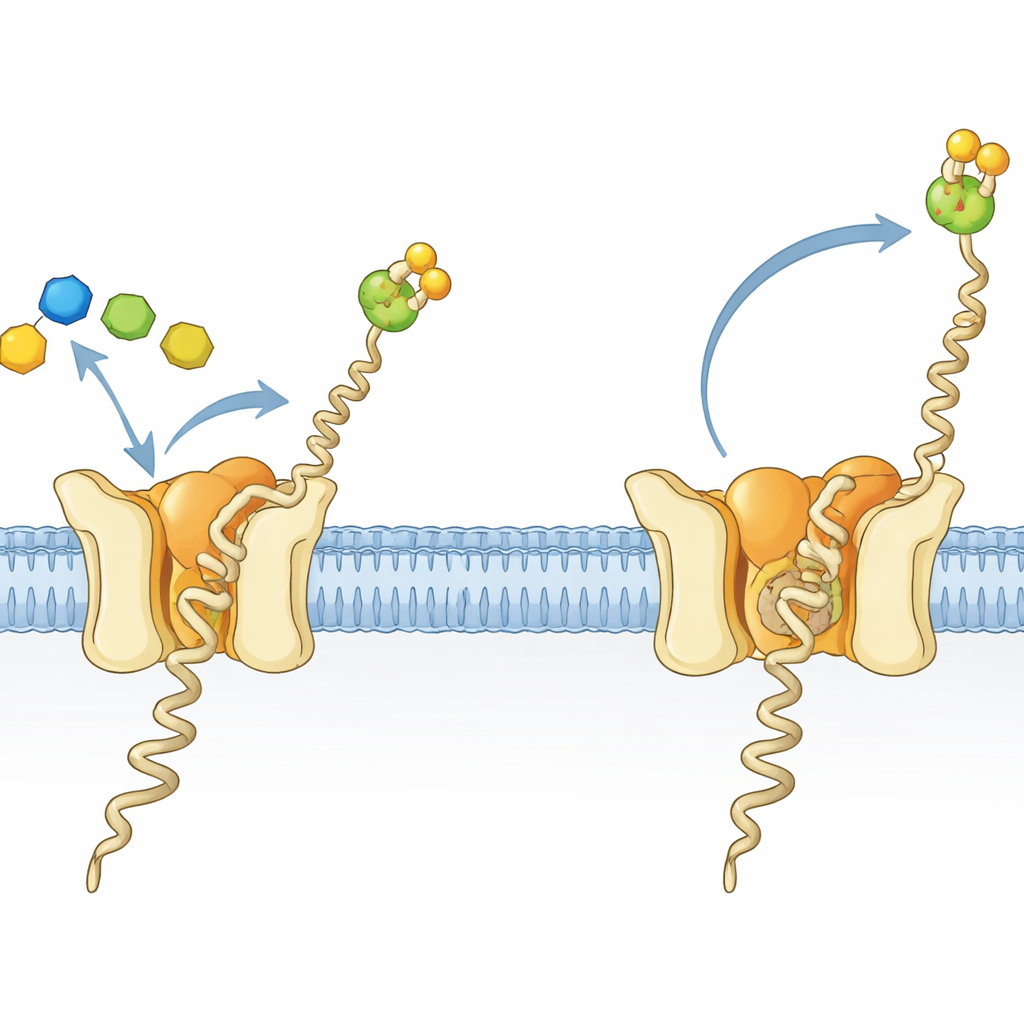
Una minúscula fábrica para una molécula grasa–azúcar crucial
Las células de todos los dominios de la vida decoran muchas proteínas con cadenas de azúcares, un proceso esencial para el plegamiento correcto, la estabilidad y la comunicación entre células. En arqueas y eucariotas, un bloque constructor clave para estas decoraciones es una molécula grasa–azúcar llamada dolifosfato manosa (Dol-P-Man). Consiste en una larga cola grasienta anclada en la membrana y una cabeza de azúcar–fosfato que sobresale hacia el entorno acuoso. Dol-P-Man lo sintetiza la enzima dolifosfato manosa sintetasa (DPMS), que transfiere una manosa desde un donante soluble hacia un lípido unido a la membrana. En la arquea hipertermófila Pyrococcus furiosus, la DPMS es una proteína de cadena simple, denominada DPMS tipo III, con una región catalítica soluble unida a una sección transmembrana formada por cuatro hélices cuya función no había quedado clara.
Cazando a la enzima en pleno acto
Los investigadores cristalizaron la DPMS de P. furiosus junto con sus sustratos y siguieron la reacción mediante cristalografía de rayos X. Su nueva estructura, combinada con tres previas, captura una serie de instantáneas alrededor del momento en que se transfiere el azúcar. En un estado, la molécula donante (GDP-manosa) y un aceptor similar a Dol-P están unidos en una geometría precisa que coloca el carbono reactivo de la manosa directamente frente al grupo fosfato del Dol-P, una disposición “pre-transferencia” ideal. Bucles en la enzima actúan como puertas frontal y posterior: se cierran para sujetar al donante y al ion metálico, y luego se reordenan para abrir un camino que permita la entrada del Dol-P y la salida del GDP gastado una vez que se ha transferido el azúcar. Estos detalles aclarar cómo la enzima asegura una transferencia de azúcar eficiente y precisa en la superficie de la membrana.
Un producto invertido escondido en la membrana
Más sorprendente fue un segundo estado distinto observado en los mismos cristales. Aquí, la Dol-P-Man terminada no se encuentra en el sitio activo, sino alojada más profundamente dentro de la porción transmembrana de la proteína, en una orientación “invertida”. Su cabeza de azúcar–fosfato se sitúa en un bolsillo polar entre dos pares de hélices (TMD1 y TMD2), mientras la cola grasienta discurre por una ranura formada por las hélices. Un aminoácido clave, una fenilalanina, parece actuar como una compuerta que puede bloquear u abrir el acceso a este bolsillo. La calidad de la densidad electrónica y el modo en que la proteína empaqueta en el cristal indican que este Dol-P-Man volteado no es un artefacto de contactos cristalográficos, sino un estado genuino y bien poblado que la enzima puede adoptar.
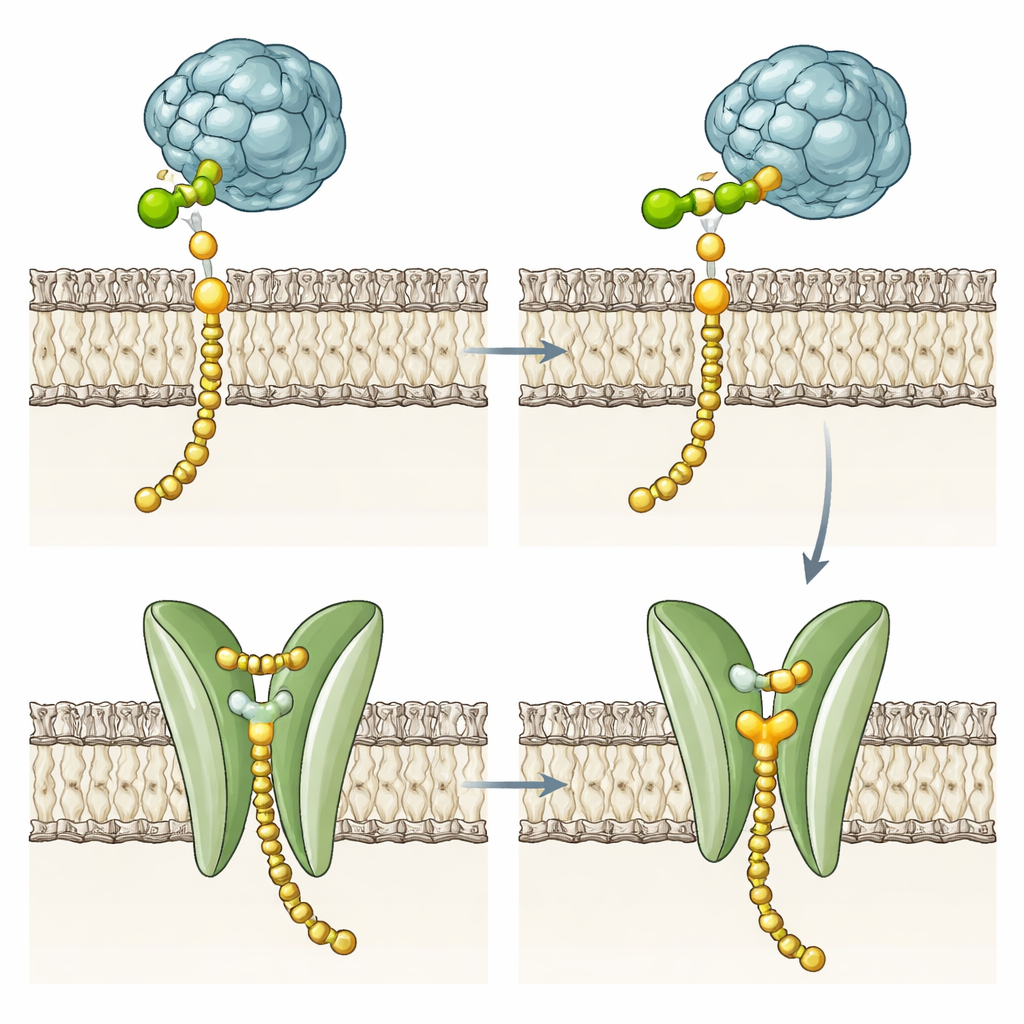
Enzimas mutantes sugieren una segunda función
Para comprobar si el dominio transmembrana es necesario para la química de transferencia de azúcares, el equipo diseñó múltiples variantes. Eliminaron la mayoría o la totalidad de las hélices, las sustituyeron por un segmento de membrana diferente de la DPMS de levadura, o alteraron residuos clave del bolsillo y la compuerta de fenilalanina. Sorprendentemente, estos mutantes aún sintetizaron Dol-P-Man a ritmos similares a los de la enzima intacta, aunque algunos fueron algo menos estables en la membrana. Esto demuestra que la química central reside en la región catalítica soluble y que el haz de cuatro hélices no es necesario para unir la manosa al Dol-P. En cambio, su bolsillo polar conservado, la ranura y el residuo compuerta sugieren un papel especializado en manejar el producto terminado, especialmente en arqueas hipertermófilas cuyas membranas rígidas hacen que el volteo espontáneo de lípidos sea energéticamente costoso.
Por qué importa una enzima con doble propósito
Poniendo juntos la evidencia estructural y mutacional, los autores proponen que la DPMS tipo III es una proteína “multifunción”. Primero sintetiza Dol-P-Man en la cara interna de la membrana plasmática arqueal; luego su dominio transmembrana podría ayudar a voltear la molécula grasa–azúcar para que el grupo cabeza emerja hacia el exterior celular, listo para ser utilizado por otras enzimas que construyen la capa azucarada de la célula. La evolución parece haber favorecido este diseño quimérico principalmente en arqueas extremófilas, donde acercar el sitio de síntesis a una ranura dedicada al volteo podría minimizar pérdidas y daños térmicos. Aunque este trabajo aún no demuestra directamente la actividad de volteo, ofrece un modelo estructural concreto de cómo una enzima puede crear y reposicionar un intermediario lipídico vital a través de una barrera de membrana hostil.
Cita: Gandini, R., Keskitalo, M.M., Reichenbach, T. et al. Crystallographic data for Pyrococcus furiosus dolichylphosphate mannose synthase suggest that the enzyme could flip its glycolipid product. Sci Rep 16, 9076 (2026). https://doi.org/10.1038/s41598-026-44343-5
Palabras clave: dolifosfato manosa, flipasa de lípidos, arqueas, glicosilación de proteínas, enzimas de membrana