Clear Sky Science · es
Modelado de la patogénesis de las toxinas de Clostridioides difficile y la protección por antisueros en una plataforma intestine-on-chip inmunocompetente
Por qué importa este modelo de infección intestinal
Los antibióticos salvan vidas, pero también pueden dejar el intestino vulnerable a infecciones peligrosas. Uno de los peores culpables es Clostridioides difficile, una bacteria que puede causar diarrea grave e inflamación potencialmente mortal del colon, especialmente en pacientes hospitalizados. Este estudio presenta un diminuto «intestino en un chip» que recrea características clave del intestino humano, incluidas las vasos sanguíneos y las células inmunitarias, para observar en tiempo real cómo las toxinas de C. difficile dañan el intestino y cómo los tratamientos con anticuerpos podrían detener ese daño.
Del persistente microbio hospitalario al daño intestinal
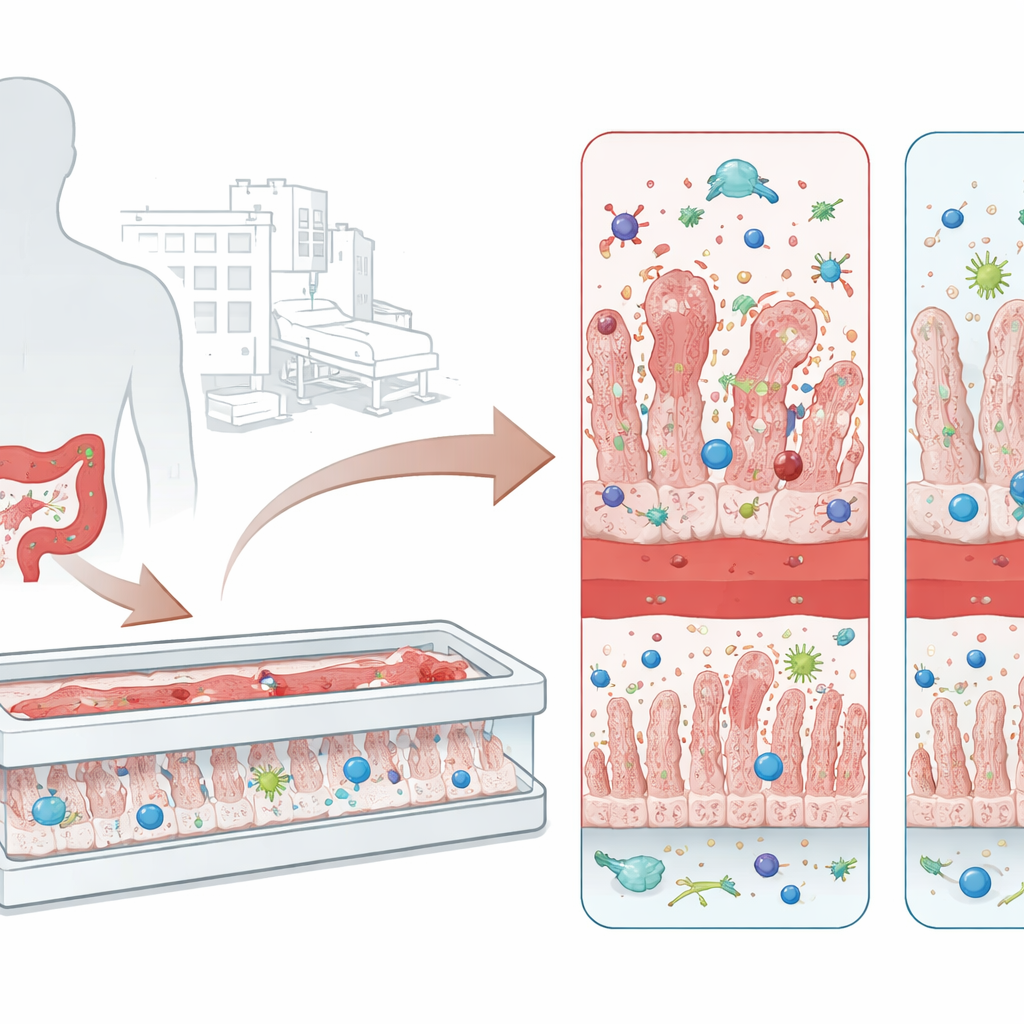
C. difficile prospera en personas cuyo microbioma intestinal normal ha sido alterado, a menudo tras un tratamiento con antibióticos de amplio espectro. El microbio sobrevive en condiciones adversas como resistentes esporas y, una vez establecido en el colon, libera dos toxinas principales conocidas como TcdA y TcdB. Estas toxinas atacan las células intestinales, aflojan las uniones entre ellas y desencadenan oleadas de inflamación. El resultado puede ir desde una diarrea molesta hasta colitis pseudomembranosa, una condición caracterizada por capas de tejido muerto y células inmunitarias que recubren la pared intestinal. Los tratamientos actuales dependen principalmente de más antibióticos y, a veces, de trasplantes de heces, sin embargo muchos pacientes sufren reinfecciones, lo que subraya la necesidad de mejores formas de estudiar la enfermedad y probar terapias que bloqueen las toxinas.
Construyendo un pequeño intestino vivo en un chip
Los modelos tradicionales en el laboratorio cultivan una capa plana de células intestinales en una placa. Aunque útiles, estos cultivos bidimensionales carecen de vasos sanguíneos, células inmunitarias y del suave flujo de fluidos que configuran un intestino real. Los investigadores, en cambio, utilizaron un dispositivo microingenierizado «intestine-on-chip» con dos canales paralelos separados por una membrana porosa. Un lado está revestido de células intestinales que crecen formando crestas en forma de dedos que recuerdan a las vellosidades y forman una barrera estrecha. El lado opuesto contiene células humanas de vasos sanguíneos. En este tejido en miniatura, el equipo añadió macrófagos derivados de monocitos que se asientan en la pared intestinal y neutrófilos circulantes que pueden viajar por el canal vascular e infiltrarse en el tejido, creando un intestino-on-chip inmunocompetente (i‑IoC) que imita más de cerca el intestino vivo.
Observando cómo las toxinas lesionan la barrera
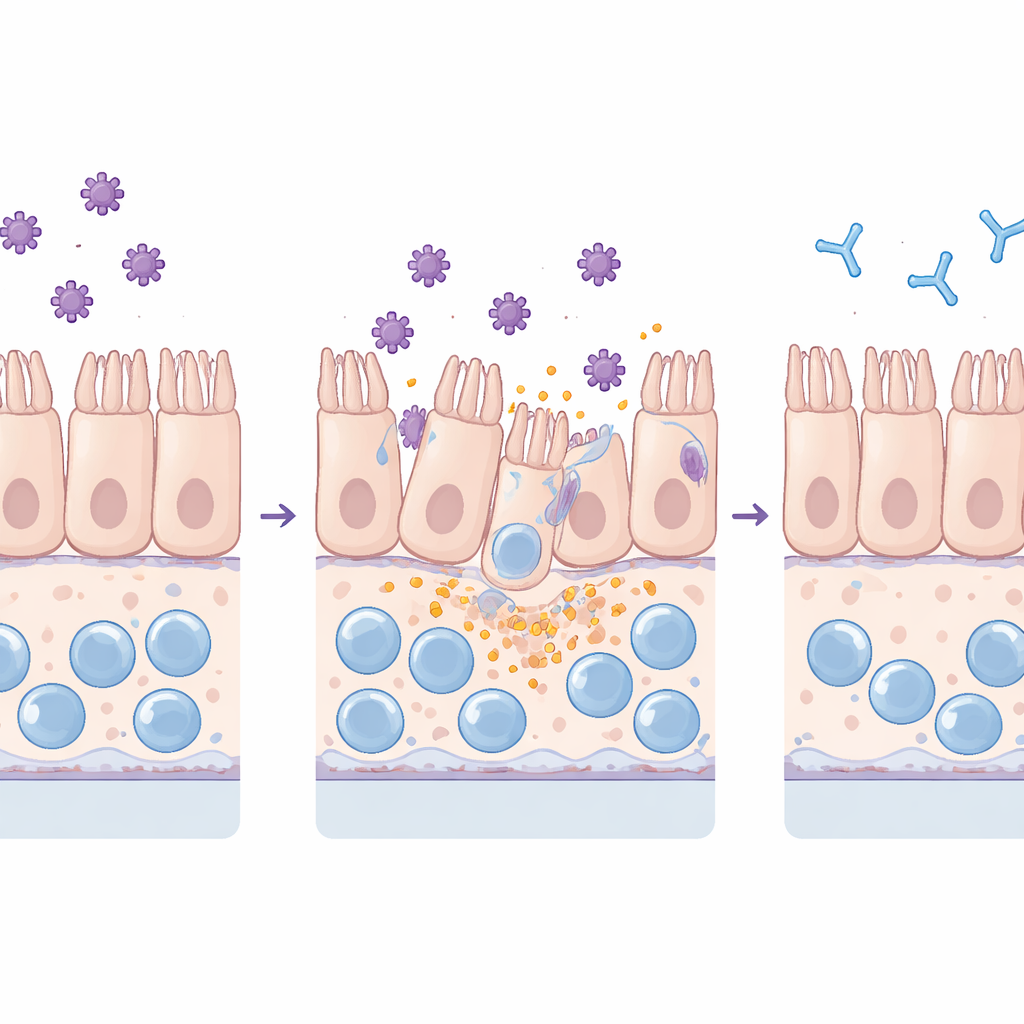
El equipo expuso tanto los cultivos estándar planos como el chip más complejo a TcdA y TcdB purificados. Monitorizaron qué tan bien la barrera intestinal impedía la entrada de un tinte fluorescente, examinaron las proteínas de unión que mantienen unidas a las células vecinas y midieron moléculas inflamatorias y marcadores de lesión celular en el líquido circundante. Ambas toxinas dañaron el tejido, pero de maneras distintas: TcdA desorganizó principalmente las uniones estrechas y provocó que las células adoptaran una forma redondeada, mientras que TcdB condujo a una pérdida generalizada de células de la capa. De forma crucial, el chip detectó estos efectos a niveles de toxina mucho más bajos que los cultivos planos, reflejando su mayor sensibilidad y un comportamiento más semejante al vivo bajo flujo continuo.
Las células inmunitarias avivan la respuesta—y pueden ser protegidas
Agregar macrófagos y neutrófilos al chip amplificó la respuesta a las toxinas. Los macrófagos aumentaron la liberación de mensajeros inflamatorios clave como IL‑6 e IL‑8 pero se vieron ellos mismos reducidos en número, consistente con una forma inflamatoria de muerte celular. Los neutrófilos se adhirieron a la pared vascular y migraron al tejido intestinal, reproduciendo la afluencia de células inmunitarias observada en pacientes. Una exposición prolongada a las toxinas dañó no solo el revestimiento intestinal sino, finalmente, también la capa vascular. Sin embargo, cuando los investigadores premezclaron las toxinas con sueros de anticuerpos neutralizantes, el daño estructural, las fugas de la barrera, las oleadas de citocinas, la pérdida de macrófagos y la infiltración de neutrófilos se redujeron notablemente. En experimentos extendidos, los tejidos lesionados por TcdB pudieron recuperarse parcialmente una vez eliminadas las toxinas, mientras que TcdA dejó un daño más persistente, lo que sugiere diferentes capacidades de reparación tras cada toxina.
Qué significa esto para pacientes y terapias
Para un lector no especializado, el mensaje clave es que este pequeño modelo de intestino vivo puede imitar de forma realista cómo las toxinas de C. difficile lesionan el intestino y activan el sistema inmunitario, a la vez que muestra qué tan bien los anticuerpos antitoxina pueden proteger el tejido. En comparación con capas celulares simples, el intestine-on-chip es más sensible, incluye vasos sanguíneos y células inmunitarias, y puede funcionar durante días para captar tanto el daño temprano como los intentos de recuperación. Eso lo convierte en una plataforma prometedora para probar tratamientos y vacunas de nueva generación que neutralicen toxinas sin alterar más el microbioma intestinal, y potencialmente en una herramienta para personalizar terapias usando células derivadas del propio paciente en el futuro.
Cita: Wegner, V.D., Warschinke, M., Brahim, I.B. et al. Modeling Clostridioides difficile toxin pathogenesis and antiserum protection in an immunocompetent intestine-on-chip platform. Sci Rep 16, 9233 (2026). https://doi.org/10.1038/s41598-026-44170-8
Palabras clave: Clostridioides difficile, intestine-on-chip, infección intestinal, anticuerpos neutralizantes, modelos organ-on-chip