Clear Sky Science · es
Microscopía multifotónica sin marcadores y aprendizaje automático para el reconocimiento del carcinoma hepatocelular
Por qué esto importa a las personas con cáncer de hígado
El cáncer de hígado, en particular el carcinoma hepatocelular, es a la vez frecuente y letal, y la cirugía suele ser la única opción con intención curativa. Durante la intervención, los cirujanos deben extirpar todo el tumor preservando la mayor cantidad posible de tejido hepático sano, un equilibrio difícil cuando el hígado enfermo ya tiene un aspecto anómalo. Este estudio explora una nueva forma de "ver" el cáncer en tiempo real durante la cirugía, sin colorantes ni largos procesos de laboratorio, al combinar microscopía láser avanzada con inteligencia artificial. El objetivo es ayudar a los cirujanos a encontrar el verdadero borde del tumor más rápida y con mayor precisión, lo que podría mejorar los resultados para los pacientes.
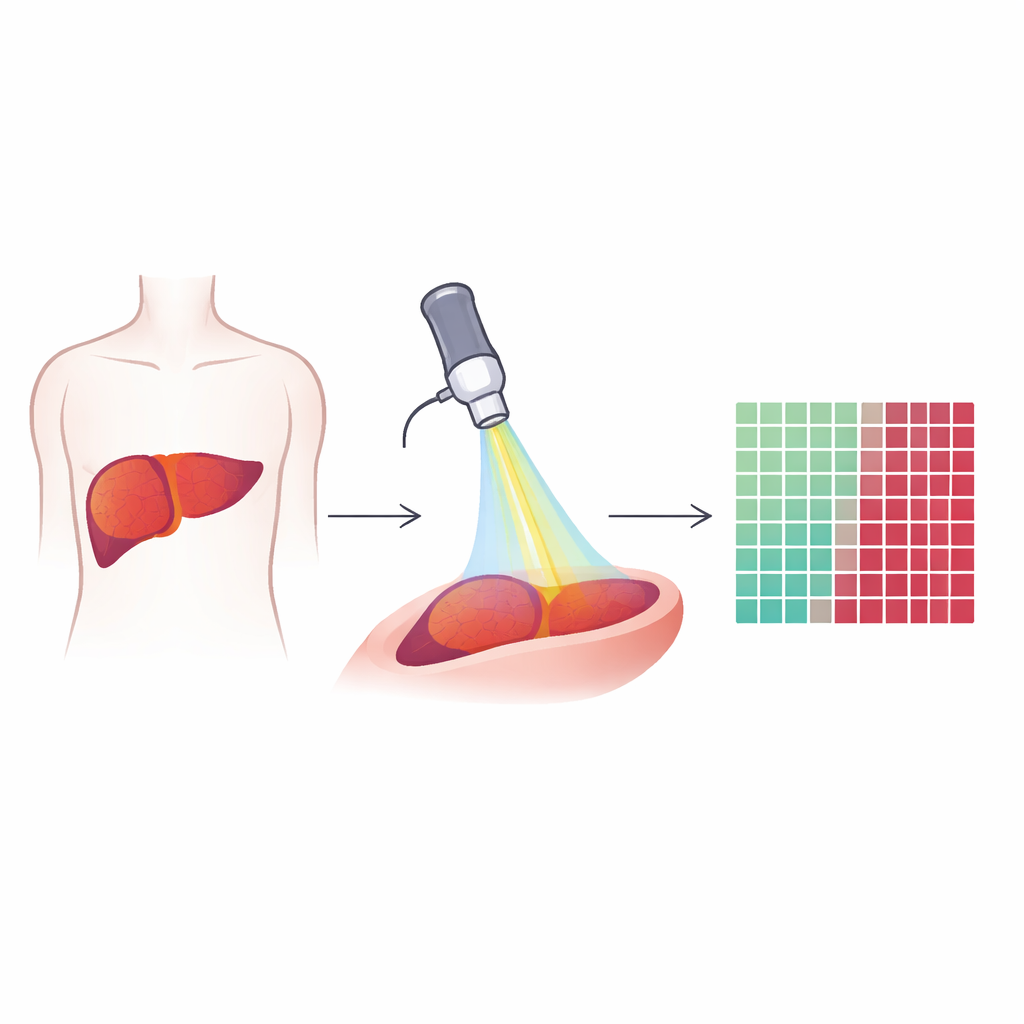
Mirar dentro del tejido con luz especial
Los investigadores emplearon una técnica llamada microscopía multifotónica, que utiliza pulsos láser muy cortos para hacer que moléculas naturales del tejido emitan luz o generen señales. En lugar de añadir colorantes o agentes de contraste, el método lee lo que ya está presente: grasas, fibras de colágeno y sustancias naturalmente fluorescentes dentro de las células. Se registraron tres tipos de señales en cada pequeño campo de visión de las muestras hepáticas: una que resalta los lípidos, otra que muestra la autofluorescencia de moléculas como NADH y la vitamina A, y otra que revela fibras de colágeno rígidas. Juntas, estas señales crean imágenes coloridas y de alta resolución que muestran tanto células individuales como la arquitectura general del tejido hepático y de los tumores.
Capturar las múltiples caras del cáncer de hígado
El equipo examinó tejido de 76 pacientes intervenidos por cáncer de hígado, observando tanto el tumor como el hígado circundante. Demostraron que esta imagen sin marcadores puede representar los patrones clásicos de crecimiento del carcinoma hepatocelular, como placas tumorales finas o gruesas, láminas sólidas y estructuras semejantes a glándulas. También revela cambios en el hígado adyacente, incluidos la acumulación de grasa y la cicatrización, comunes en pacientes con enfermedad hepática crónica. Es importante que estos patrones eran visibles incluso cuando las imágenes se adquirían a resolución relativamente baja, similar a la que podrían proporcionar futuros dispositivos endoscópicos dentro del cuerpo. Esto sugiere que el enfoque podría ser práctico en el quirófano, no solo en el laboratorio.
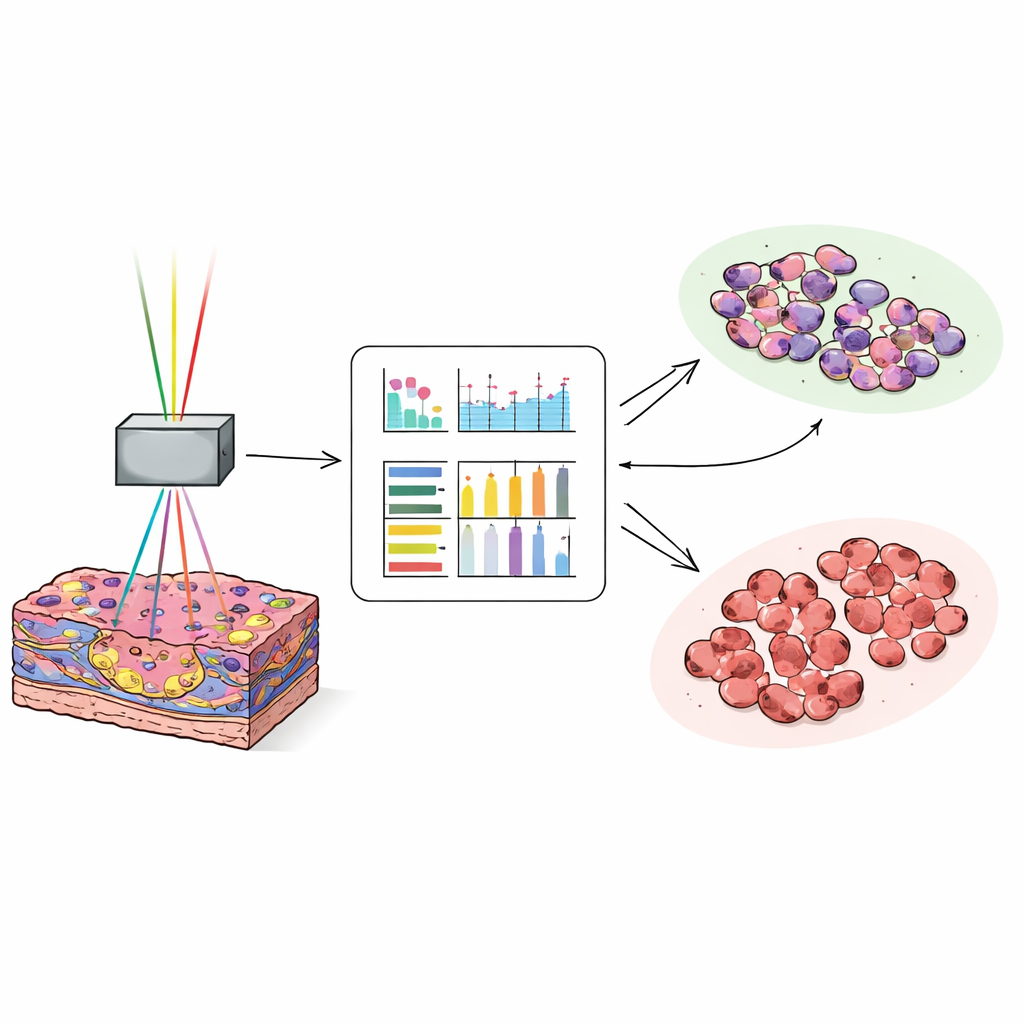
Enseñar a un ordenador a detectar el borde del tumor
Para convertir imágenes ricas pero complejas en decisiones rápidas, los científicos transformaron cada imagen en números que describen la textura, como qué tan suaves, ásperos o variados son los patrones de los píxeles. Para cada canal de imagen calcularon 17 de estas medidas y luego entrenaron una red neuronal con unas 25.000 imágenes de 35 pacientes para distinguir tejido tumoral de hígado no canceroso. A continuación probaron el modelo con aproximadamente 27.000 imágenes nuevas de otros 38 pacientes. Cuando el ordenador utilizó una combinación de las señales de autofluorescencia y las sensibles al colágeno, etiquetó correctamente las imágenes como tumorales o normales en alrededor de 97 de cada 100 casos. Incluso los tumores bien diferenciados y más sutiles, que pueden ser difíciles de reconocer para los patólogos en cortes congelados rápidos, se clasificaron con alta precisión.
Qué revelan los patrones de luz sobre el cáncer
Al comparar diferentes combinaciones de señales, el estudio encontró que la autofluorescencia aportaba la información más útil para diferenciar tejido canceroso de no canceroso. Este resplandor proviene de muchas moléculas naturales dentro de las células y de estructuras como la elastina y el colágeno, de modo que codifica la densidad celular, el tamaño y la forma del núcleo (vistos como áreas más oscuras), las gotas de grasa y la composición del tejido circundante. Añadir la señal específica de colágeno acentuó aún más el contraste entre el tumor y el hígado de fondo, reflejando diferencias conocidas en la disposición de fibras y vasos sanguíneos. Sorprendentemente, la señal centrada en lípidos contribuyó menos a la clasificación automática, un hallazgo práctico porque podría permitir diseños de dispositivos más simples que dependan de un único haz láser en lugar de configuraciones más complejas de dos haces.
Del banco de laboratorio al quirófano
Para imitar el uso quirúrgico real, el equipo también aplicó su mejor modelo a muestras de tejido que incluían el borde real entre tumor y hígado, creando mapas de probabilidad que destacaban dónde terminaba el cáncer y comenzaba el tejido normal. Estos mapas coincidieron en general con la histología convencional, aunque las regiones muy grasas o ricas en colágeno a veces confundieron al clasificador. Los autores señalan obstáculos pendientes antes de que esta tecnología pueda guiar cirugías en vivo, incluyendo la profundidad limitada de la imagen óptica, la necesidad de endoscopios robustos y estériles, el movimiento y la presencia de sangre en el campo quirúrgico, y el reto de validar la inteligencia artificial con conjuntos de datos grandes y del mundo real. Aun así, el trabajo muestra que la imagen multifotónica sin marcadores, combinada con aprendizaje automático, puede funcionar como un microscopio digital rápido que algún día podría ayudar a los cirujanos a resecar con mayor precisión y seguridad, aumentando las probabilidades de extirpar todo el cáncer mientras se preserva la mayor cantidad posible de hígado sano.
Cita: Galli, R., Korn, S., Aust, D. et al. Label-free multiphoton microscopy and machine learning for recognition of hepatocellular carcinoma. Sci Rep 16, 8734 (2026). https://doi.org/10.1038/s41598-026-43831-y
Palabras clave: imagen del cáncer de hígado, microscopía multifotónica, autofluorescencia, márgenes quirúrgicos, aprendizaje automático