Clear Sky Science · es
Elucidando la relación entre afinidad y potencia en el rendimiento de IgE terapéuticas
Volver las inmunoglobulinas de la alergia contra el cáncer
Las personas alérgicas conocen la potencia de los anticuerpos IgE: las moléculas que desencadenan ojos llorosos y estornudos repentinos. Este estudio plantea una pregunta sorprendente: ¿puede esa misma biología tan potente redirigirse para combatir el cáncer y, de ser así, con qué precisión deben ajustarse estos anticuerpos para funcionar mejor? Los investigadores se centraron en carcinomas de mama que expresan la proteína HER2, incluyendo casos en que HER2 está presente a niveles muy bajos y los fármacos actuales a menudo fracasan.
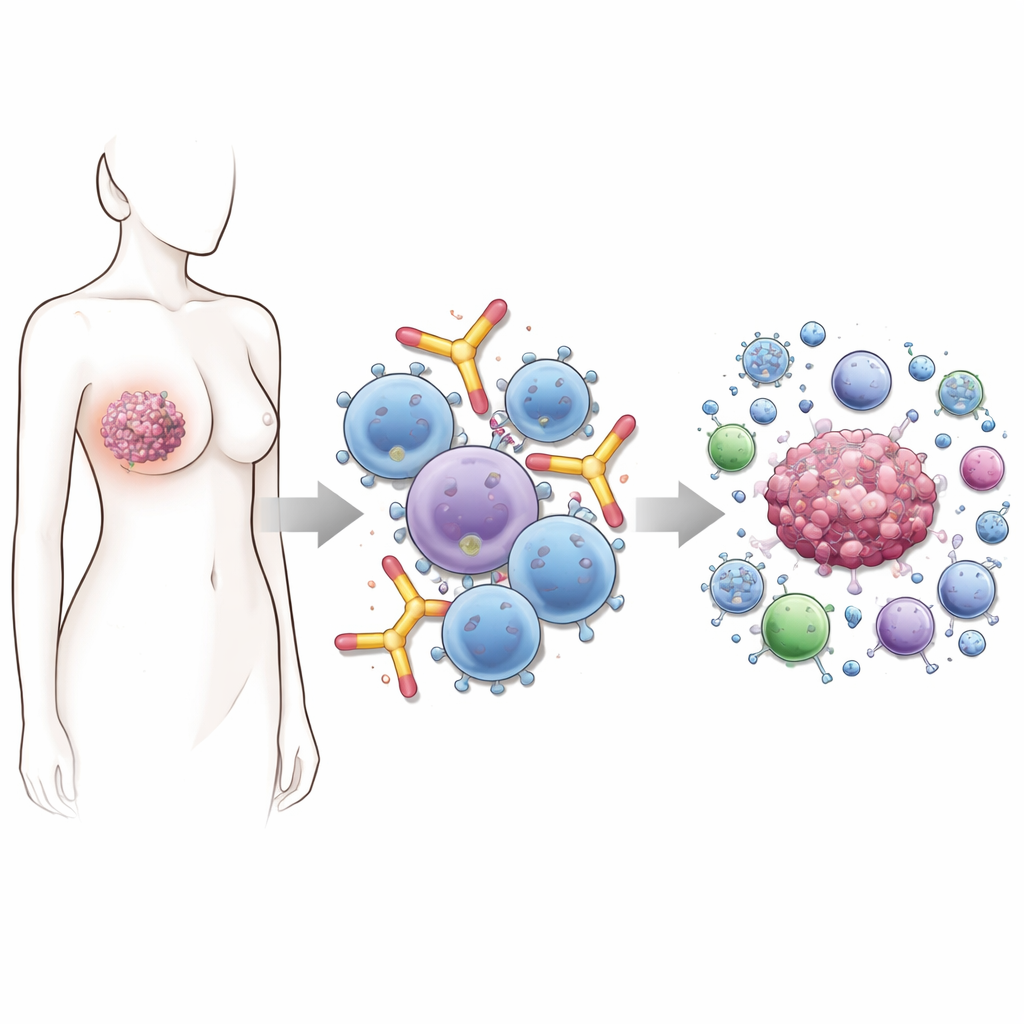
Por qué esta clase de anticuerpo es tan especial
La mayoría de los fármacos con anticuerpos en el mercado pertenecen a la clase IgG. Son los caballos de batalla de la terapia oncológica moderna, pero tienen límites—especialmente cuando los tumores evaden el ataque reduciendo la cantidad de proteína diana en su superficie. Las IgE son distintas. Se unen de forma natural con gran firmeza a células inmunes como mastocitos, basófilos, monocitos y macrófagos, preparándolas para respuestas rápidas. En la alergia, eso significa reacciones explosivas ante polen o alimentos. En el cáncer, la misma configuración podría traducirse en ataques rápidos y focalizados sobre las células tumorales en cuanto la IgE encuentra su objetivo en la superficie tumoral.
Diseñando una IgE más afin a la búsqueda del cáncer
El equipo había creado previamente un anticuerpo IgE, llamado EPS 226, que reconoce HER2 en células de cáncer de mama y puede frenar el crecimiento tumoral en modelos experimentales. En este nuevo trabajo, se propusieron responder a una cuestión sutil pero crucial de diseño: ¿mejorar el agarre del anticuerpo sobre HER2 aumenta realmente su capacidad para movilizar el sistema inmune, o la adhesión natural de “muchas manos” de la IgE (llamada avididad) ya realiza la mayor parte del trabajo? Para explorar esto, emplearon un enfoque de mutagénesis dirigida y selección en bacterias para generar millones de pequeñas variaciones de la región de unión a HER2 y luego seleccionaron 12 nuevas variantes de IgE que se unían a HER2 con mayor fuerza que el anticuerpo original.
Probar la potencia en células y animales
Estos anticuerpos mejorados se sometieron luego a una serie de pruebas en experimentos celulares. Cuando se cargaron en mastocitos y se expusieron a células cancerosas HER2-positivas, la mayoría de las IgE de mayor unión provocaron una desgranulación más potente—una respuesta de activación que libera poderosas sustancias inmunes. Una variante, renombrada EPS 232, destacó por su capacidad de activar células manteniendo al mismo tiempo una unión eficaz a HER2 en células tumorales humanas y de rata. Pruebas adicionales mostraron que EPS 232 mejoró la preparación de las células inmunes para matar el cáncer: aumentó la citotoxicidad por basófilos y promovió una fagocitosis más eficiente de células tumorales HER2-positivas tanto por células inmunes diseñadas como por macrófagos humanos primarios. Curiosamente, aumentar la fuerza de unión ayudó solo hasta cierto punto; variantes con afinidad extremadamente alta no superaron a EPS 232, lo que sugiere que existe un "punto óptimo" en el que el agarre es lo suficientemente fuerte para ser efectivo pero no tan fuerte que dificulte cuántos anticuerpos y células inmunes pueden comprometerse con cada célula tumoral.
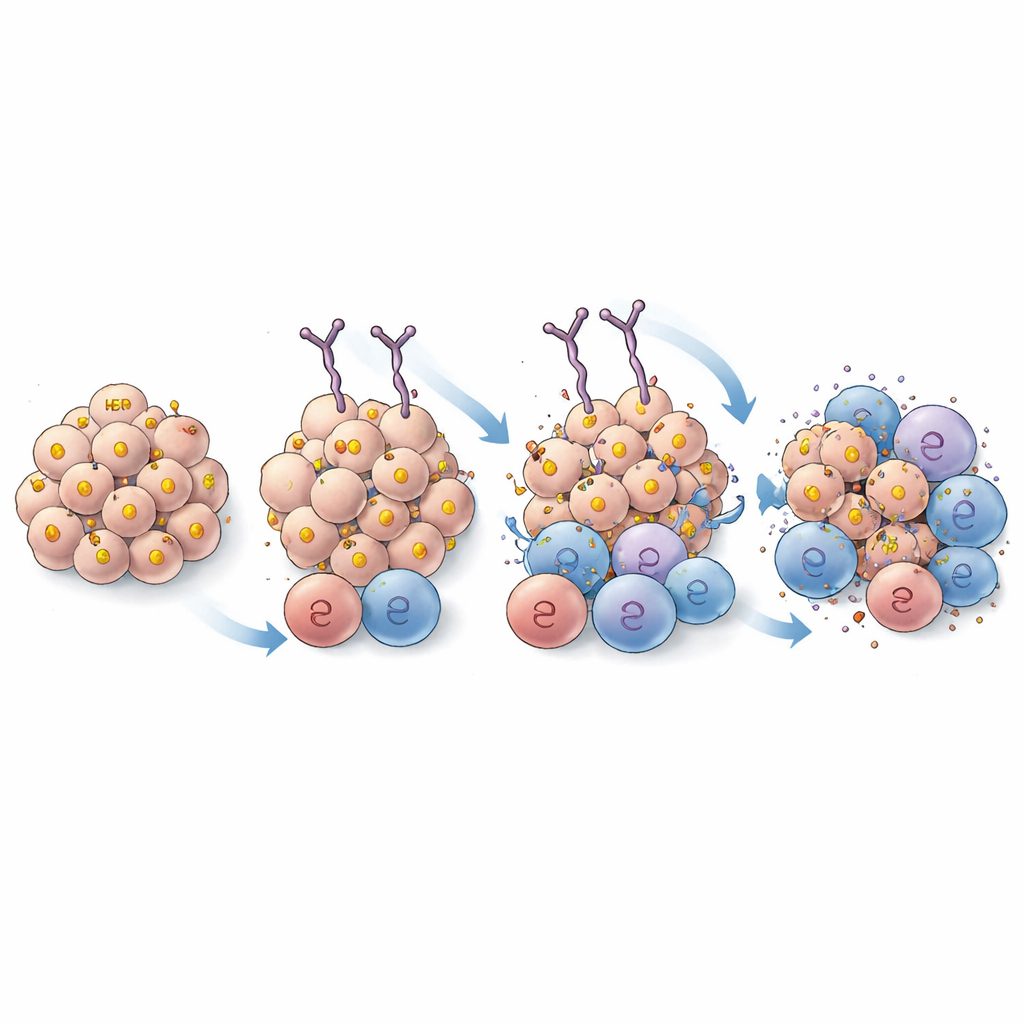
Analizando cómo se une el anticuerpo
Para asegurarse de que las mejoras provenían de una mayor fuerza de unión y no de reconocer un nuevo parche de HER2, los científicos usaron criomicroscopía electrónica de alta resolución para visualizar cómo se sitúan EPS 232 y el EPS 226 original sobre la proteína HER2. Las estructuras mostraron que ambos anticuerpos se acoplan en la misma región de HER2 y emplean puntos de contacto muy similares, con diferencias sutiles que no parecían alterar el sitio de unión global. Esto respalda la idea de que el mejor rendimiento de EPS 232 se debe a una afinidad mejorada y no a un cambio de diana.
Del banco al control tumoral
La prueba definitiva llegó en modelos animales. En ratones portadores de tumores mamarios humanos y provistos de células inmunes humanas, EPS 232 frenó el crecimiento tumoral de forma más eficaz y a dosis más bajas que EPS 226. En ratas con un modelo agresivo de cáncer de mama que expresa niveles ultra-bajos de HER2—similar a algunos cánceres de mama triple negativos—una versión adaptada de EPS 232 para rata no solo ralentizó el crecimiento tumoral más que su predecesor, sino que también prolongó la supervivencia. Los tumores de animales tratados mostraron una mayor infiltración de células T y macrófagos, lo que indica que el anticuerpo mejorado fue más eficaz en remodelar el microambiente tumoral hacia uno más favorable al ataque inmune.
Qué significa esto para futuras terapias contra el cáncer
Para el lector general, el mensaje principal es que afinar cuán firmemente una IgE agarra su diana tumoral puede marcar una diferencia real en su eficacia, aun cuando la IgE ya establece múltiples contactos simultáneos con las células. El estudio identifica a EPS 232 como candidata líder de IgE terapéutica contra cánceres de mama HER2-positivos y HER2-bajos, incluidas formas que actualmente carecen de buenas opciones de tratamiento. En términos más amplios, demuestra que los anticuerpos “al estilo alergia” pueden diseñarse con el equilibrio adecuado de fuerza de unión para convertir un sistema de respuesta rápida que normalmente provoca estornudos en uno que ayuda al sistema inmunitario a localizar y eliminar tumores.
Cita: Marano, F., McKenzie, C., Birtley, J.R. et al. Elucidating the relationship between affinity and potency in the performance of therapeutic IgE. Sci Rep 16, 10555 (2026). https://doi.org/10.1038/s41598-026-43772-6
Palabras clave: IgE terapéutica, cáncer de mama HER2, afinidad de anticuerpos, inmunoterapia del cáncer, cáncer de mama triple negativo