Clear Sky Science · es
La estratificación por dosis de prescripción mejora la predicción de dosis basada en aprendizaje profundo para VMAT en CPNM localmente avanzado
Por qué importan planes de radiación más inteligentes
Cuando los médicos tratan el cáncer de pulmón avanzado con radiación, caminan por una cuerda floja: administrar suficiente energía para controlar el tumor a la vez que protegen órganos sensibles cercanos. Diseñar estos planes es lento, complejo y depende en gran medida de la pericia del planificador. Este estudio explora cómo la inteligencia artificial puede predecir el patrón de radiación en el tórax y, lo que es crucial, demuestra que entrenar a la IA con niveles de dosis agrupados con cuidado mejora la precisión y la utilidad clínica de sus predicciones.
Cómo se trata el cáncer de pulmón con haces focalizados
La mayoría de las personas con cáncer de pulmón no microcítico (CPNM) localmente avanzado no pueden someterse a resección quirúrgica del tumor. En su lugar, a menudo reciben quimioterapia junto con haces de radiación altamente conformados que barren el tórax en arcos, una técnica conocida como VMAT. El objetivo es bañar el tumor con una dosis alta y uniforme mientras se limita la exposición a los pulmones, el corazón, el esófago y la médula espinal. Alcanzar este equilibrio suele requerir múltiples rondas de ajustes por ensayo y error, lo que consume tiempo y puede retrasar decisiones de tratamiento. Si los médicos pudieran estimar rápidamente qué patrón de dosis es realísticamente alcanzable para un paciente concreto, podrían elegir la mejor estrategia terapéutica antes.
Enseñar a un algoritmo a reconocer patrones de dosis
Los investigadores recurrieron al aprendizaje profundo, una forma de IA que aprende patrones directamente a partir de imágenes. Reunieron tomografías computarizadas y planes de tratamiento finalizados de 72 pacientes con cáncer de pulmón tratados con VMAT. Para cada paciente, recalcularon cómo la misma configuración de haces produciría tres dosis totales diferentes: 50, 54 y 60 gray (Gy), las unidades estándar de radiación. Cada caso se convirtió en una rejilla tridimensional que marcaba el tumor, órganos clave y la imagen de TC subyacente. Estos nueve canales de información se introdujeron en una U-Net 3D, un diseño común de red neuronal que puede aprender cómo tiende a distribuirse la dosis por el cuerpo en función de la anatomía.
Por qué importa agrupar por dosis de prescripción
Una cuestión central fue cómo manejar el hecho de que los pacientes reciben distintas dosis totales prescritas. El equipo construyó cuatro modelos de IA idénticos en lo demás. Tres fueron modelos de “prescripción única”, cada uno entrenado solo con planes de un nivel de dosis (50, 54 o 60 Gy). El cuarto modelo mezcló casos de 50 y 60 Gy sin decirle a la red qué prescripción estaba viendo. Al evaluarlos con pacientes nuevos, los modelos específicos por prescripción hicieron un mejor trabajo en reproducir la dosis real en el tumor, manteniendo tanto la cobertura como los puntos calientes próximos a los planes clínicos, normalmente dentro de unos pocos Gy. En contraste, el modelo mixto cometió errores notablemente mayores en las regiones de dosis más alta del tumor y alrededor de la médula espinal, donde la dosis debe mantenerse por debajo de límites de seguridad estrictos.
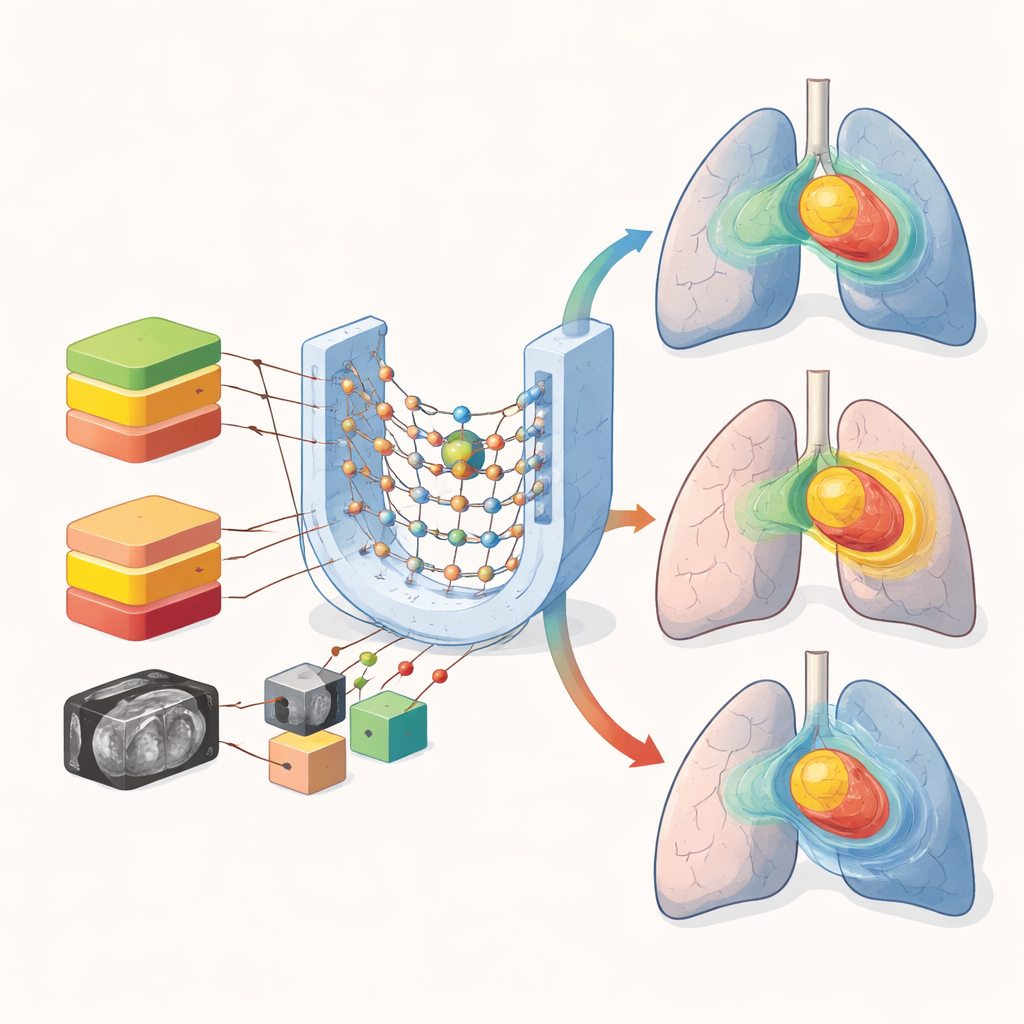
Proteger órganos vitales a la vez que se agiliza la planificación
Curiosamente, para muchos órganos como los pulmones, el corazón y el esófago, los modelos mixto y estratificado mostraron un rendimiento similar. Los errores medios de dosis en estas estructuras más grandes se mantuvieron modestos en todos los enfoques. La principal debilidad de mezclar prescripciones surgió en estructuras pequeñas y sensibles como la médula espinal, donde es esencial una caída de dosis pronunciada. Las comprobaciones visuales de los mapas de dosis predichos mostraron que todos los modelos capturaron la forma general de la región de alta dosis en el tumor, pero mezclar prescripciones condujo a un mayor desenfoque en los gradientes pronunciados y en las zonas de baja dosis de los pulmones. Estas diferencias, aunque sutiles numéricamente, pueden ser importantes cuando los médicos deciden si una prescripción más alta es segura.
Qué significa esto para pacientes y centros clínicos
Para los pacientes, este trabajo no sustituye los cálculos de dosis detallados que ya realizan los sistemas clínicos, pero podría ayudar a garantizar que tiempo y esfuerzo se dediquen a planes que sean realmente factibles y seguros. Al mostrar que agrupar los datos de entrenamiento por dosis de prescripción afina significativamente las predicciones de la IA—especialmente para la cobertura tumoral y la protección de la médula espinal—el estudio destaca una elección de diseño práctica que puede hacer que la asistencia por ordenador sea más fiable. Con más pruebas en grupos de pacientes más grandes y diversos, dichos modelos podrían convertirse en herramientas de uso cotidiano que ofrezcan a los médicos una vista previa rápida, basada en la anatomía, de los probables intercambios de radiación, apoyando una planificación de tratamiento mejor y más consistente.
Cita: Chaipanya, T., Nimjaroen, K., Chamchod, S. et al. Prescription‑dose stratification improves deep learning‑based VMAT dose prediction in locally advanced NSCLC. Sci Rep 16, 8707 (2026). https://doi.org/10.1038/s41598-026-43192-6
Palabras clave: radioterapia del cáncer de pulmón, predicción de dosis por aprendizaje profundo, planificación VMAT, optimización de planes de tratamiento, órganos en riesgo