Clear Sky Science · es
Diseño dirigido por datos de bloqueadores LNA para la eliminación eficiente de contaminantes en bibliotecas de Ribo-Seq
Por qué importa limpiar los datos de secuenciación
La biología moderna a menudo se basa en leer millones de pequeños fragmentos de ARN para comprender cómo las células fabrican proteínas. Pero estas mediciones potentes, en especial un método llamado ribosome profiling (Ribo‑Seq), pueden estar llenas de piezas de ARN irrelevantes que desperdician capacidad de secuenciación y dinero. Este estudio describe una forma simple y dirigida por datos de diseñar "bloqueadores" moleculares especializados que eliminan selectivamente esos fragmentos no deseados, casi duplicando la información útil que los investigadores obtienen del mismo experimento.
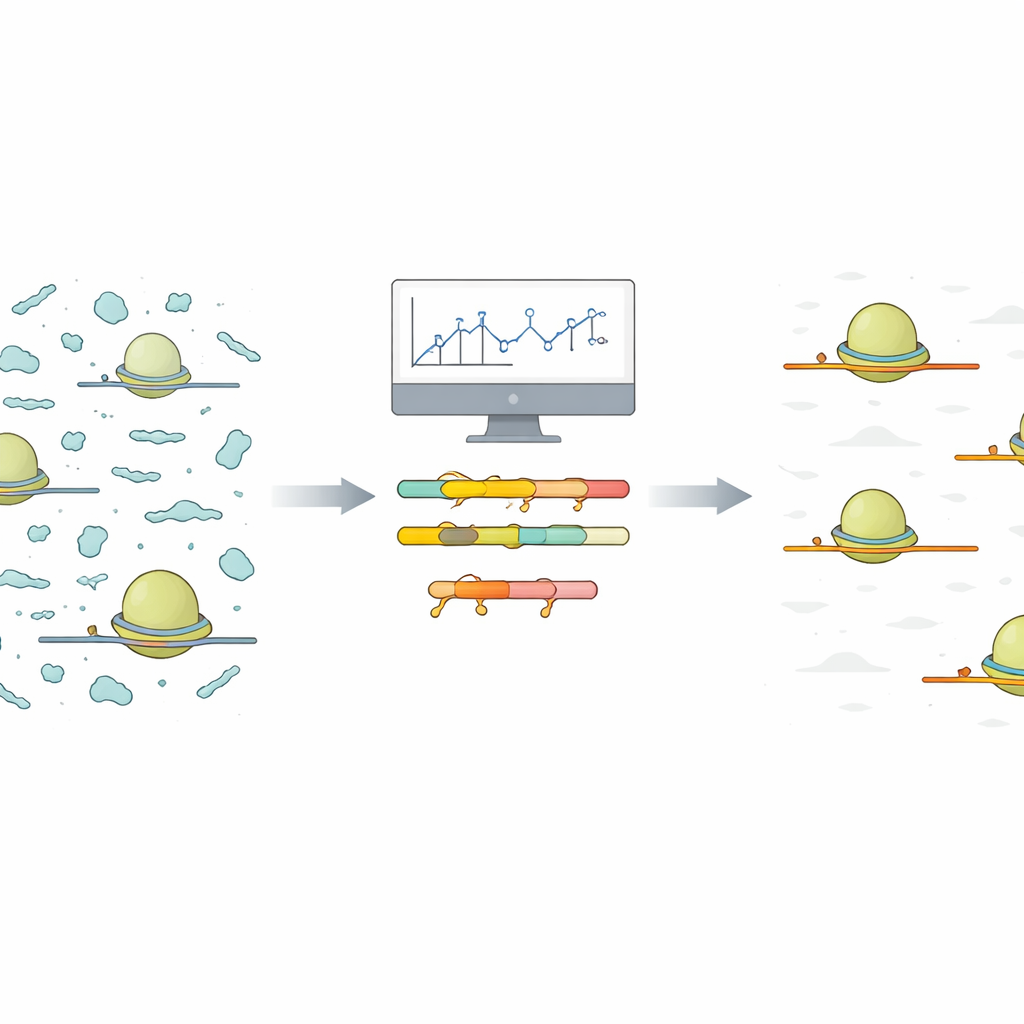
El problema de las instantáneas ruidosas de los ribosomas
Ribo‑Seq captura una instantánea momento a momento de qué mensajes en una célula se están traduciendo activamente en proteínas. Para ello, los científicos aíslan los ribosomas junto con los cortos tramos de ARN mensajero (ARNm) que protegen. Todo lo demás se descompone, y los fragmentos protegidos se secuencian y se mapean de vuelta al genoma. En la práctica, sin embargo, muchos otros pequeños fragmentos de ARN no codificante se cuelan en este proceso. Dado que estos fragmentos contaminantes son abundantes y altamente variables, consumen una gran fracción de las lecturas de secuenciación, dejando menos lecturas para las señales verdaderas de codificación proteica que interesan a los investigadores.
Por qué las técnicas actuales de limpieza son insuficientes
Las estrategias estándar intentan eliminar los abundantes ARNr y otros ARN no codificantes con sondas de captura predefinidas o enzimas. Estos métodos funcionan bien cuando los ARN objetivo están intactos y son predecibles, pero Ribo‑Seq deliberadamente fragmenta el ARN en muchos tamaños diferentes. Esa fragmentación desordena los sitios objetivo para conjuntos de sondas fijas, haciendo la depleción mucho menos eficiente. Además, la mezcla exacta de contaminantes depende de la especie estudiada, las condiciones de crecimiento e incluso de la nuclease concreta utilizada. Los flujos de trabajo de limpieza existentes también suelen implicar múltiples pasos de incubación y purificación, que consumen tiempo y pueden causar pérdida de muestra o sesgo.
Bloqueadores personalizados diseñados a partir de datos reales
Los autores proponen un enfoque simplificado que comienza con una pequeña corrida piloto de secuenciación de bajo coste bajo las mismas condiciones previstas para el experimento completo. Proporcionan un script en R que toma las lecturas alineadas de esta corrida piloto y agrupa automáticamente fragmentos contaminantes similares según su secuencia. Para cada grupo, el script informa la secuencia común más corta que aparece en los fragmentos. Estos tramos cortos y compartidos son sitios objetivo ideales para moléculas especializadas llamadas oligonucleótidos de ácido nucleico bloqueado (LNA). Los LNA son cadenas cortas con una modificación química que hace que se unan muy fuertemente al ARN coincidente. El script también genera mapas de calor y gráficos resumen intuitivos, ayudando a los usuarios a ver qué contaminantes dominan y cuántos objetivos LNA serían necesarios para una limpieza sustancial.
Una limpieza de un solo paso durante la amplificación
En lugar de eliminar físicamente los contaminantes de la muestra, el método utiliza oligonucleótidos LNA como bloqueadores durante el paso de amplificación de ADN que construye la biblioteca de secuenciación. Los autores probaron añadir estos bloqueadores ya sea durante la etapa inicial de transcripción inversa o durante la posterior amplificación por PCR. Hallaron que añadir LNA durante la amplificación era más eficiente y requería concentraciones más bajas, reduciendo un contaminante de prueba por más de mil veces y funcionando independientemente de la orientación de la hebra. Los consejos prácticos de diseño incluyen alternar bloques constructores de ADN estándar y LNA, usar una longitud mínima de 14 unidades para la planta Arabidopsis y modificar el extremo de cola para que el propio bloqueador no pueda extenderse accidentalmente.
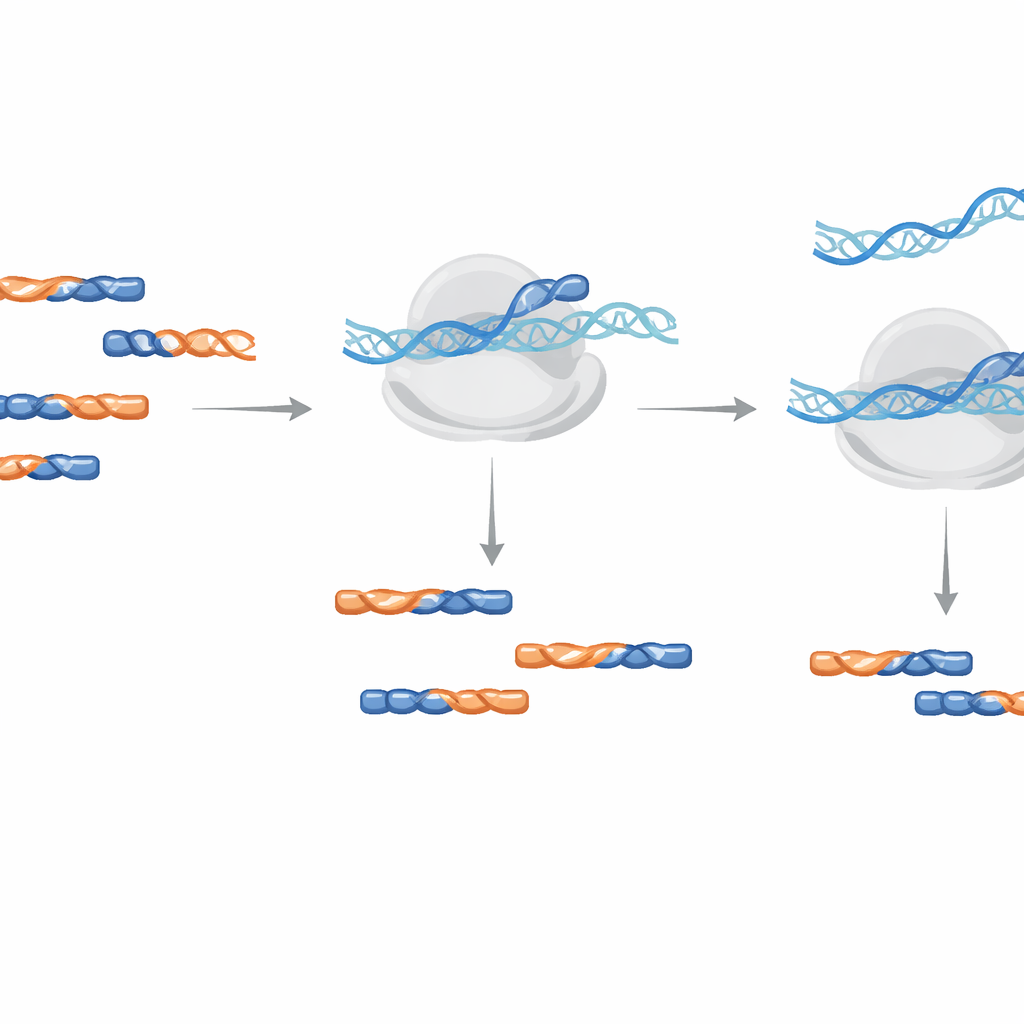
Más lecturas útiles sin distorsionar la señal
Para demostrar el rendimiento en condiciones reales, el equipo diseñó cinco bloqueadores LNA dirigidos a los grupos contaminantes más comunes observados en condiciones de crecimiento típicas de Arabidopsis. Cuando añadieron esta mezcla durante la amplificación de la biblioteca, la proporción de contaminantes identificados cayó en más de un 30%, y el número de lecturas útiles de codificación proteica casi se duplicó. De forma crucial, al comparar los conteos de lecturas a nivel de gen entre bibliotecas con y sin tratamiento con LNA, los valores concordaron casi perfectamente, lo que indica que los bloqueadores eliminaron fragmentos de desecho sin distorsionar la señal biológica procedente de huellas genuinas de ARNm.
Qué significa esto para experimentos futuros
Este trabajo muestra que un experimento piloto corto, junto con un script de análisis fácil de usar y un pequeño conjunto de bloqueadores LNA a medida, puede convertir bibliotecas de Ribo‑Seq desordenadas en conjuntos de datos mucho más limpios e informativos en un solo paso de pipeteo. Los investigadores obtienen más lecturas significativas por corrida, ahorrando costes y simplificando el diseño experimental, mientras preservan mediciones precisas de cómo se traducen los genes. Los autores también proporcionan perfiles de contaminantes y diseños de bloqueadores listos para condiciones vegetales comunes, y sugieren que recursos similares podrían crearse para muchos organismos, haciendo que el ribosome profiling de alta calidad sea más accesible en la comunidad investigadora.
Cita: Ricciardi, D.A., Peter, F.E. & Böhmer, M. Data-driven design of LNA-blockers for efficient contaminant removal in Ribo-Seq libraries. Sci Rep 16, 8565 (2026). https://doi.org/10.1038/s41598-026-43117-3
Palabras clave: perfiles de ribosomas, contaminantes de ARN, ácidos nucleicos bloqueados, limpieza de bibliotecas de secuenciación, regulación de la traducción