Clear Sky Science · es
PGE2 regula la ferroptosis y la osteogénesis de las células MC3T3-E1 a través de NOS2
Por qué el enderezamiento dental afecta a tus huesos
Los brackets y los alineadores transparentes hacen más que mover los dientes: inducen al hueso que rodea cada diente a remodelarse. Ese lento trabajo biológico de construcción es una de las razones por las que el tratamiento ortodóntico puede durar años. Este estudio se adentra en las células formadoras de hueso para entender cómo una señal inflamatoria habitual, la prostaglandina E2, podría acelerar el movimiento y a la vez debilitar en silencio el hueso nuevo, lo que apunta a vías futuras para hacer la ortodoncia más rápida y estable.
Señales liberadas cuando se empujan los dientes
Cuando un ortodoncista aplica fuerza a un diente, el ligamento y el hueso alrededor de la raíz sufren una lesión controlada. Las células de esta zona liberan mensajeros químicos, incluida la prostaglandina E2, que ayudan a coordinar cómo se degrada el hueso en un lado del diente y se reconstruye en el otro. Los autores se centraron en las células formadoras de hueso conocidas como osteoblastos, usando una línea celular de ratón estándar como modelo. Querían saber cómo la prostaglandina E2 condiciona dos resultados clave dentro de estas células: su capacidad para formar hueso mineralizado y su tendencia a sufrir una forma de muerte celular dependiente del hierro recientemente descrita, llamada ferroptosis.
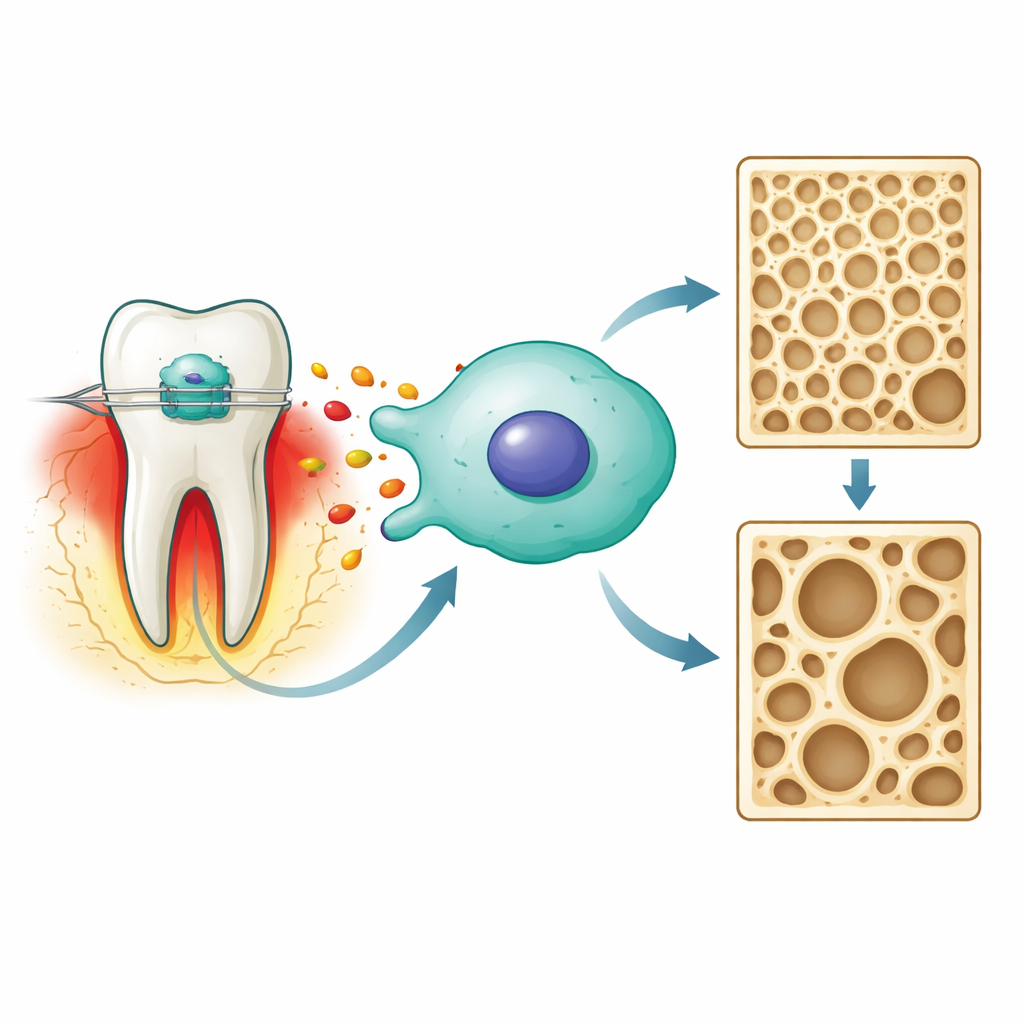
Una vía de estrés centrada en una única enzima
Usando datos genéticos de ratas sometidas a movimiento dental, el equipo buscó primero moléculas vinculadas tanto con la fuerza ortodóntica como con la ferroptosis. Un candidato, una enzima llamada sintasa de óxido nítrico 2 (NOS2), destacó como un punto central. En cultivo, exponer células osteoblásticas a una dosis clínicamente relevante de prostaglandina E2 creó un estado de inflamación “estéril”—sin gérmenes, solo estrés mecánico. Bajo esta señal aumentaron los niveles de NOS2, así como otros marcadores de estrés y moléculas reactivas de oxígeno dañinas, mientras que cayeron proteínas protectoras antioxidantes y las encargadas del manejo del hierro. En conjunto, estos cambios son características del inicio de la ferroptosis dentro de la célula.
Cuando los formadores de hueso se apagan
El mismo tratamiento con prostaglandina E2 también empeoró la capacidad de las células para comportarse como formadoras de hueso. Los marcadores clásicos de formación ósea disminuyeron, y las pruebas que visualizan el mineral óseo temprano y una enzima clave llamada fosfatasa alcalina mostraron tinción más débil y menos deposición mineral. Cuando los investigadores añadieron ferrostatina-1, un fármaco conocido por bloquear la ferroptosis, gran parte de este daño se revirtió: el estrés oxidativo disminuyó, las señales de ferroptosis se atenuaron y la actividad osteogénica se recuperó. Esto sugiere que, al menos en este modelo, la señal inflamatoria obstaculiza la formación ósea en parte al empujar a las células hacia la ferroptosis.
Regular NOS2 como un interruptor
Para comprobar si NOS2 es solo un espectador o un impulsor activo, el equipo moduló genéticamente sus niveles hacia arriba y hacia abajo. Reducir NOS2 en células tratadas con prostaglandina atenuó los marcadores de ferroptosis, disminuyó el daño oxidativo y restauró el comportamiento formador de hueso a niveles cercanos a lo normal. La sobreexpresión de NOS2 tuvo el efecto contrario: intensificó el estrés y suprimió aún más los rasgos constructores de hueso. De forma llamativa, aumentar NOS2 por sí sola—sin añadir prostaglandina E2—fue suficiente para desencadenar cambios similares a la ferroptosis y frenar la osteogénesis. Esto demuestra que NOS2 no solo responde a la inflamación; puede por sí misma empujar a los osteoblastos a alejarse de la formación de hueso mineralizado y resistente.
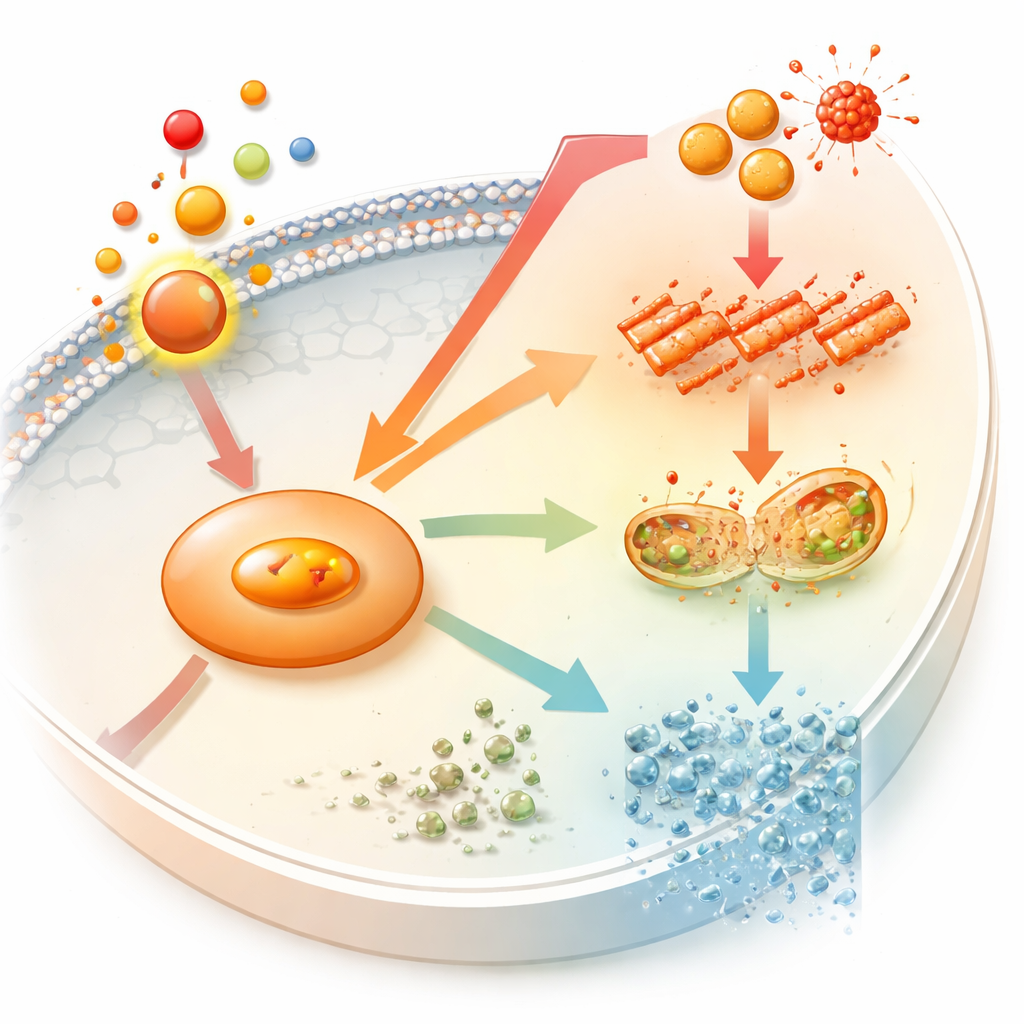
Qué significa esto para los futuros brackets
En conjunto, estos experimentos describen un nuevo eje en la biología ósea durante el movimiento dental: la prostaglandina E2 eleva NOS2, NOS2 alimenta el daño oxidativo y la ferroptosis, y la capacidad de formar hueso disminuye. Para los pacientes, esto no significa que los brackets sean inseguros, pero sí explica por qué el tratamiento puede ser un equilibrio delicado entre mover los dientes rápidamente y preservar un hueso fuerte a su alrededor. A largo plazo, fármacos o materiales que modulen finamente la actividad de NOS2 o protejan a los osteoblastos de la ferroptosis podrían ayudar a los ortodoncistas a acortar los tiempos de tratamiento manteniendo, o incluso mejorando, la calidad y la estabilidad del hueso de soporte.
Cita: Sun, M., Yang, Y., Pang, L. et al. PGE2 regulates ferroptosis and osteogenesis of MC3T3-E1 cells via NOS2. Sci Rep 16, 8893 (2026). https://doi.org/10.1038/s41598-026-43001-0
Palabras clave: movimiento dentario ortodóntico, remodelación ósea, ferroptosis, sintasa de óxido nítrico, función osteoblástica