Clear Sky Science · es
Explorando el doble papel de las vesículas extracelulares en la coagulación y la modulación inmune en el glioblastoma
Por qué importan los coágulos en el cáncer cerebral
Las personas diagnosticadas con glioblastoma, la forma más agresiva de cáncer cerebral, a menudo se enfrentan a un peligro inesperado: coágulos sanguíneos peligrosos en las piernas o el cerebro. Estos coágulos pueden acortar la supervivencia y complicar tratamientos ya exigentes. Este estudio plantea una pregunta simple pero crucial: ¿qué tienen las células de glioblastoma que hace que la sangre a su alrededor sea tan proclive a coagular, y cómo las pequeñas partículas que desprenden en la sangre también remodelan las defensas inmunitarias del organismo?
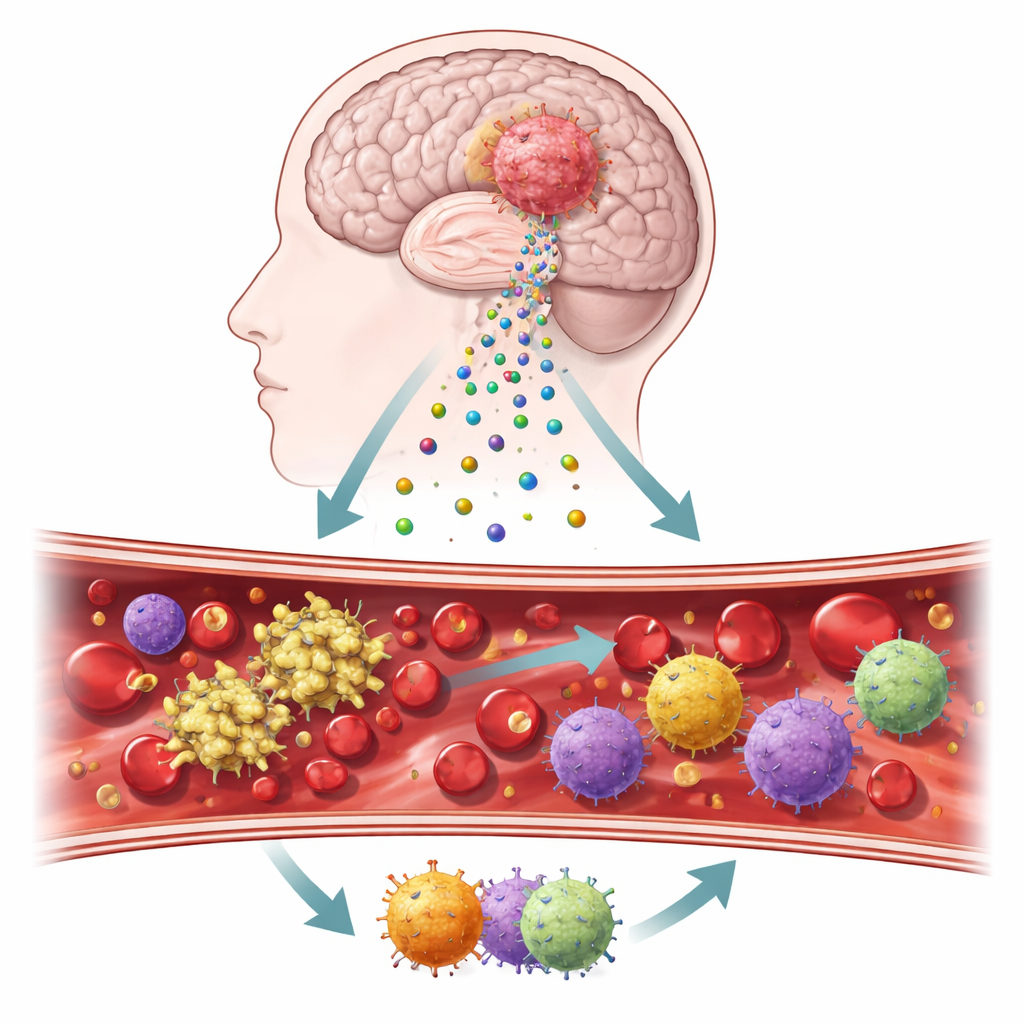
Mensajeros minúsculos que salen de un tumor cerebral
Los investigadores se centraron en burbujas microscópicas llamadas vesículas extracelulares, que brotan de las células tumorales y circulan por la sangre y el tejido cerebral. Estas vesículas llevan en su superficie dos proteínas clave, el factor tisular y la podoplanina, que se sabe que desencadenan la formación de coágulos e influyen en la inflamación. Usando muestras tumorales, sangre recogida durante la cirugía y cultivos celulares derivados de los tumores de los pacientes, el equipo construyó un flujo de trabajo por etapas para rastrear cómo se comportan estas moléculas en pacientes reales y en pruebas de laboratorio controladas. También compararon tejido tumoral con cerebro normal para ver con qué intensidad se activaban estas señales vinculadas a la coagulación.
Una sangre aparentemente tranquila, pero una zona tumoral predispuesta
Las pruebas hospitalarias estándar sugirieron que, antes de la cirugía, la sangre de muchos pacientes parecía sorprendentemente normal: los tiempos de coagulación habituales y los valores de firmeza del coágulo estaban en gran medida dentro de los rangos de referencia. Sin embargo, cuando los científicos examinaron los propios tumores, emergió una imagen diferente. El tejido de glioblastoma mostró de forma consistente niveles altos de factor tisular y podoplanina y niveles muy bajos de un freno natural llamado inhibidor de la vía del factor tisular. Las líneas celulares tumorales derivadas de pacientes mantuvieron en gran medida este patrón en cultivo, confirmando que la firma «propicia para la coagulación» es una característica intrínseca de las células cancerosas. Cuando estas células, o las vesículas que liberaban, se mezclaron con plasma en el laboratorio, los coágulos se formaron más rápido, especialmente a través de la llamada vía extrínseca que depende del factor tisular.
Diferentes células tumorales, distintas estrategias de coagulación
No todos los glioblastomas se comportaron igual. Algunas líneas celulares derivadas de pacientes tenían mucho factor tisular, otras presentaban más podoplanina y algunas tenían poco de ambos. Las células ricas en factor tisular fueron las más potentes para acortar el tiempo de coagulación, mientras que las células ricas en podoplanina contribuyeron de forma modesta mediante efectos sobre las plaquetas. Cuando una de estas líneas celulares se separó en subgrupos que expresaban solo factor tisular, solo podoplanina, ambos o ninguno, las células no conservaron esos perfiles por mucho tiempo. A lo largo de tres semanas, tendieron a regresar hacia perfiles mixtos, revelando un alto grado de plasticidad. Esta remodelación dinámica se acompañó de cambios en el estrés oxidativo dentro de las células, lo que sugiere que el estrés químico en el tumor puede empujar a las células hacia estados más procoagulantes.
Vesículas que moldean la inmunidad cerebral y sanguínea
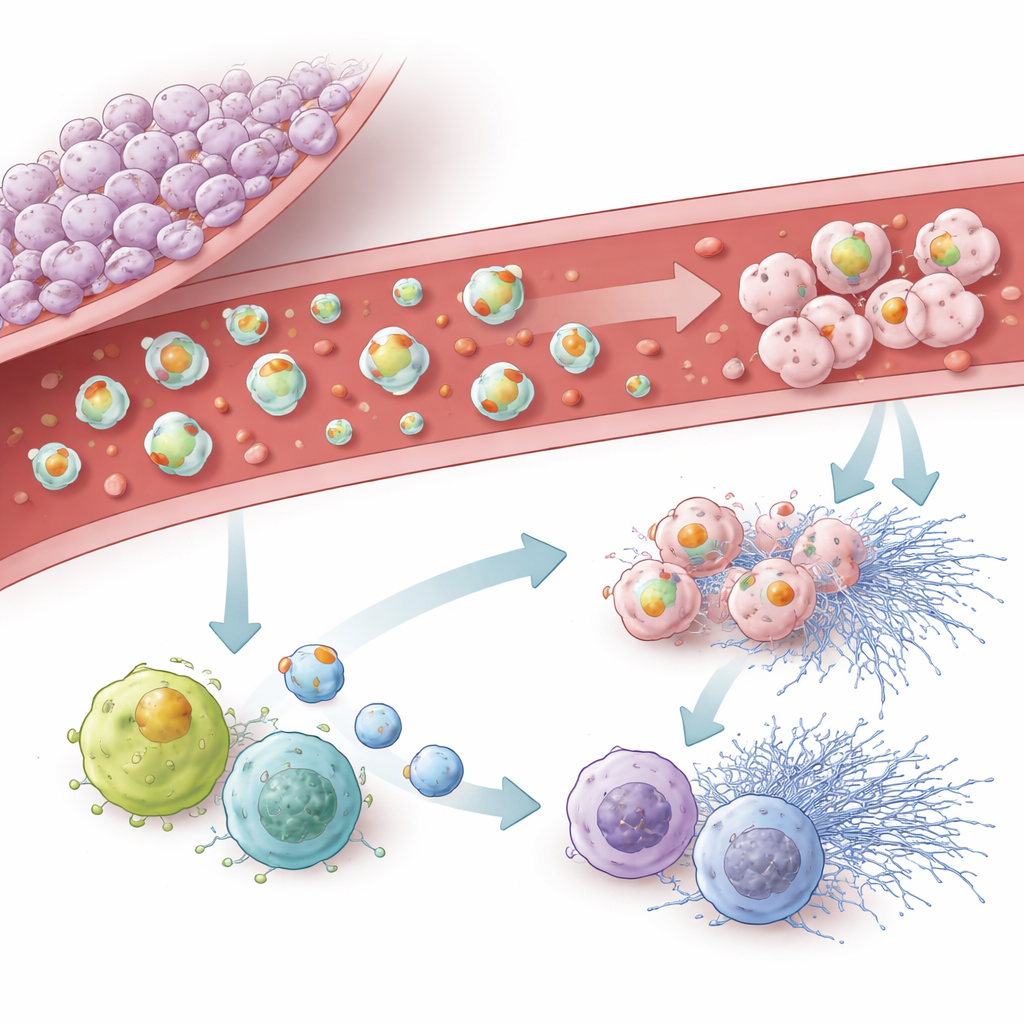
El equipo profundizó luego en cómo las vesículas derivadas del tumor influyen en las propias células inmunes del cerebro, llamadas microglía, y en los glóbulos blancos circulantes y neutrófilos. Las vesículas de líneas tumorales altamente procoagulantes fueron fácilmente captadas por la microglía y ralentizaron su migración, al tiempo que las orientaron hacia un estado más inflamatorio, similar a «M1», y mostraron signos de envejecimiento celular. En la sangre, las vesículas ricas en factor tisular activaron leucocitos, aumentaron la producción de especies reactivas de oxígeno y promovieron la liberación de estructuras pegajosas en forma de red por parte de los neutrófilos, conocidas como trampas extracelulares. Las vesículas que portaban podoplanina fueron menos potentes a la hora de impulsar estas reacciones inmunes explosivas pero fomentaron con fuerza un programa similar a la senescencia, en el que las células inmunes dejan de dividirse y alteran su comportamiento. Incluso las vesículas que carecían de ambas proteínas clave todavía podían provocar cierta senescencia, lo que implica que otros componentes de su carga también importan.
Qué significa esto para los pacientes y la atención futura
En conjunto, los hallazgos muestran que el glioblastoma no simplemente espesa la sangre en todas partes. En lugar de eso, el tumor y las vesículas que libera crean una zona localizada y muy compleja donde la coagulación y la inflamación se retroalimentan. El factor tisular emerge como el motor principal de la formación de coágulos y de la activación inflamatoria, mientras que la podoplanina añade su propia influencia sobre las plaquetas, el envejecimiento inmune y el comportamiento microglial. Dado que estas vesículas circulan y reflejan el estado del tumor, podrían servir en el futuro como marcadores basados en sangre para identificar a pacientes con un riesgo especialmente alto de coágulos. También podrían señalar estrategias de prevención más personalizadas que apunten a la maquinaria procoagulante del tumor sin afinar la sangre de forma generalizada.
Cita: Wolff, A., Waitz, G., Kaps, P. et al. Exploring the dual role of extracellular vesicles in coagulation and immune modulation in glioblastoma. Sci Rep 16, 9534 (2026). https://doi.org/10.1038/s41598-026-42867-4
Palabras clave: glioblastoma, coágulos sanguíneos, vesículas extracelulares, microambiente tumoral, respuesta inmune