Clear Sky Science · es
Análisis multiómico de NEDD1 en carcinoma hepatocelular: función biológica, valor pronóstico y significado clínico
Por qué esto importa para pacientes y familias
La mayoría de los cánceres de hígado se detectan tarde, cuando las opciones de tratamiento son limitadas y la supervivencia es baja. Los médicos necesitan con urgencia mejores señales de alerta en sangre o tejido para detectar los tumores antes y elegir la terapia adecuada para cada persona. Este estudio se centra en una proteína poco conocida llamada NEDD1 y plantea una pregunta sencilla con grandes consecuencias: ¿puede esta molécula ayudar a explicar por qué algunos cánceres de hígado crecen más rápido y resisten los tratamientos inmunitarios modernos, y podría convertirse en un nuevo objetivo para el diagnóstico y la terapia?
Un nuevo sospechoso en el crecimiento del cáncer de hígado
Los investigadores empezaron revisando grandes bases de datos públicas de cáncer y muestras de su propio hospital para ver cuánto NEDD1 está presente en distintos tejidos. Encontraron que los niveles de NEDD1 eran más altos en muchos tipos de cáncer y, en especial, en el carcinoma hepatocelular, la forma más común de cáncer de hígado, en comparación con hígado sano. Los pacientes cuyos tumores presentaban más NEDD1 tendían a vivir menos tiempo y eran más propensos a que su enfermedad reapareciera o empeorara. Modelos estadísticos que combinaron NEDD1 con información clínica habitual sugirieron que esta proteína tiene un valor pronóstico independiente, lo que significa que puede ayudar a los médicos a predecir mejor cómo se comportará el cáncer en un individuo.
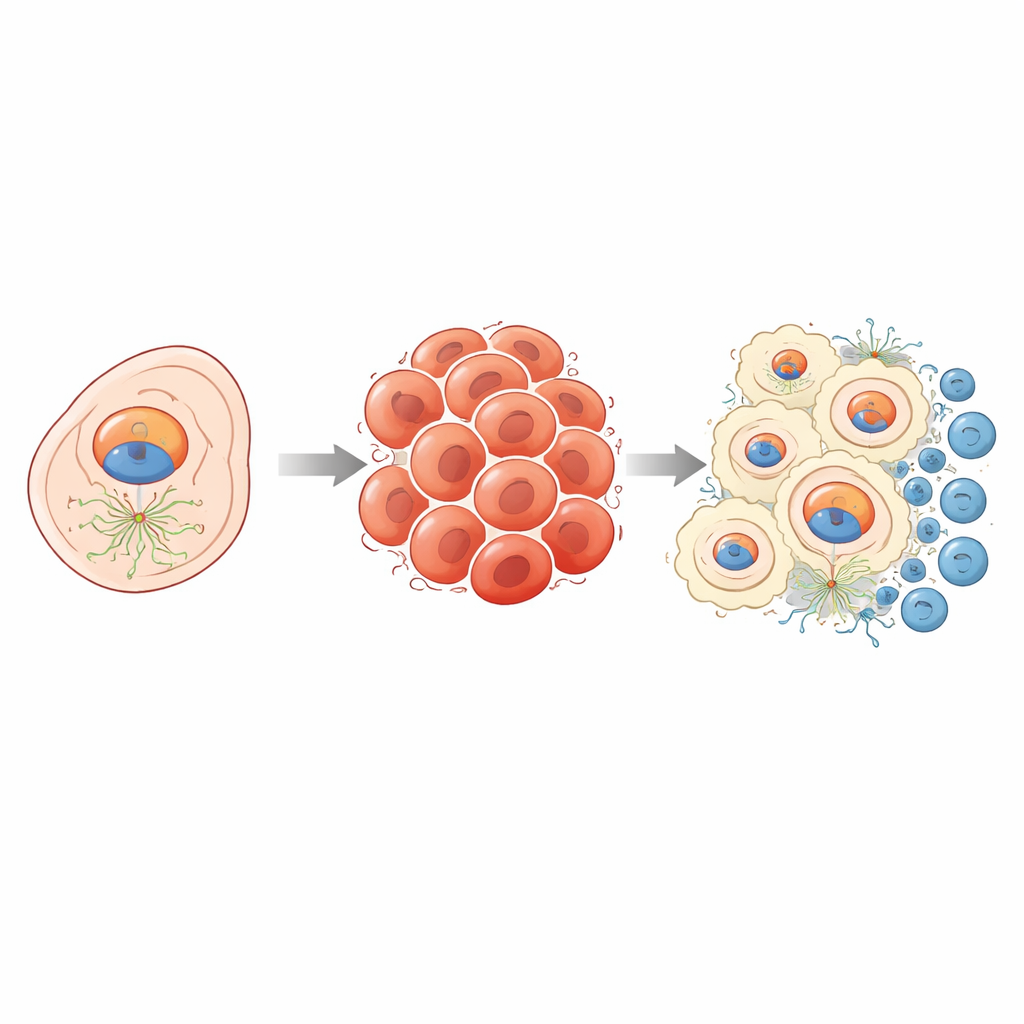
Cómo NEDD1 ayuda a que los tumores se dividan y se diseminen
NEDD1 normalmente contribuye a organizar el andamiaje interno que las células usan para separar sus cromosomas durante la división. Cuando este proceso está sobreactivado en el cáncer, las células pueden multiplicarse sin control. Al comparar tumores con niveles altos y bajos de NEDD1, el equipo observó que genes implicados en el ciclo celular, la adhesión celular y vías de crecimiento bien conocidas se activaban junto con NEDD1. En experimentos de laboratorio, las células de cáncer de hígado a las que se les redujo NEDD1 ralentizaron su crecimiento, formaron menos colonias y tuvieron menor capacidad de migración—comportamientos asociados a una menor agresividad. En ratones, los tumores formados por células con NEDD1 silenciado crecieron mucho más despacio, y la tinción de los tejidos mostró un cambio hacia un estado celular menos invasivo, con descenso de marcadores de diseminación y proliferación.
Capas ocultas de control y pistas para el tratamiento
El estudio también exploró por qué NEDD1 se vuelve sobreactivo. Los autores descubrieron que un tramo regulador del ADN cerca del gen NEDD1 estaba menos «metilado» químicamente en los tumores hepáticos que en el tejido hepático normal. Esta pérdida de metilación suele asociarse a una activación excesiva de genes. Los pacientes cuyos tumores combinaban baja metilación con altos niveles de NEDD1 tuvieron resultados particularmente malos, lo que sugiere que este cambio epigenético podría ser uno de los desencadenantes de la sobreactivación de NEDD1. Además, ciertas marcas químicas llamadas grupos fosfato en la proteína NEDD1 eran más frecuentes en los tumores, destacando un sitio (s523) vinculado a peor pronóstico. Mediante el cribado de bases de datos de respuesta a fármacos, el equipo identificó varios compuestos existentes—como axitinib, topotecán y pevonidistat—que, al menos en modelos computacionales, podrían funcionar mejor en cánceres con alta actividad de NEDD1.
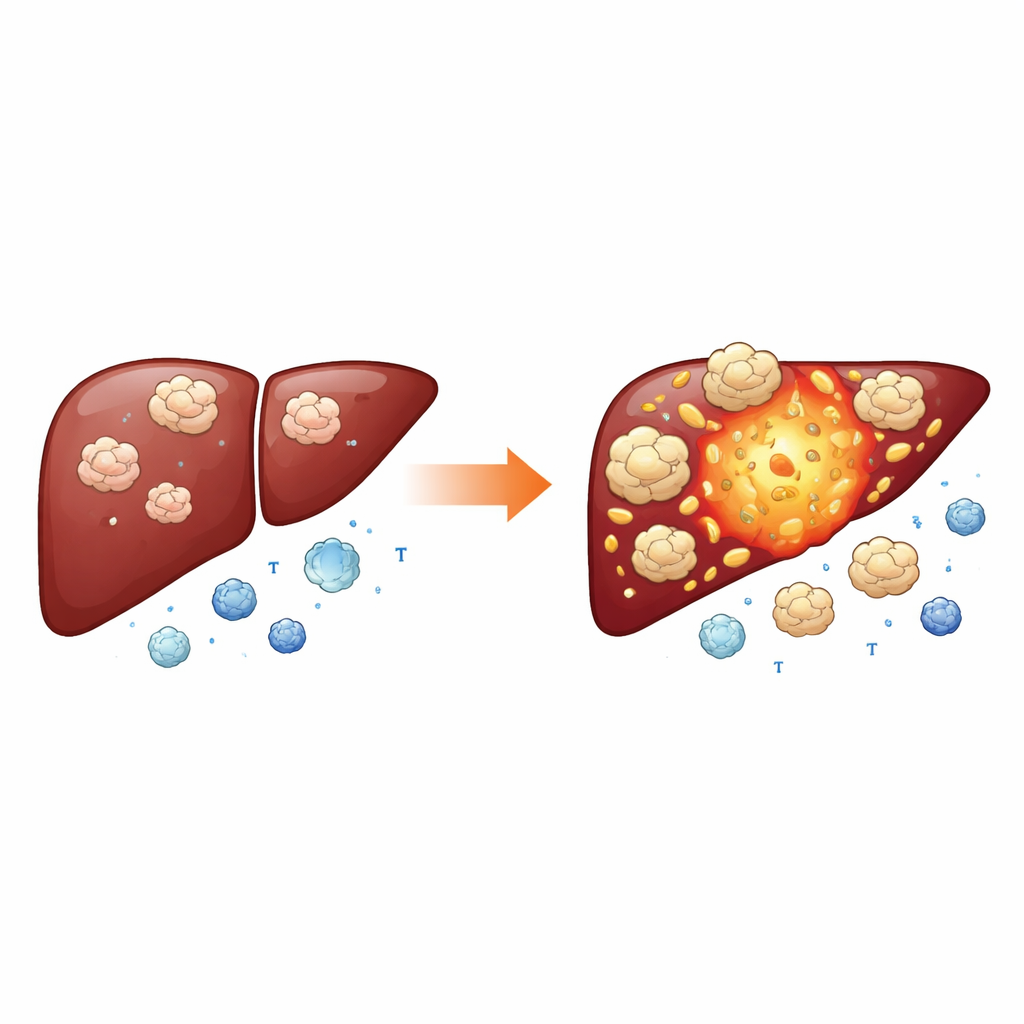
Configurando una «zona segura» inmune para el tumor
Las inmunoterapias modernas intentan liberar a las células T del propio organismo contra el cáncer bloqueando frenos como PD-1 y CTLA-4. De forma intrigante, los tumores con más NEDD1 también presentaban niveles más altos de estas moléculas de control inmunitario, y los pacientes con bajos niveles de NEDD1 parecían tener más probabilidad de beneficiarse de fármacos que bloquean los puntos de control. Para entender por qué, los investigadores recurrieron a datos de transcriptómica de célula única y de mapeo espacial, que revelan qué células en un tumor expresan qué genes y dónde se localizan. Encontraron que NEDD1 suele actuar junto con otra proteína, MZT2B, formando un par funcional que aparece no solo en las células tumorales sino también en un grupo especial de macrófagos enriquecidos en la molécula APOE. Estos macrófagos se han asociado en otros cánceres con diseminación y resistencia a la inmunoterapia. El par NEDD1–MZT2B se concentró a veces en nichos ricos en macrófagos y otras veces en conglomerados de células tumorales, lo que sugiere un módulo flexible que distintos tipos celulares pueden usar para apoyar el crecimiento tumoral y atenuar el ataque inmune.
Qué podría significar esto para la atención futura
En pocas palabras, este trabajo dibuja a NEDD1 tanto como un motor de crecimiento dentro de las células del carcinoma hepatocelular como un posible arquitecto de un refugio inmune alrededor del tumor. Su sobreactividad, probablemente impulsada por cambios en las marcas del ADN y en el etiquetado de proteínas, se asocia con una progresión más rápida de la enfermedad, respuestas más débiles a la inmunoterapia y un patrón distintivo de cooperación con ciertas células inmunes. Aunque queda mucho por probar en cohortes de pacientes más grandes y en modelos más refinados, NEDD1 surge ahora como un biomarcador prometedor para ayudar a estratificar el riesgo y guiar el tratamiento—y como un posible objetivo para nuevos fármacos dirigidos a frenar el cáncer de hígado y mejorar la eficacia de las terapias inmunitarias.
Cita: Chen, Y., Wan, Z., Xie, H. et al. Multi-omics analysis of NEDD1 in hepatocellular carcinoma: biological function, prognostic value, and clinical significance. Sci Rep 16, 11383 (2026). https://doi.org/10.1038/s41598-026-42505-z
Palabras clave: carcinoma hepatocelular, NEDD1, microambiente tumoral, inmunoterapia contra el cáncer, biomarcadores