Clear Sky Science · es
GV1001 reduce la tau patológica 4R y los déficits funcionales en modelos relevantes para la parálisis supranuclear progresiva
Por qué esto importa para las personas y las familias
La parálisis supranuclear progresiva (PSP) es un trastorno cerebral raro pero devastador que priva a las personas del equilibrio, el movimiento y la claridad mental en apenas unos años. Actualmente no existen medicamentos que puedan ralentizar su progresión. Este estudio explora una pequeña molécula, GV1001, desarrollada originalmente para el cáncer, y muestra que puede aliviar los problemas de movimiento y reducir cambios celulares clave relacionados con la enfermedad en modelos de laboratorio de la PSP. El trabajo sugiere una nueva vía para abordar un grupo de enfermedades impulsadas por una forma dañina de la proteína tau.
El auxiliar del tráfico cerebral que se estropea
Muchas enfermedades cerebrales implican la tau, una proteína que normalmente ayuda a estabilizar las “vías” internas por las que viajan materiales dentro de las neuronas. En la PSP, una forma particular llamada tau 4R se acumula en ciertas regiones profundas del cerebro, especialmente en el mesencéfalo, donde altera la estructura celular, daña las conexiones y acaba provocando la muerte celular. Las personas desarrollan rigidez, caídas, problemas en los movimientos oculares y dificultades cognitivas, con frecuencia empeorando rápidamente en cinco a ocho años. A diferencia de la enfermedad de Alzheimer, la PSP está dominada por esta forma 4R de la tau, lo que la convierte en un objetivo importante para tratamientos dirigidos específicamente a las tauopatías relacionadas con el movimiento.
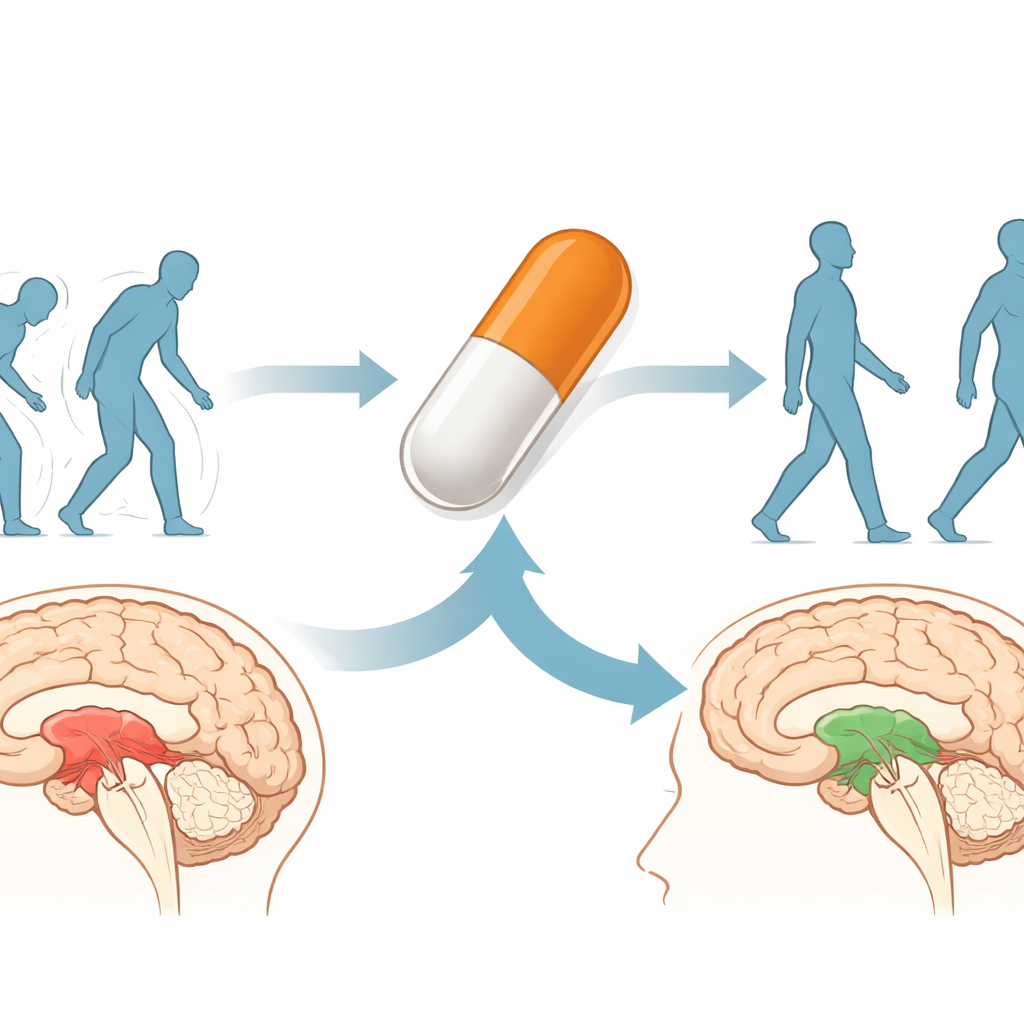
Un candidato para cáncer encuentra un nuevo papel
GV1001 es un péptido corto derivado de la telomerasa humana, una enzima activa en muchos cánceres. Ya se ha probado en varios tumores y, más recientemente, en condiciones como la hiperplasia prostática y la enfermedad de Alzheimer, con un historial de seguridad en general favorable. Trabajos anteriores mostraron que GV1001 puede proteger a las neuronas del daño oxidativo, apoyar a las mitocondrias productoras de energía y calmar las respuestas inflamatorias en el cerebro. El estudio actual plantea si estas acciones protectoras amplias, además de posibles efectos nuevos, podrían hacer que GV1001 sea útil en trastornos donde la tau 4R es la principal culpable, como la PSP.
Evaluación del movimiento, la memoria y los cambios cerebrales en ratones
Los investigadores usaron un ratón especialmente diseñado que produce una tau 4R similar a la humana, proclive a agregarse, provocando con el tiempo problemas de movimiento y memoria. A partir de los siete meses de edad, estos ratones recibieron GV1001 por vía subcutánea tres veces por semana durante aproximadamente cinco meses. En comparación con los animales sin tratar, los ratones tratados con GV1001 aguantaron más tiempo en una barra giratoria, recorrieron distancias mayores y a mayor velocidad en una arena abierta y mostraron mejor reconocimiento de objetos nuevos, lo que sugiere mejoras en la motricidad y la memoria. Al examinar los cerebros, los investigadores encontraron menos agregados de tau y menos marcas químicas asociadas con la tau “hiperactiva” en múltiples regiones, incluyendo la corteza, el hipocampo y la sustancia negra, todas áreas importantes para el movimiento y la cognición.
Mirando dentro de las células cerebrales y calmando la inflamación cerebral
Más allá de la propia tau, la PSP y enfermedades relacionadas presentan pérdida de sinapsis —los puntos de contacto entre neuronas— y sobreactivación de células de soporte llamadas astrocitos y microglía, que impulsan una inflamación crónica. En los ratones tratados, los niveles de proteínas sinápticas clave volvieron hacia valores normales, lo que sugiere que GV1001 ayuda a preservar las conexiones neuronales. Los marcadores de astrocitos y microglía activados disminuyeron, tanto en cerebros de ratón como en líneas celulares humanas estimuladas para imitar la inflamación. El fármaco también redujo los niveles de TSPO, una proteína utilizada en imágenes cerebrales para seguir la inflamación, lo que abre la posibilidad de que en el futuro la imagenología pueda monitorizar el impacto de GV1001 en pacientes.
Apuntando directamente a la forma dañina 4R de la tau
Para comprobar si GV1001 afecta más específicamente a la tau 4R, el equipo creó un modelo celular de PSP diferenciando células humanoides neuronales y exponiéndolas a la anonacina, una toxina vegetal que daña las mitocondrias y aumenta la tau 4R. Como era de esperar, la anonacina incrementó marcadamente la cantidad de tau 4R sin cambiar la tau total. Cuando se añadió GV1001 tras el inicio de este daño, los niveles excesivos de tau 4R y la proporción de tau 4R respecto a la tau total volvieron hacia valores normales, mientras que la tau global se mantuvo mayormente sin cambios. Reducciones selectivas similares de la tau 4R se observaron en los cerebros de los ratones tratados. Estos hallazgos sugieren que GV1001 hace más que proteger las células de forma general: parece reducir la misma forma de tau más estrechamente ligada a la PSP.
Qué podría significar esto para tratamientos futuros
En conjunto, los resultados muestran que GV1001 puede mejorar el movimiento y la memoria, reducir los cambios tóxicos de la tau, preservar sinapsis y atenuar la inflamación cerebral en modelos que imitan aspectos clave de la PSP y de otras enfermedades impulsadas por tau 4R. Las pruebas clínicas iniciales en personas con PSP ya han sugerido un enlentecimiento del empeoramiento de los síntomas y buena tolerabilidad, aunque se necesitan estudios mucho más amplios y prolongados. Para pacientes y familias, este trabajo ofrece un optimismo cauto de que un fármaco diseñado originalmente para el cáncer podría reutilizarse para frenar el curso de una enfermedad cerebral de rápido avance al atacar su anormalidad proteica central.
Cita: Jang, KB., Kang, D.M., Lee, MH. et al. GV1001 reduces pathological 4R tau and functional deficits in models relevant to progressive supranuclear palsy. Sci Rep 16, 8638 (2026). https://doi.org/10.1038/s41598-026-42195-7
Palabras clave: parálisis supranuclear progresiva, proteína tau, tauopatía 4R, neuroinflamación, GV1001