Clear Sky Science · es
Visualización de la progresión maligna: ensayo de inmunofluorescencia espacial in situ basado en CD109 que delimita la transformación de carcinoma papilar a anaplásico de tiroides dentro del microambiente tumoral
Por qué importa este estudio sobre cáncer de tiroides
El carcinoma anaplásico de tiroides es uno de los cánceres humanos más letales, y con frecuencia convierte un tumor tiroideo que suele ser curable en una enfermedad rápidamente fatal. Sin embargo, los médicos aún no comprenden del todo cómo un carcinoma papilar de tiroides, común y de crecimiento lento, puede transformarse de forma abrupta en esta variante agresiva. Este estudio sigue esa transformación directamente dentro del tumor de un paciente, usando una técnica de imagen nueva para observar cómo las células cancerosas y su microvecindario cambian paso a paso. El trabajo ofrece una imagen más detallada de cómo el entorno local del tumor puede empujar a las células hacia un estado más letal, sugiriendo nuevas vías para frenar o prevenir esta transición.
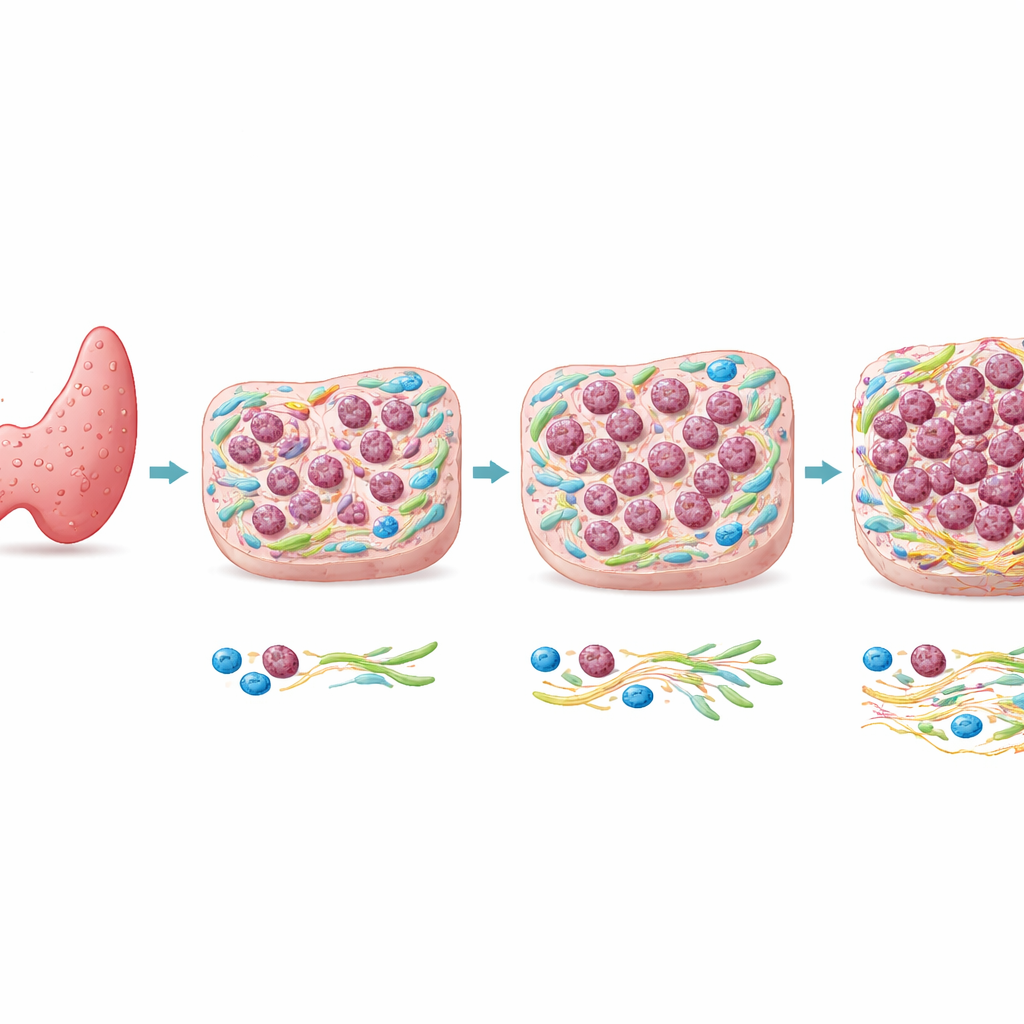
De un tumor común a un asesino raro
La mayoría de los cánceres de tiroides son carcinomas papilares de tiroides (CPT), que por lo general crecen despacio y tienen resultados excelentes. El carcinoma anaplásico de tiroides (CAT), en contraste, es raro pero a menudo fatal en cuestión de meses. Estudios genéticos han mostrado que el CAT y el CPT adyacente en el mismo paciente frecuentemente comparten muchas de las mismas mutaciones del ADN, incluidas alteraciones en genes cancerígenos bien conocidos. Esa semejanza sugiere que los genes por sí solos pueden no explicar por qué solo algunas regiones de un tumor se vuelven anaplásicas. Por ello, los autores se centraron en lo que ocurre en el paisaje tisular alrededor de las células—el microambiente tumoral—para ver si las condiciones locales ayudan a impulsar este cambio peligroso.
Una nueva forma de cartografiar el cáncer in situ
El equipo desarrolló un ensayo de inmunofluorescencia espacial (SPI), un tipo de microscopía multicolor que mide la intensidad de proteínas específicas en mosaicos pequeños y definidos a lo largo de una sección de tejido. Centraron este método en CD109, una proteína de superficie que identificaron como marcador de comportamiento maligno en tejido tiroideo, y en CK8/18, una proteína característica de las células tumorales papilares ordinarias. Calculando la proporción de CD109 respecto a CK8/18 en cientos de pequeñas regiones, generaron mapas codificados por color que separaron áreas claras de CPT de áreas claras de CAT y, crucialmente, revelaron zonas intermedias donde ambos marcadores se solapaban. En lugar de una frontera nítida, la transición de cáncer papilar a anaplásico apareció como un continuo gradual y parcheado.
Cinco zonas a lo largo de un camino de cambio
Para comprender mejor este continuo, los investigadores dividieron el tejido en cinco regiones, desde CPT puro hasta CAT totalmente desarrollado. Luego examinaron muchas proteínas adicionales que informan sobre la identidad celular, crecimiento, movimiento y el tejido de sostén. A lo largo de estas regiones, rasgos epiteliales clásicos como E-cadherina y CK8/18 disminuyeron de forma sostenida, mientras que los marcadores vinculados a la motilidad celular y al cambio de forma, como la vimentina, aumentaron. Las proteínas que indican división celular rápida se incrementaron en las zonas más anaplásicas. Al mismo tiempo, las células de soporte circundantes—fibroblastos asociados al cáncer—y las células inmunitarias, especialmente ciertos macrófagos, se volvieron más numerosas y más activadas, y aumentaron las proteínas que producían.
Cuando el andamiaje tumoral se vuelve hostil
Se observó un cambio llamativo en el andamiaje del tumor, o matriz extracelular. En las regiones anaplásicas, células con apariencia de fibroblasto depositaron más colágenos de los tipos III y VI y una proteína de matriz llamada TGFBI, y estas fibras eran más gruesas, enredadas y orientadas en múltiples direcciones en lugar de en líneas suaves y paralelas. Esta malla reorganizada probablemente aumenta la rigidez mecánica del tejido. En estas zonas más rígidas, una proteína de señalización sensible a la presión llamada YAP estaba más activa tanto en las células cancerosas como en las de sostén. Las mismas áreas mostraron más signos de daño del ADN y de una forma de muerte celular inflamatoria, junto con la liberación de proteínas S100 que pueden actuar como señales de peligro y agravar la inflamación local. Los autores proponen que esta combinación de compresión, muerte celular e inflamación crónica favorece la supervivencia y el diseminamiento de células cancerosas ya mutadas que pueden resistir el estrés y sufrir una transición tipo epitelio-mesénquima.
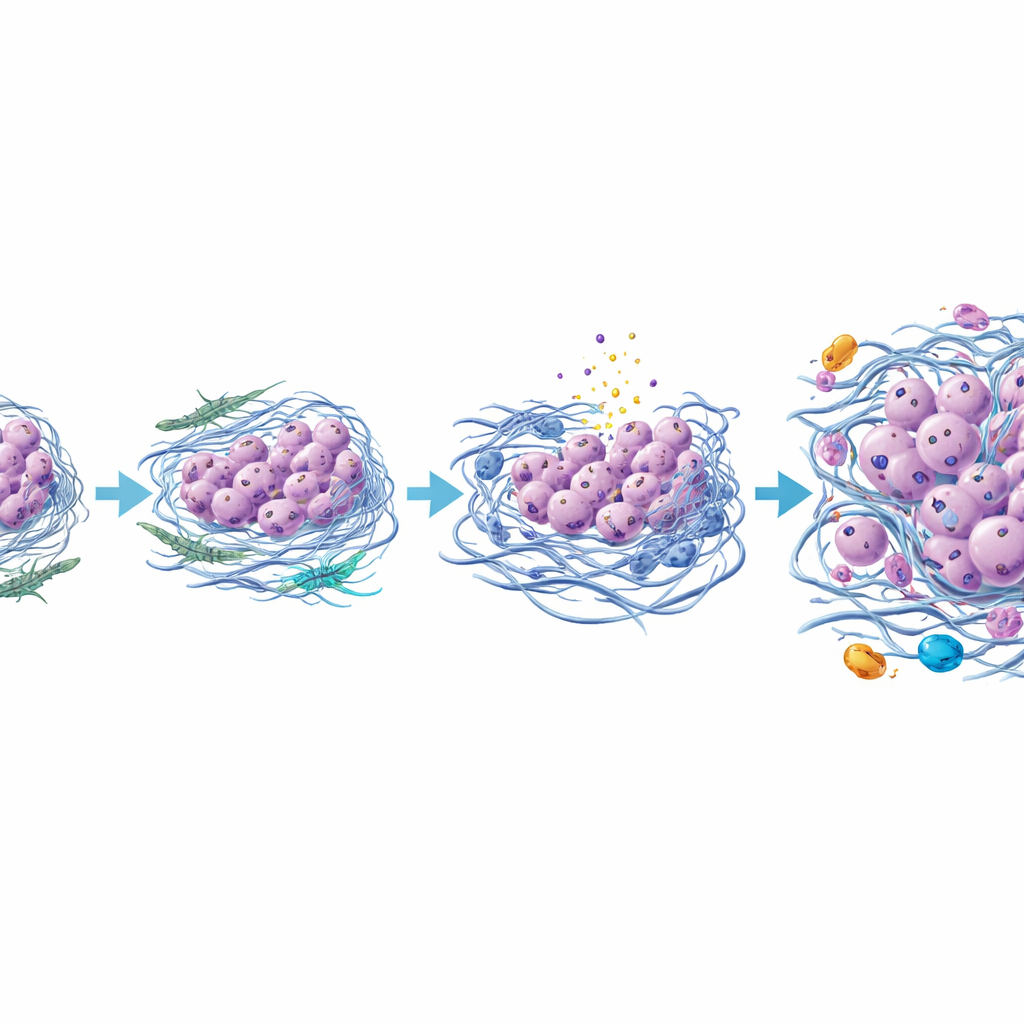
Una nueva imagen de cómo un tumor tiroideo se vuelve letal
Juntando estos hallazgos, el estudio sugiere que el carcinoma anaplásico de tiroides surge no solo por mutaciones genéticas adicionales sino por un vecindario remodelado alrededor del tumor. A medida que las células tumorales papilares y las células de soporte cercanas interactúan, algunos fibroblastos evolucionan hacia un tipo más agresivo que engrosa y endurece la matriz circundante, comprime células vulnerables hasta la muerte y recluta células inmunitarias inflamatorias. Las células cancerosas supervivientes, más resistentes, pierden progresivamente sus rasgos tiroideos originales y adoptan una identidad más móvil e invasiva, formando finalmente un tumor anaplásico. Aunque este trabajo se basa en un solo caso bien estudiado y necesita confirmación en más pacientes, presenta una herramienta de imagen poderosa y un modelo detallado en el que dirigir las células de soporte del tumor, la matriz o las señales inflamatorias podría ayudar a prevenir o retrasar una de las transformaciones más temidas en el cáncer de tiroides.
Cita: Cohen, T., Suzuki, K., Matsuda, K. et al. Visualizing malignant progression: in situ CD109-based spatial immunofluorescence assay delineates papillary to anaplastic thyroid carcinoma transformation within the tumor microenvironment. Sci Rep 16, 8682 (2026). https://doi.org/10.1038/s41598-026-41927-z
Palabras clave: carcinoma anaplásico de tiroides, carcinoma papilar de tiroides, microambiente tumoral, rigidez de la matriz extracelular, inmunofluorescencia espacial