Clear Sky Science · es
Análisis de vesículas extracelulares derivadas de células epiteliales bronquiales mediante citometría de flujo convencional, de imagen y a escala nanométrica
Por qué importan las burbujas diminutas en los pulmones
Nuestros pulmones están revestidos por células que mantienen una comunicación constante con el sistema inmunitario, especialmente cuando inhalamos polvo, contaminación o gérmenes. Gran parte de esta “conversación” se produce a través de burbujas microscópicas llamadas vesículas extracelulares: paquetes de lípidos y proteínas liberados por las células. Estas vesículas pueden empeorar o atenuar las enfermedades pulmonares, y podrían en el futuro servir como señales tempranas para afecciones como el asma, la enfermedad pulmonar obstructiva crónica (EPOC) y la fibrosis. Este estudio explora la mejor manera de medir estas partículas elusivas usando distintos tipos de instrumentos láser avanzados, con la idea de hacer esas mediciones prácticas para la investigación y posibles pruebas clínicas futuras.
Mensajes invisibles de las células de las vías aéreas
Las vesículas extracelulares (VE) son paquetes diminutos envueltos por una membrana que casi todas las células liberan a fluidos como la sangre, la orina y la fina capa líquida que recubre nuestras vías respiratorias. Las VE procedentes de células epiteliales bronquiales humanas —las células que recubren los conductos respiratorios— ya se han vinculado a varios procesos pulmonares: pueden influir en el desarrollo de alergias, ayudar a combatir infecciones respiratorias, modelar la estructura de las vías en la EPOC e incluso limitar la formación de cicatrices en el tejido pulmonar. Porque transportan fragmentos de proteínas, lípidos y material genético de sus células de origen, las VE podrían actuar como huellas dactilares de la salud o la enfermedad pulmonar, y quizá llegar a usarse como terapias. El reto es que son extremadamente pequeñas, muy heterogéneas y están presentes en cantidades bajas, lo que dificulta verlas y contarlas con precisión.
Avanzando más allá de pruebas lentas y fragmentadas
Tradicionalmente, los científicos han dependido de varios métodos separados para estudiar las VE. La ultracentrifugación o la cromatografía de exclusión por tamaño se usan para aislarlas; el análisis de seguimiento de nanopartículas mide su movimiento para estimar tamaño y número; y el microscopio electrónico proporciona imágenes detalladas. Aunque potentes, estos enfoques son lentos, laboriosos y no resultan ideales para uso rutinario o clínico. De forma crucial, son poco eficaces a la hora de decir qué proteínas específicas porta cada vesícula. La citometría de flujo —una tecnología usada ampliamente para analizar células sanguíneas e inmunitarias— ofrece una alternativa más ágil. Hace pasar partículas una por una frente a láseres, midiendo su dispersión de luz (relacionada con el tamaño) y la fluorescencia (de colorantes o anticuerpos). Los diseños instrumentales recientes prometen llevar la citometría de flujo hasta la escala de las vesículas más pequeñas, abriendo la posibilidad de que una sola máquina mida tamaño, cuente y caracterice VE en una única corrida.
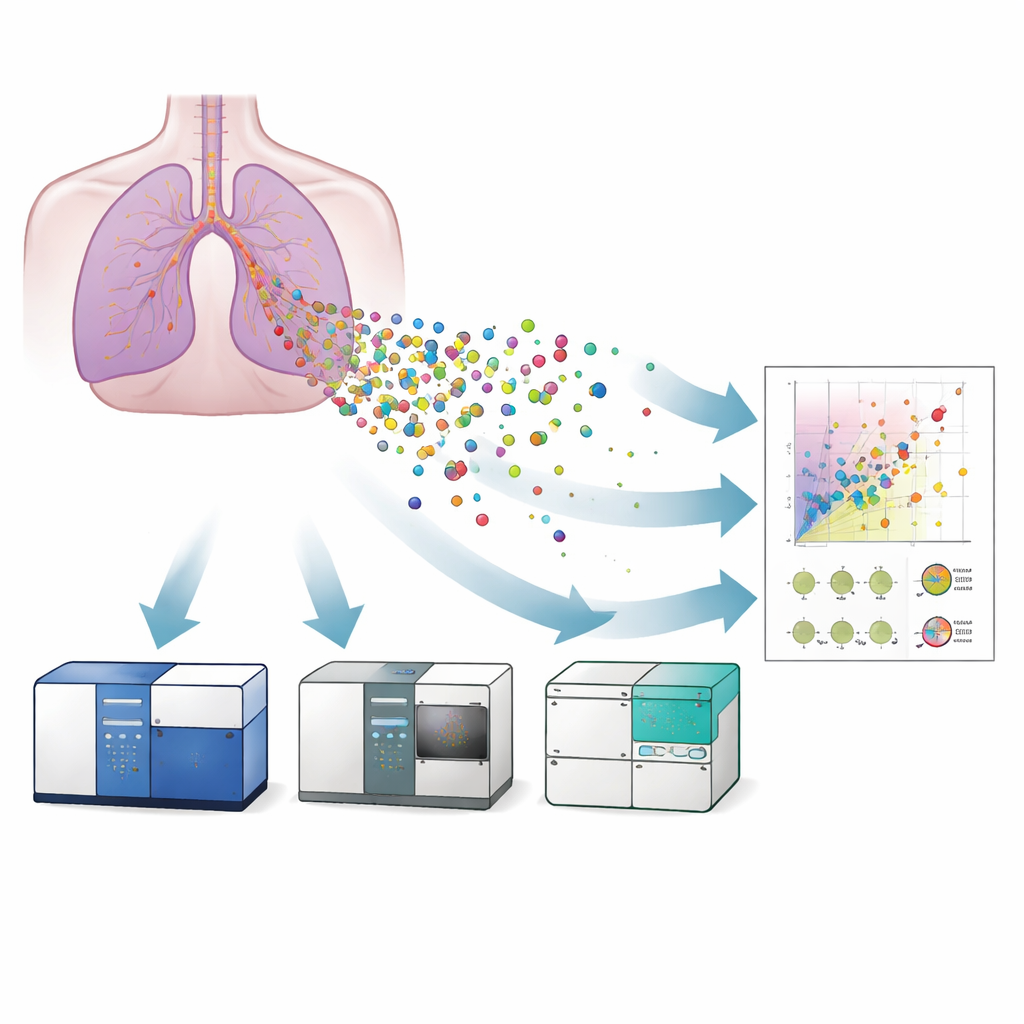
Tres máquinas, un objetivo
Los investigadores compararon tres variantes de citometría de flujo para estudiar las VE liberadas por un modelo cultivado en laboratorio del epitelio bronquial humano: un citómetro de flujo convencional, uno de imagen y otro a escala nanométrica. Primero, confirmaron la presencia y la apariencia típica de las vesículas mediante microscopía electrónica y microscopía de superresolución, que también mostraron que las vesículas portaban proteínas de superficie conocidas como tetraspaninas (CD9, CD63, CD81), marcadores estándar para identificar VE. Luego emplearon perlas de referencia calibradas y estándares de liposomas para traducir las señales de luz de cada instrumento en tamaños aproximados de vesículas. El citómetro de flujo a escala nanométrica pudo detectar vesículas de aproximadamente 40 nanómetros, el instrumento de imagen hasta unos 55 nanómetros, mientras que el equipo convencional tenía dificultades por debajo de aproximadamente 120 nanómetros. Eso implicó que solo los sistemas más sensibles podían capturar plenamente las vesículas más pequeñas y potencialmente más relevantes desde el punto de vista médico.
Etiquetado y recuento de las vesículas
Para asegurarse de que medían vesículas íntegras y biológicamente activas en lugar de desechos, el equipo utilizó un tinte llamado calceína-AM. Este tinte solo se ilumina una vez que atraviesa una membrana intacta y es procesado por enzimas dentro de la vesícula. Ajustaron cuidadosamente la concentración del tinte para que marcara las vesículas con intensidad mientras se minimizaba la señal de fondo, optando por una concentración que produjo respuestas claras y lineales a través de diluciones de las muestras. La calceína se combinó después con anticuerpos fluorescentes que se unen a las tetraspaninas en la superficie de las vesículas, lo que permitió a los instrumentos separar vesículas que portaban distintas combinaciones de estos marcadores. El grupo también midió la sensibilidad de cada máquina a estas etiquetas fluorescentes: cuántas moléculas de anticuerpo debían estar presentes en una vesícula para poder detectarla de forma fiable. La citometría de flujo de imagen generalmente ofreció umbrales de detección más bajos que el citómetro convencional, lo que la hace más adecuada para partículas con solo un pequeño número de proteínas marcadoras.
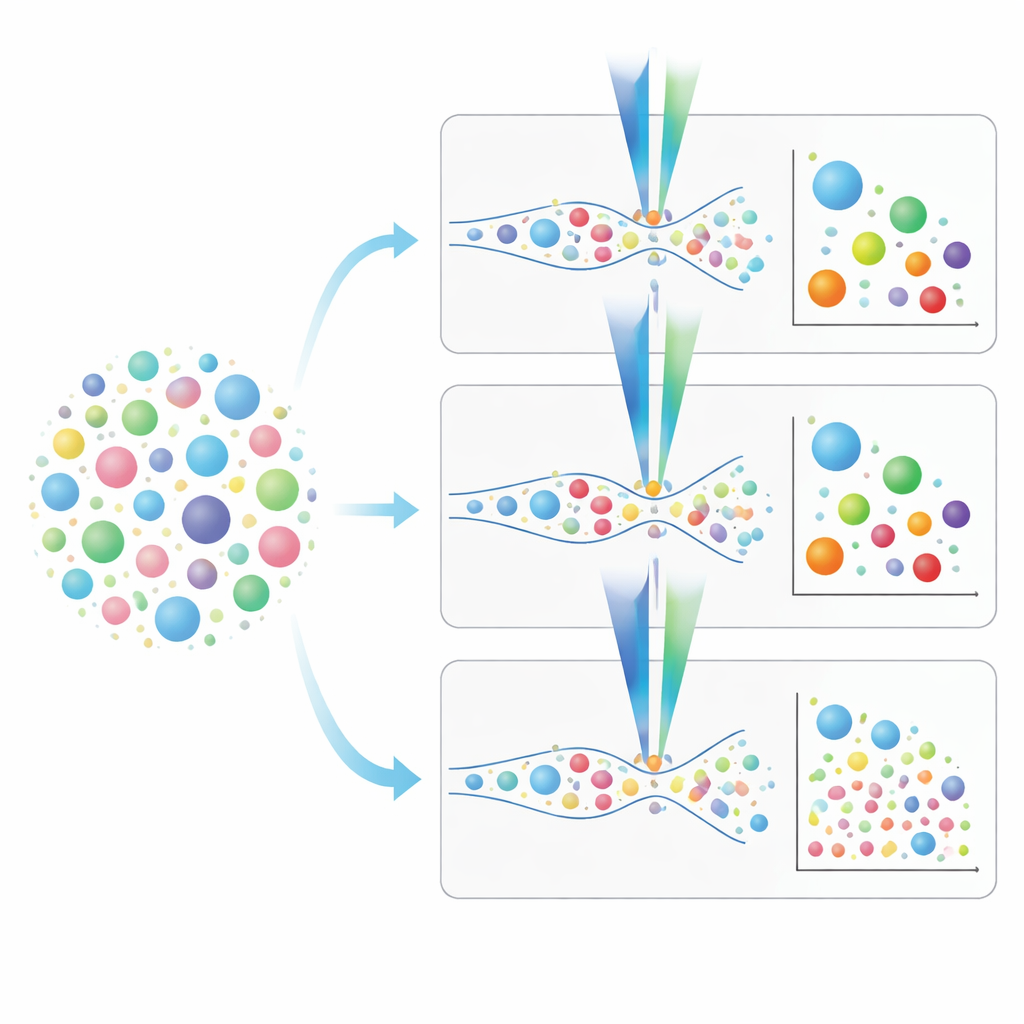
Elegir la herramienta adecuada para estudiar vesículas pulmonares
De esta comparación directa surge una imagen práctica. Los citómetros de flujo convencionales son más rápidos y pueden analizar muestras sin aislamiento previo, pero no detectan muchas de las vesículas más pequeñas que pueden portar señales clave de enfermedad. La citometría de imagen y la de escala nanométrica, aunque más lentas y, en el caso del instrumento nano, más dependientes de una limpieza previa de la muestra, pueden ver tamaños mucho menores y permiten un perfilado más rico de los marcadores de superficie de las vesículas. Los autores describen estrategias paso a paso de tinción y calibración, enfatizan la importancia de conocer el límite de detección de cada etiqueta fluorescente y muestran cómo evitar señales engañosas de colorantes que también marcan fragmentos o partículas no vesiculares. En términos sencillos, ofrecen una hoja de ruta para que los investigadores decidan qué instrumento y protocolo se ajustan mejor a sus preguntas sobre VE pulmonares, acercando al campo a usar estos mensajeros microscópicos como herramientas prácticas para entender, diagnosticar y, eventualmente, tratar las enfermedades respiratorias.
Cita: Hopkins, G., Browne, W., Tucis, D. et al. Bronchial epithelial cell-derived extracellular vesicle analysis using conventional, imaging, and nanoscale flow cytometry technologies. Sci Rep 16, 11162 (2026). https://doi.org/10.1038/s41598-026-41848-x
Palabras clave: vesículas extracelulares, epitelio pulmonar, citometría de flujo, enfermedad respiratoria, análisis de biomarcadores