Clear Sky Science · es
Evaluación cuantitativa ex vivo de la temperatura objetivo y la duración de ablación para la optimización de protocolos de ablación por microondas con termometría por RM
Vigilar los tratamientos tumorales en tiempo real
Cuando los médicos destruyen tumores hepáticos con calor, quieren ver exactamente qué partes del órgano se están eliminando mientras se realiza el procedimiento. La imagen por resonancia magnética (RM) ofrece una manera de “ver la temperatura” dentro del cuerpo a medida que se propaga el calor. Este estudio explora qué tan calientes, y durante cuánto tiempo, los médicos pueden calentar el tejido hepático durante la ablación por microondas sin perder mapas de temperatura claros y fiables por RM —un paso importante hacia tratamientos oncológicos más precisos y menos invasivos.
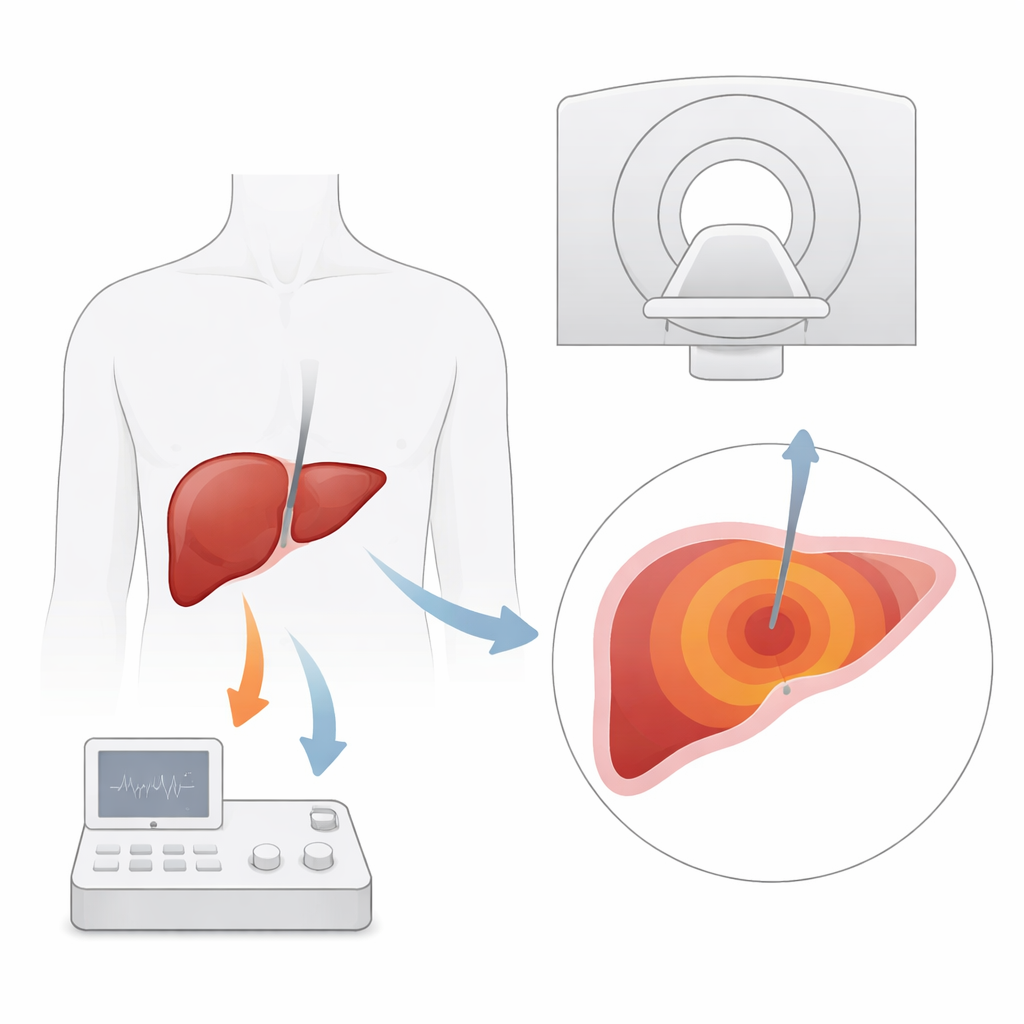
Por qué los tratamientos térmicos del hígado necesitan mejores ojos
La ablación por microondas usa una aguja fina para administrar energía que cocina y destruye el tejido tumoral dentro del hígado. Es especialmente importante para pacientes con cáncer de hígado o metástasis que no pueden someterse a cirugía. Las herramientas de imagen tradicionales, como la ecografía y la tomografía computarizada, guían la colocación de la aguja, pero tienen dificultades para mostrar tumores pequeños con claridad o para seguir hasta dónde se ha difundido el calor durante el tratamiento. La RM destaca porque no solo muestra los tejidos blandos con gran detalle, sino que también puede medir cambios de temperatura usando una propiedad de las moléculas de agua. En teoría, esto permite a los médicos observar un mapa térmico del hígado en tiempo real y asegurarse de que todo el tumor, más un margen de seguridad, quede destruido.
Cuando demasiado calor ciega la vista
En la práctica, los mapas de temperatura por RM pueden volverse poco fiables cuando el tejido alcanza temperaturas muy altas. A temperaturas elevadas, el agua en el tejido hierve, formando pequeñas burbujas de gas que distorsionan el campo magnético. Estas distorsiones aparecen como lecturas de temperatura falsas y formas extrañas en el mapa, lo que dificulta saber dónde termina realmente la zona de ablación. Los investigadores sospecharon que usar temperaturas objetivo algo más bajas podría ofrecer mapas de RM más limpios y de confianza, aunque eso implicara áreas tratadas más pequeñas. Su objetivo fue encontrar combinaciones de temperatura objetivo y tiempo de calentamiento que equilibraran mejor la claridad de la imagen con la destrucción tisular suficiente.
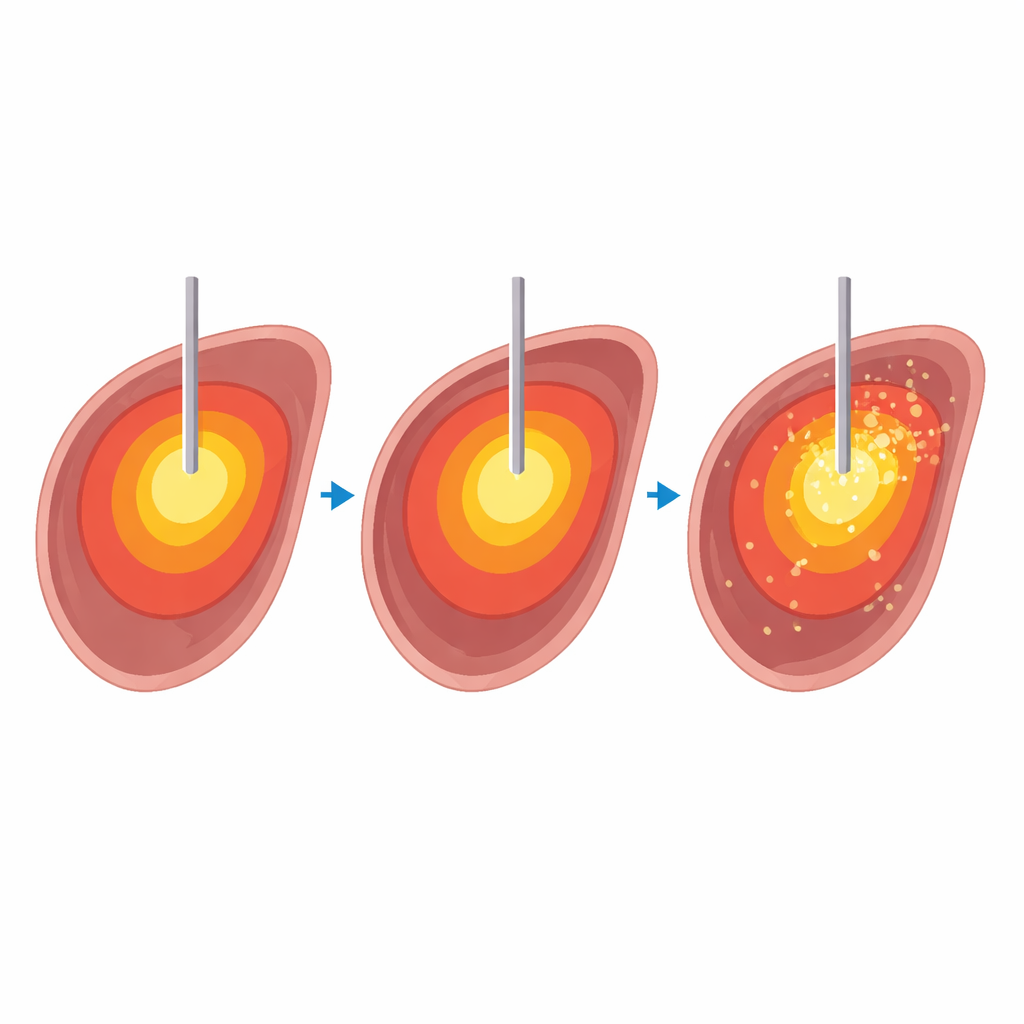
Probar ajustes de calor en hígados de animales donantes
Para investigar esto de forma segura y precisa, el equipo realizó 32 ablaciones por microondas en diez hígados bovinos que se habían extraído poco después del sacrificio. Dentro de un escáner de RM de 1,5 tesla calentaron tejido hepático a cuatro temperaturas objetivo: 60, 80, 100 y 120 grados Celsius, durante cuatro periodos distintos entre 5 y 15 minutos. Durante cada ablación, una secuencia rápida de RM produjo mapas tridimensionales de temperatura y de “dosis térmica” cada pocos segundos. Tras el calentamiento, los hígados se cortaron a lo largo de la trayectoria de la aguja y se midieron las áreas de tejido visible muerto para compararlas con las áreas predichas por los mapas de RM. Dos radiólogos valoraron la calidad de los mapas de RM en una escala de cinco puntos, considerando qué tan redonda y regular aparecía la zona calentada y cuánto interferían los artefactos provocados por el gas y la aguja.
Quemaduras más frías, mapas más claros
Los experimentos mostraron un claro equilibrio. Las temperaturas más altas produjeron zonas de tejido muerto mayores, como cabría esperar, pero los mapas de temperatura por RM se deterioraron de forma notable por encima de los 100 grados. En estos ajustes más calientes, las formas de ablación se volvieron más irregulares y las distorsiones relacionadas con el gas mostraron valores de temperatura aparentemente descendentes o incluso negativos cerca de la aguja. En contraste, a 60 y 80 grados, los mapas de RM eran más suaves, más circulares y mucho mejor ajustados a los tamaños reales de las lesiones observadas en los cortes del tejido. Los análisis estadísticos confirmaron una fuerte concordancia entre las áreas derivadas por RM y la necrosis real a temperaturas más bajas, con correlaciones que se debilitaban o desaparecían a temperaturas mayores. Alargar el tiempo de calentamiento compensó parcialmente las temperaturas más bajas en términos de daño total, pero no pudo igualar por completo las lesiones más grandes observadas a 120 grados.
Una estrategia en dos pasos para una ablación más segura e inteligente
Con base en estos hallazgos, los autores proponen un compromiso práctico para futuros tratamientos guiados por RM. Una primera fase de calentamiento en torno a 80 grados Celsius durante 15 minutos ofreció un buen equilibrio: la calidad de imagen fue alta, la zona de ablación fue razonablemente grande y los estudios tisulares demostraron muerte celular efectiva. Para casos que requieran zonas de tratamiento aún mayores, sugieren un enfoque en dos pasos: empezar con una fase de temperatura más baja para obtener un mapa térmico limpio y verificar la cobertura; luego, una vez que la colocación y los márgenes parezcan satisfactorios, aumentar la temperatura en una segunda fase para ampliar el área destruida, aceptando que el mapa de temperatura será menos fiable durante este impulso final.
Qué significa esto para la atención futura de los pacientes
Para un público no especialista, el mensaje clave es que “bajar un poco la temperatura” puede, en realidad, hacer que los tratamientos oncológicos térmicos sean más seguros y precisos —al menos en condiciones controladas de laboratorio. Las temperaturas objetivo más bajas ofrecieron mapas de temperatura por RM mucho más claros, lo que facilitó ver dónde el tejido había sido realmente destruido. La desventaja es que las quemaduras más frías producen lesiones más pequeñas, por lo que los médicos pueden necesitar tratamientos más largos o de varios pasos para cubrir tumores grandes. Dado que esta investigación se realizó en hígados animales no vivos, sin flujo sanguíneo ni movimiento respiratorio, se necesita trabajo adicional en pacientes. Aun así, el estudio apunta a protocolos de tratamiento que usan la RM no solo para dirigir la aguja, sino para observar y ajustar la ablación en tiempo real, lo que podría mejorar los resultados en personas con tumores hepáticos.
Cita: Nardone, L., Tan, A.S.M., Bour, P. et al. Quantitative ex vivo assessment of target temperature and ablation duration for protocol optimization of microwave ablation procedures with mr thermometry. Sci Rep 16, 8153 (2026). https://doi.org/10.1038/s41598-026-41656-3
Palabras clave: ablación por microondas, termometría por RM, cáncer de hígado, ablación térmica, terapia guiada por imagen