Clear Sky Science · es
Síntesis y caracterización de nanopartículas de CuFe2O4 dopadas con Mg para posibles aplicaciones anticancerígenas
Por qué los imanes diminutos podrían importar en el cáncer
Los tratamientos contra el cáncer, como la quimioterapia y la radiación, pueden dañar tanto el tejido sano como los tumores. Los científicos buscan terapias más inteligentes que afecten con más intensidad a las células cancerosas que a las normales. Este estudio explora partículas magnéticas ultrapequeñas hechas de hierro, cobre y magnesio, diseñadas para dirigirse a las células cancerosas y activar sus programas de autodestrucción desde el interior. El trabajo sugiere que ajustar cuidadosamente la composición y el tamaño de estas partículas puede hacerlas especialmente letales para las células tumorales al tiempo que preservan las sanas.
Construyendo partículas metálicas inteligentes
Los investigadores crearon una familia de “nanoferritas”: pequeños cristales que contienen hierro, al combinar cobre y magnesio en diferentes proporciones con hierro y oxígeno. Estas partículas, de solo unos 17–30 milmillonésimos de metro de diámetro, son lo bastante pequeñas como para penetrar en las células. El equipo usó varios microscopios avanzados y técnicas de rayos X para confirmar que las partículas tenían la estructura cristalina adecuada, eran químicamente puras y formaban agrupaciones aproximadamente esféricas. Descubrieron que la versión con metales mezclados y cantidades iguales de cobre y magnesio producía las partículas más pequeñas, lo que aumenta el área superficial y tiende a potenciar su reactividad química.
Poniendo las partículas a prueba en células cancerosas
Luego probaron la toxicidad de cada tipo de partícula en células humanas cancerosas cultivadas en el laboratorio, incluidas células de próstata (PC‑3), colon (Caco‑2), mama (MCF‑7) e hígado (HepG‑2), junto con células intestinales normales como comprobación de seguridad. Las tres formulaciones dañaron las células cancerosas de forma dependiente de la dosis, aunque no por igual. Las partículas mixtas de cobre y magnesio fueron las más potentes en general, particularmente frente a las células de próstata y colon, donde eliminaron la mitad de las células a dosis relativamente bajas. Es importante que las células normales toleraran dosis más altas, lo que sugiere un grado de selectividad crucial para cualquier terapia futura.
Forzando a las células cancerosas a la autodestrucción controlada
Para entender cómo matan las nanopartículas, los investigadores examinaron la apoptosis, la forma ordenada de muerte celular en la que las células dañadas se desmantelan a sí mismas en lugar de reventar. Mediante citometría de flujo, mostraron que las células de próstata y colon tratadas pasaron claramente de un estado sano a etapas tempranas y tardías de apoptosis. De nuevo, las partículas mixtas de cobre y magnesio tuvieron el efecto más intenso, elevando la apoptosis total a niveles muchas veces superiores a los de las células no tratadas. También hubo un aumento moderado de la necrosis, una forma más caótica de muerte celular, lo que indica que pueden activarse múltiples vías de daño.
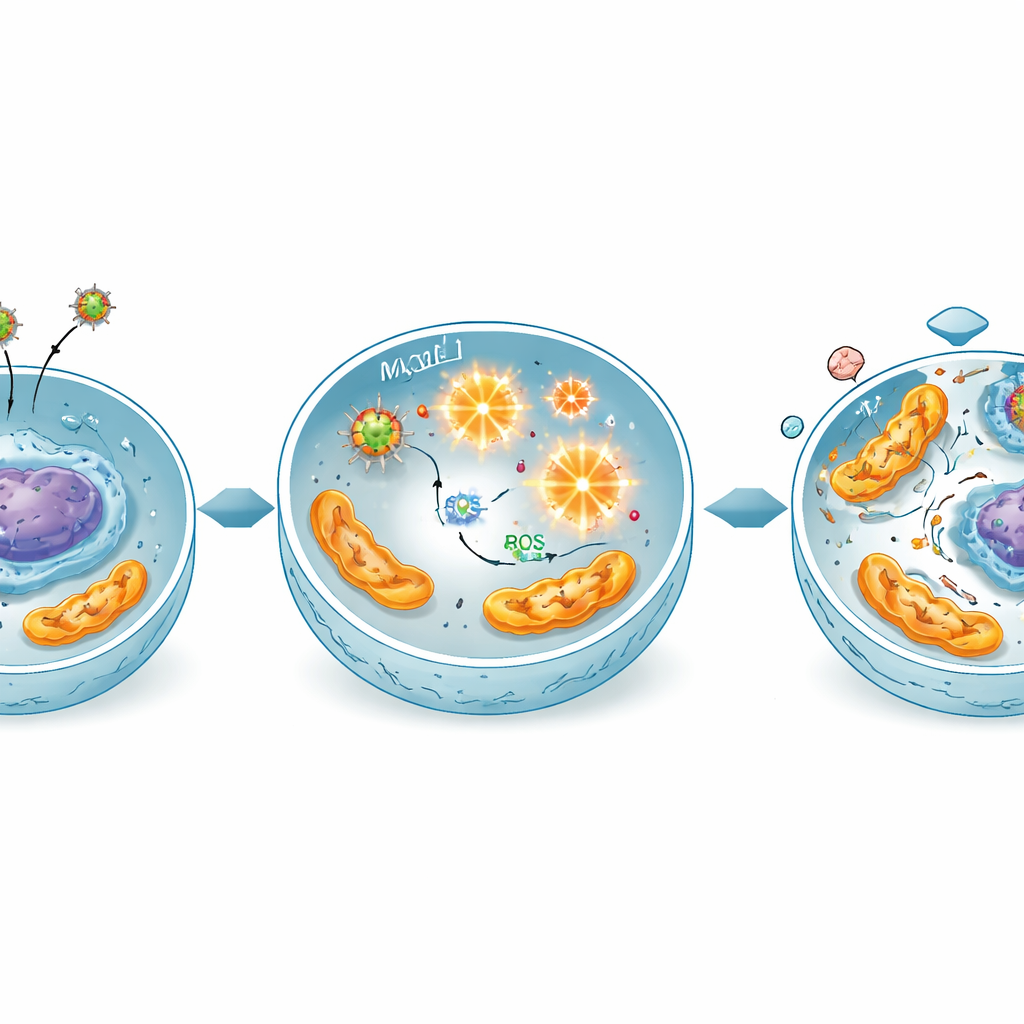
Sobrecargar a las células cancerosas con química oxidativa dañina
El estudio apunta a una reacción en cadena química en el núcleo de este efecto. Estas partículas a base de hierro pueden actuar como pequeños catalizadores, convirtiendo el peróxido de hidrógeno natural dentro de las células en formas de oxígeno altamente reactivas. Las mediciones mostraron que las células cancerosas tratadas produjeron mucho más de estas especies reactivas de oxígeno, especialmente cuando se expusieron a las partículas mixtas de cobre y magnesio. Esta oleada oxidativa daña componentes celulares, en particular las mitocondrias productoras de energía y el ADN. Las pruebas de expresión génica confirmaron que genes clave «guardianes» y «ejecutores» vinculados al suicidio celular se activaron, mientras que genes de supervivencia y del ciclo celular se reprimieron, coincidiendo con un panorama de apoptosis dependiente de mitocondrias inducida por estrés.
Qué podría significar esto para la atención futura del cáncer
En conjunto, el trabajo muestra que, eligiendo con cuidado los metales y ajustando el tamaño y la estructura de las nanoferritas, es posible crear partículas que impulsen con fuerza a las células cancerosas hacia la autodestrucción mientras son más benignas con las células normales. La versión con partes iguales de cobre y magnesio destacó como la más efectiva, probablemente porque su pequeño tamaño y química de metales mixtos mejoran su capacidad para entrar en las células y generar oxígeno reactivo. Aunque estos resultados se limitan todavía a cultivos celulares y están lejos de un uso clínico, resaltan una vía prometedora hacia tratamientos contra el cáncer más precisos basados en nanotecnología que se apoyan en activar los propios mecanismos de muerte del tumor en lugar de inundar el organismo con fármacos de amplia toxicidad.
Cita: Ali, M., Zein, N., Abdo, M.A. et al. Synthesis, characterization of Mg doped CuFe2O4 nanoparticles for potential anticancer applications. Sci Rep 16, 8276 (2026). https://doi.org/10.1038/s41598-026-41540-0
Palabras clave: nanopartículas, terapia del cáncer, especies reactivas de oxígeno, apoptosis, ferritas