Clear Sky Science · es
Efectos antagónicos de los aminoácidos que sostienen nanoambientes abióticos en arcilla
Cómo los diminutos huecos en la arcilla podrían nutrir la primera química de la vida
La vida podría no haber comenzado en mares abiertos, sino dentro de espacios inimaginablemente pequeños entre las capas de minerales comunes de arcilla. Este estudio explora cómo moléculas sencillas relacionadas con los aminoácidos actuales pueden reorganizar la arcilla a escala nanométrica, esculpiendo compartimentos acogedores que atrapan y ordenan la química. Al mostrar cómo distintos aminoácidos fortalecen o desestabilizan las láminas de arcilla, el trabajo sugiere una manera natural por la que la Tierra primitiva —o otros mundos rocosos— podría haber creado pequeños “laboratorios” donde los bloques de construcción de la vida podían ensamblarse.
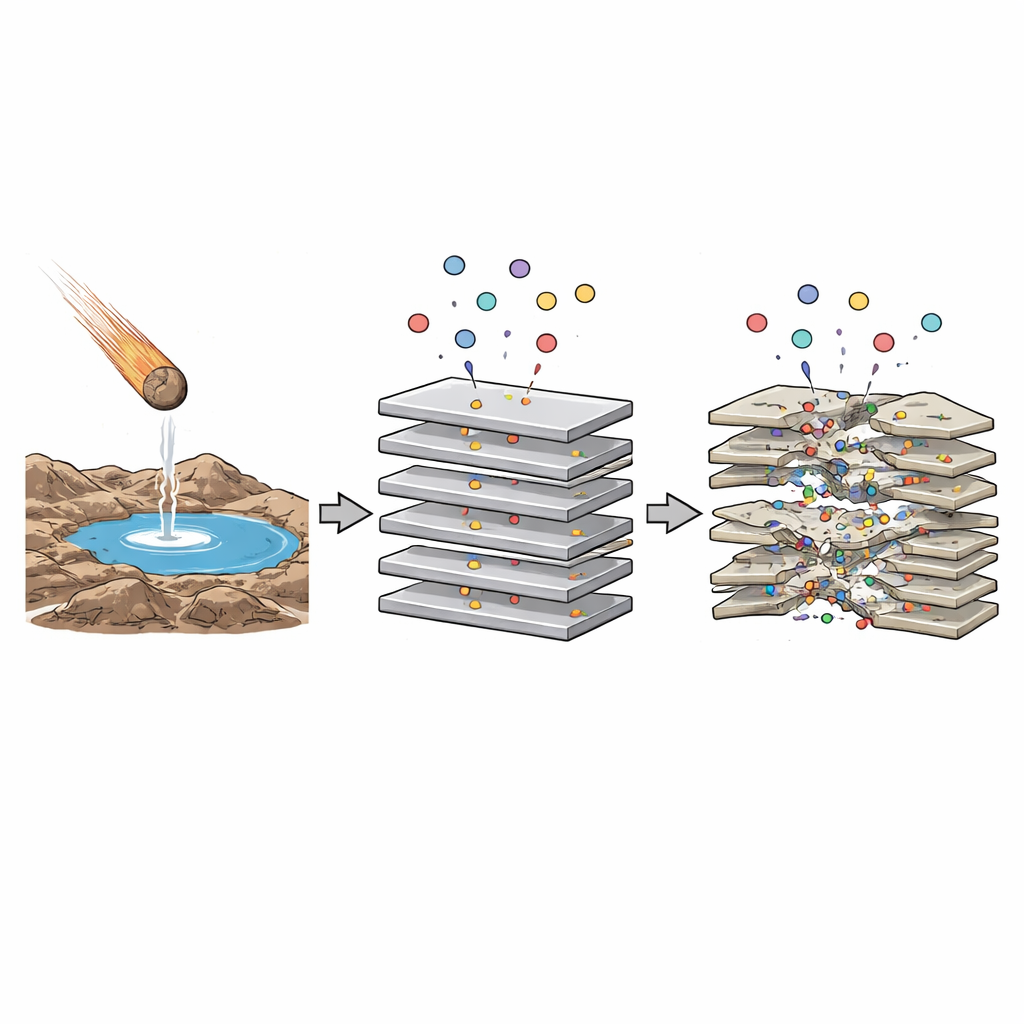
La promesa de los espacios ocultos
Los científicos han sospechado durante mucho tiempo que los minerales hicieron más que yacer bajo los océanos y estanques primitivos: podrían haber ayudado a ensamblar las primeras cadenas moleculares. En particular, arcillas como la montmorillonita pueden hincharse y contraerse cuando el agua y pequeñas moléculas se deslizan entre sus láminas apiladas. Dentro de estas brechas estrechas, el agua se comporta de manera diferente, las fuerzas eléctricas son más intensas y reacciones difíciles en agua ordinaria pueden volverse más fáciles. Esos espacios confinados podrían ayudar a unir bloques sencillos —como aminoácidos y nucleótidos— en cadenas más largas, un paso clave hacia la vida. Pero los ambientes prebióticos reales eran caldos químicos con muchos compuestos orgánicos presentes a la vez. Esto plantea una pregunta: cuando varios tipos de aminoácidos interactúan con la arcilla simultáneamente, ¿se anulan entre sí o sus efectos opuestos pueden en realidad crear entornos más ricos para la química?
Constructores amigables y perturbadores traviesos
Los investigadores se centraron en una forma de montmorillonita rica en calcio y en tres aminoácidos. Dos, lisina y arginina, son aminoácidos habituales en las proteínas que aparecen en los libros de biología. El tercero, el ácido gamma-aminobutírico (GABA), no se usa en proteínas modernas pero es común en meteoritos y por tanto es probable que llegara a la Tierra primitiva. Trabajos previos mostraron que lisina y arginina se alojan entre las capas de la arcilla y se unen firmemente, ayudando a mantener las láminas ordenadas y relativamente planas. GABA, en cambio, se adhiere apenas—sin embargo tiene un efecto desproporcionado: dobla y despega parcialmente las láminas de arcilla, creando cavidades a escala nanométrica. Este estudio preguntó qué ocurre cuando una pequeña cantidad de aminoácido tipo proteico se mezcla con un gran exceso de GABA parecido al de meteoritos, imitando un estanque fuertemente abonado con compuestos orgánicos extraterrestres.
Observando la transformación de las capas de arcilla
Para seguir estos cambios, el equipo combinó varias técnicas que revelan cada una un aspecto diferente de la arcilla. La espectroscopía infrarroja sondeó cómo vibran las partes silicio–oxígeno del armazón de la arcilla, que varían cuando las capas se distorsionan, separan o se llenan con distintas especies. La difracción de rayos X midió el espaciado y el orden de las láminas apiladas, tanto en muestras secas como tras rehidratación con vapor de agua. El análisis termogravimétrico vigiló con qué fuerza se retenían las moléculas orgánicas y el agua en la arcilla. Finalmente, la microscopía electrónica de alta resolución proporcionó imágenes directas de las estructuras por capas y de las diminutas cavidades entre ellas. En conjunto, estas herramientas permitieron a los autores separar las acciones estabilizadoras de la lisina y la arginina de la influencia disruptiva del GABA, incluso cuando todos estaban presentes en la misma mezcla.
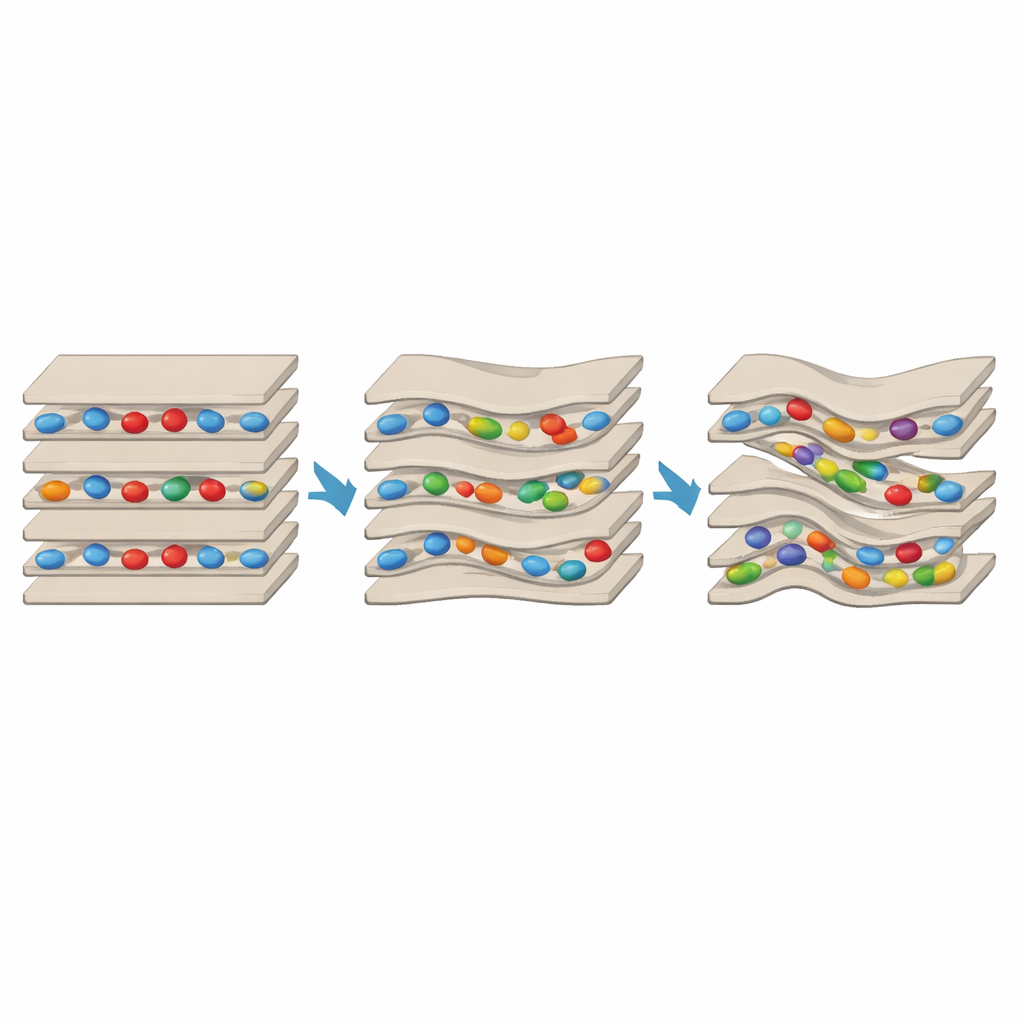
Un yin–yang a nanoescala en la arcilla
Los resultados revelan un marcado empuje y tirón. Cuando solo estaban presentes lisina o arginina, se intercalaban en los espacios entre capas, actuando como travesaños que unen una lámina con la siguiente. Esto reducía la capacidad de la arcilla para hincharse con agua y hacía la estructura más ordenada y resistente al desprendimiento. Pero cuando se añadió GABA en gran exceso, éste superó ese efecto estabilizador en muchas regiones. Las señales espectroscópicas mostraron la presencia de dominios parcialmente exfoliados, y los patrones de rayos X indicaron mayor desorden y una alineación reducida de las láminas. La microscopía electrónica fue más allá, revelando pilas altamente distorsionadas con cavidades claras incrustadas a mitad de capa —pequeños huecos de un par de nanómetros que no aparecían en los controles ni en las muestras con solo aminoácidos proteicos. Es importante: regiones con láminas puentes y fuertemente unidas coexistían junto a regiones con capas distorsionadas y ricas en cavidades dentro del mismo grano de arcilla, demostrando que ambos efectos pueden operar lado a lado.
Nano-compartimentos naturales para la química primitiva
Para un público no especializado, el mensaje clave es que mezclas simples de aminoácidos pueden esculpir la arcilla en un mosaico de diminutos compartimentos con propiedades distintas. Los aminoácidos que forman proteínas ayudan a mantener unidas las capas, mientras que el GABA de origen meteórico las separa sutilmente y talla nanocavidades. Estos bolsillos confinados probablemente alojan agua y moléculas disueltas en condiciones distintas del entorno circundante, favoreciendo potencialmente reacciones como la formación de polímeros que son centrales para el origen de la vida. Dado que los meteoritos entregan abundantes aminoácidos no proteicos a mundos ricos en arcilla, este antagonismo “yin–yang” entre moléculas estabilizadoras y disruptivas puede ser una vía común por la que planetas rocosos y asteroides generan y sostienen diversos nanoambientes donde la bioquímica primitiva podría comenzar.
Cita: Bezaly, O.R., King, H.E. & Petrignani, A. Antagonistic effects of amino acids support abiotic nano-environments in clay. Sci Rep 16, 8959 (2026). https://doi.org/10.1038/s41598-026-41502-6
Palabras clave: orígenes de la vida, química prebiótica, minerales de arcilla, aminoácidos, nanoconfinamiento