Clear Sky Science · es
DUSP29 no regula las interacciones melanoma–mioblasto en un modelo de co‑cultivo de músculo esquelético
Por qué importa la resistencia del músculo a la diseminación del cáncer
Cuando el cáncer se disemina por el cuerpo, a menudo se instala en lugares como los pulmones, el hígado o los huesos. Curiosamente, nuestros músculos esqueléticos —que en conjunto representan cerca de la mitad del peso corporal— rara vez albergan estos depósitos peligrosos. Este enigma ha intrigado a médicos y científicos durante más de un siglo. El estudio resumido aquí plantea una pregunta concreta dentro de ese rompecabezas mayor: ¿las propias células musculares, y una proteína enriquecida en músculo llamada DUSP29, frenan directamente a las células cancerosas, o la protección del músculo se debe a algo completamente distinto?
Un lugar poco habitual para células cancerosas errantes
Los médicos observan muchas menos metástasis en el músculo esquelético que en muchos otros órganos, incluso en personas cuyo cáncer se ha diseminado ampliamente. Una hipótesis es que las células musculares crean un vecindario hostil para las células tumorales entrantes, quizá enviando señales químicas o forzando a las células cancerosas a cambiar su comportamiento. Trabajos previos en ratones sugirieron que cuando células de cáncer de piel (melanoma) crecen junto a células musculares inmaduras, pierden algo de pigmento e incluso empiezan a parecer músculo. Partiendo de esto, los autores se centraron en una proteína específica, DUSP29, que se encuentra a niveles mucho más altos en el músculo que en otros tejidos y forma parte de una familia de enzimas conocida por controlar vías de crecimiento y supervivencia que los cánceres frecuentemente secuestran.
Probando los encuentros músculo–tumor en placa
Para explorar estas ideas, los investigadores construyeron un modelo de laboratorio controlado usando dos líneas celulares de ratón bien estudiadas: células de melanoma (B16F10) y precursoras musculares, o mioblastos (C2C12). Mezclaron estos dos tipos celulares en placas compartidas en diferentes proporciones, desde números iguales hasta situaciones en las que los mioblastos superaban ampliamente a las células tumorales. En algunos experimentos las células estuvieron en contacto directo; en otros, las células de melanoma solo estuvieron bañadas en el medio de cultivo líquido tomado de cultivos de mioblastos, capturando así factores solubles liberados por las células musculares. Durante varios días, el equipo midió cuántas células estaban vivas y en división mediante una prueba colorimétrica estándar, y comprobaron signos de muerte celular programada mediante citometría de flujo, una técnica que puede distinguir células vivas, moribundas y muertas.
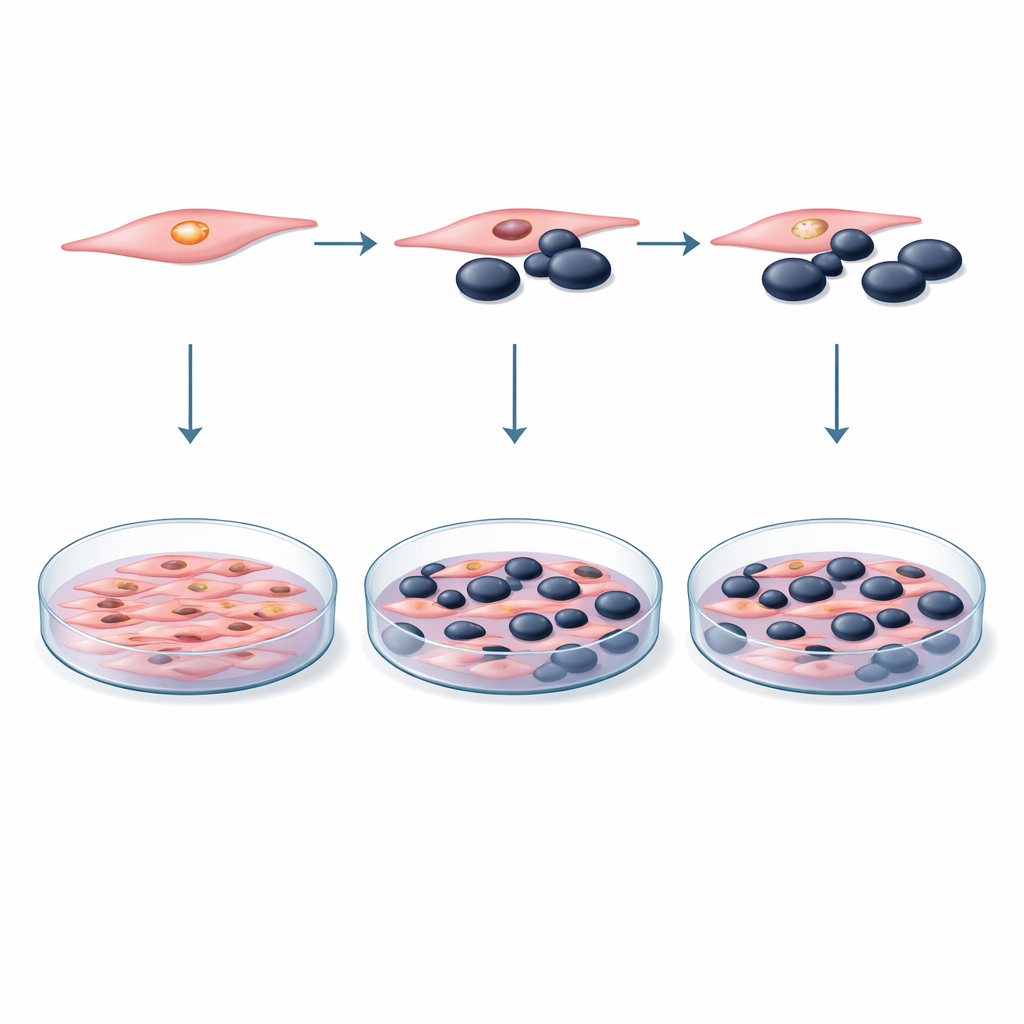
Poniendo a DUSP29 bajo el microscopio
El segundo eje del estudio se centró en DUSP29 en sí. Primero, los científicos confirmaron que los mioblastos producen el mensaje genético de esta proteína en niveles apreciables. Luego usaron ARN interferente pequeño (siRNA), fragmentos genéticos cortos que actúan como "interruptores" dirigidos, para reducir drásticamente los niveles de DUSP29 en las células musculares. Controles cuidadosos mostraron que los reactivos de entrega y los siRNA de control no dañaban las células por sí mismos. Con DUSP29 reducido, los mioblastos modificados volvieron a cultivarse junto con células de melanoma, o su medio de crecimiento se aplicó a cultivos de melanoma. Se repitieron las mismas pruebas de supervivencia y muerte celular en múltiples puntos temporales para ver si silenciar esta proteína enriquecida en músculo inclinaría la balanza a favor o en contra de las células tumorales.
Cuando no ocurre nada, ese es el resultado importante
En todos estos experimentos, el resultado fue llamativo precisamente por la falta de efectos. Tanto si las células de melanoma se cultivaban solas como junto a mioblastos, con o sin contacto directo, su supervivencia permaneció esencialmente sin cambios dentro de la variación experimental normal. El co‑cultivo no desencadenó muerte celular adicional en las células de melanoma, ni impulsó su crecimiento. La reducción de DUSP29 en los mioblastos tampoco alteró la viabilidad de las células de melanoma, a pesar de que la actividad del gen en las células musculares se redujo claramente. En otras palabras, bajo estas condiciones simplificadas a corto plazo, ni los vecinos mioblásticos ni la presencia o ausencia de DUSP29 dirigieron de forma mensurable a las células de melanoma hacia la supervivencia o la destrucción.
Qué significa esto para el misterio músculo–cáncer
Los hallazgos sugieren que la relativa protección del músculo esquelético frente a la metástasis probablemente no proviene de una conversación directa y sencilla entre células de melanoma y mioblastos cercanos, ni de DUSP29 actuando de forma aislada en esta interacción temprana. En cambio, la resistencia del músculo probablemente emerge de una mezcla más compleja de características: su estructura densa, las fuerzas mecánicas de la contracción, su bioquímica metabólica singular y una serie de otras moléculas señalizadoras que no quedan capturadas en este sistema basado en placas. Al mostrar de forma clara dónde no opera un mecanismo plausible, este trabajo ayuda a acotar la búsqueda de cómo el músculo mantiene a raya a la mayor parte del cáncer metastásico y orienta estudios futuros hacia modelos tisulares más realistas, otros tipos tumorales y el entorno más amplio en el que se encuentran las células musculares y cancerosas.
Cita: Ön, S., İlhan, H.A., Günenç, D. et al. DUSP29 does not regulate melanoma–myoblast interactions in a skeletal muscle co-culture model. Sci Rep 16, 8372 (2026). https://doi.org/10.1038/s41598-026-41300-0
Palabras clave: metástasis en músculo esquelético, melanoma, interacciones tumor–músculo, DUSP29, microambiente tumoral