Clear Sky Science · es
Clasificación pan‑cáncer de cortes congelados usando un transformador visual con mezcla suave de expertos bajo supervisión débil
Por qué importa en el quirófano
Cuando los cirujanos extirpan un tumor sospechoso, muchas veces disponen de solo unos minutos para saber si se ha eliminado todo el cáncer. Los patólogos se apresuran a examinar una lámina de tejido rápidamente congelada y dan una respuesta mientras el paciente aún está en la mesa. Este proceso de alta presión puede verse afectado por preparaciones borrosas, tumores sutiles y, simplemente, el límite de tiempo. El estudio descrito aquí explora cómo un sistema de inteligencia artificial (IA) puede ayudar a los patólogos a distinguir de forma rápida y fiable entre tejido inocuo y peligroso en múltiples órganos, utilizando equipamiento realista para hospitales cotidianos.
Una prueba rápida con desafíos inherentes
El análisis de cortes congelados es un pilar de la cirugía moderna: se congela una delgada porción de tejido, se corta, tiñe y observa al microscopio para juzgar si es benigno o maligno y si el margen quirúrgico está limpio. A diferencia de las láminas permanentes de laboratorio, los cortes congelados suelen presentar grietas, pliegues y tinción desigual. Diferentes patólogos pueden discrepar en casos marginales, y el reloj siempre avanza. Estos problemas son especialmente graves en hospitales pequeños o muy concurridos, donde solo unos pocos especialistas deben atender muchos tipos de cáncer. Los autores sostienen que un asistente informático robusto podría hacer que las decisiones sobre cortes congelados sean más consistentes, rápidas y accesibles.
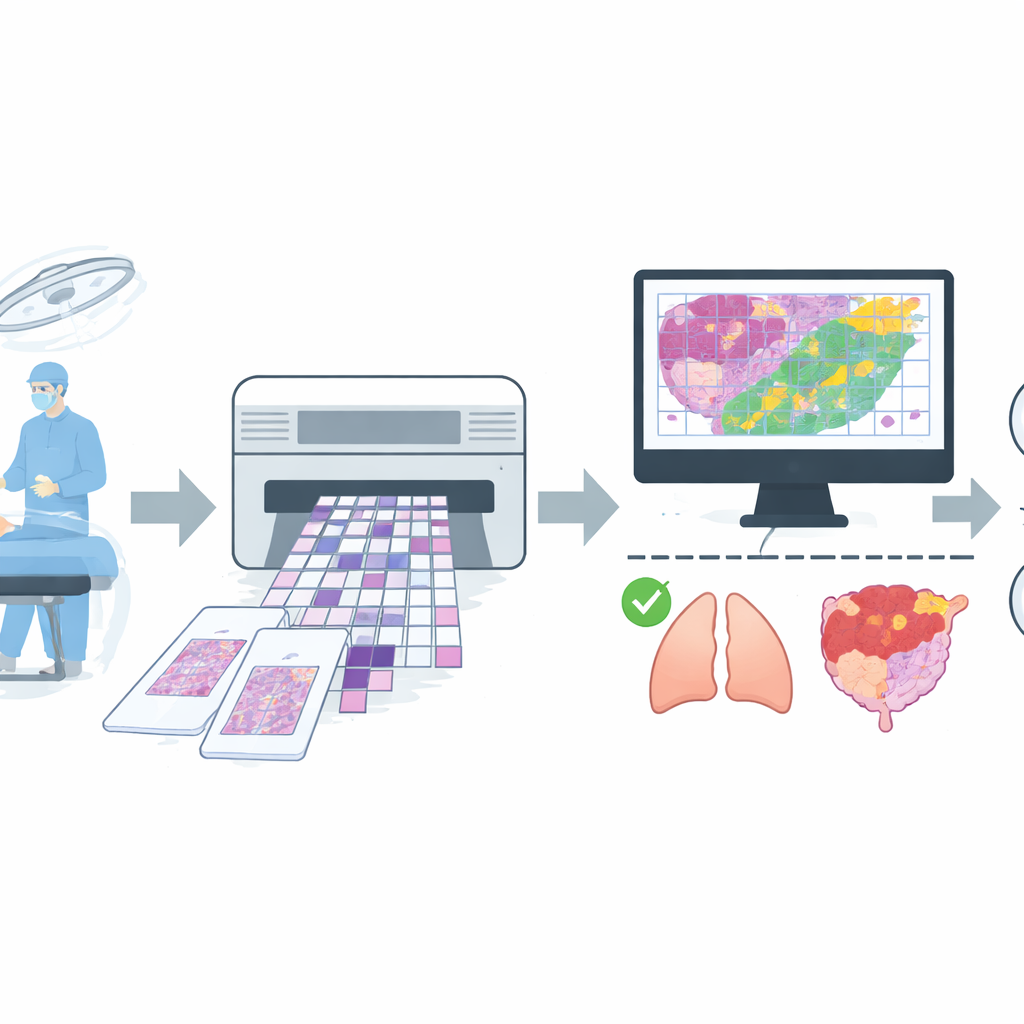
Construyendo un conjunto de imágenes amplio y realista
Para entrenar dicho asistente, el equipo reunió una gran colección de imágenes digitales obtenidas en operaciones rutinarias en un hospital importante. Reunieron 4.754 imágenes de portaobjetos completos de cortes congelados procedentes de más de 2.600 pacientes, y aplicaron normas estrictas de calidad para eliminar láminas con artefactos severos o diagnósticos inciertos. El conjunto final contenía 4.667 láminas, cada una etiquetada simplemente como benigna o maligna según el acuerdo entre la lectura rápida del corte congelado y el posterior informe más cuidadoso de la sección permanente. Las láminas cubrieron sitios comunes como pulmón, mama, tiroides, ganglios linfáticos y órganos reproductores femeninos, además de un grupo mixto de ubicaciones menos frecuentes como estómago, hígado y piel. Los datos se dividieron en grupos separados para entrenamiento, afinado y prueba final, cuidando que imágenes del mismo paciente nunca aparecieran en más de un grupo.
Cómo aprende la IA a partir de pistas débiles
Los investigadores construyeron su modelo sobre una clase de red neuronal llamada Vision Transformer, que destaca por encontrar patrones en imágenes de gran tamaño. Cada imagen tisular gigante se fragmentó automáticamente en muchos azulejos y parches más pequeños para poder procesarla en hardware gráfico estándar. Una innovación clave fue reemplazar parte de la red por una “mezcla suave de expertos”, un conjunto de muchas ramas especialistas pequeñas que se centran en distintos patrones visuales. En lugar de activar o desactivar expertos, el sistema mezcla sus contribuciones de forma continua, lo que estabiliza el entrenamiento y aprovecha mejor los datos limitados. Dado que los patólogos no delinearon los contornos de los tumores, el modelo tuvo que aprender con supervisión débil: solo sabía si una lámina completa era benigna o maligna. Una estrategia de aprendizaje por instancias múltiples promovió los parches más sospechosos dentro de una lámina maligna para que sirvieran como ejemplos positivos, permitiendo que la red se centrara gradualmente en las regiones más informativas.
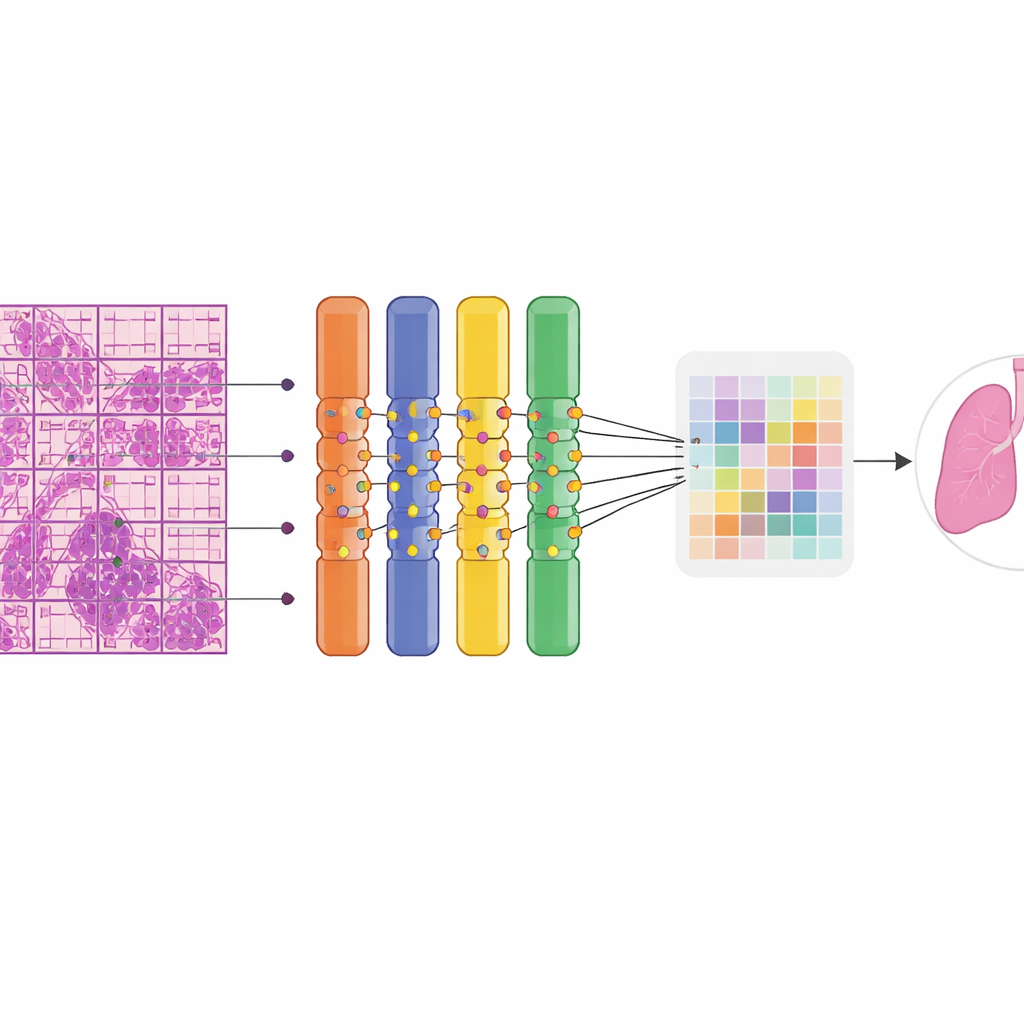
Qué tan bien funciona el sistema en la práctica
Al probarse en 669 láminas no vistas, la IA distinguió tejido benigno de maligno con alta precisión. Clasificó correctamente alrededor del 90% de los casos en conjunto y mostró una excelente capacidad para separar los dos grupos a través de umbrales de probabilidad. La sensibilidad, la probabilidad de señalar una lámina verdaderamente maligna, fue de alrededor de cuatro de cada cinco, mientras que la especificidad, la probabilidad de declarar con seguridad una lámina benigna como benigna, fue aún mayor. Es importante que el rendimiento se mantuvo sólido entre órganos: detectó perfectamente todos los casos malignos de pulmón y mama en el conjunto de prueba y rindió bien en grupos más raros como tumores anexiales femeninos y órganos “otros” mixtos. Mapas de calor en color superpuestos a las láminas revelaron que la atención del modelo se concentraba en regiones que los patólogos expertos reconocieron como tumor, incluidos focos metastásicos en ganglios linfáticos, mientras que en gran medida ignoraba estructuras normales. El sistema funcionó de forma eficiente, necesitando menos de 5 GB de memoria, lo que lo hace adecuado para usarse en tarjetas gráficas habitualmente disponibles en lugar de en clústeres costosos.
Límites, tropiezos y margen de mejora
Los autores también examinaron dónde falló la IA. Los falsos negativos a menudo involucraron células cancerosas extremadamente escasas, zonas de escaneo borrosas o inflamación intensa que ocultaba nidos malignos. Los falsos positivos tendieron a surgir en condiciones benignas que imitan el cáncer al microscopio, como proliferaciones reactivas o tejido congelado distorsionado. Debido a que los flujos de trabajo quirúrgicos rutinarios no incluyen contornos detallados de las regiones tumorales, el equipo no pudo cuantificar exactamente cuánto coincidían los mapas de calor con las marcas de los expertos, y se tuvo que confiar en evaluaciones cualitativas. Algunos tipos de órgano, como la lengua o ciertos tumores de tejido blando, siguieron estando poco representados, lo que sugiere que harán falta colecciones mayores y multicéntricas para ampliar el alcance del sistema.
Qué podría significar esto para pacientes y hospitales
En conjunto, el estudio demuestra que un sistema de IA cuidadosamente diseñado puede asistir de forma precisa e interpretable en una tarea central de la patología quirúrgica: decidir, en tiempo real, si un tejido es benigno o maligno en múltiples tipos de órgano. Al operar solo con etiquetas a nivel de lámina, funcionar en hardware ampliamente disponible y resaltar áreas sospechosas para revisión humana, el modelo ofrece una vía práctica hacia decisiones de cortes congelados más consistentes. Para los pacientes, esto podría traducirse en cirugías mejor informadas en una sola intervención; para los hospitales, especialmente aquellos con escasez de especialistas, apunta a un futuro en el que herramientas digitales avanzadas contribuyan a ofrecer atención oncológica de alta calidad de forma más equitativa.
Cita: Wu, J., Yang, M., Li, J. et al. Pan-cancer frozen section classification using a soft mixture of experts vision transformer under weak supervision. Sci Rep 16, 10297 (2026). https://doi.org/10.1038/s41598-026-40924-6
Palabras clave: corte congelado, patología digital, diagnóstico del cáncer, vision transformer, aprendizaje débilmente supervisado