Clear Sky Science · es
IA explicable para la vigilancia de lesiones gastrointestinales y la administración de fármacos de precisión
Exploraciones más inteligentes, tratamientos más seguros
Muchas personas temen los fármacos contra el cáncer por sus efectos secundarios agresivos. Esta investigación explora un futuro en el que diminutas cámaras ingeribles, algoritmos inteligentes y portadores microscópicos de fármacos trabajan juntos para que los medicamentos potentes se liberen solo donde realmente se necesitan. Al cerrar el ciclo entre detectar un problema en el intestino y tratarlo in situ, los autores pretenden que la atención gastrointestinal sea más precisa, menos invasiva y mucho más segura.
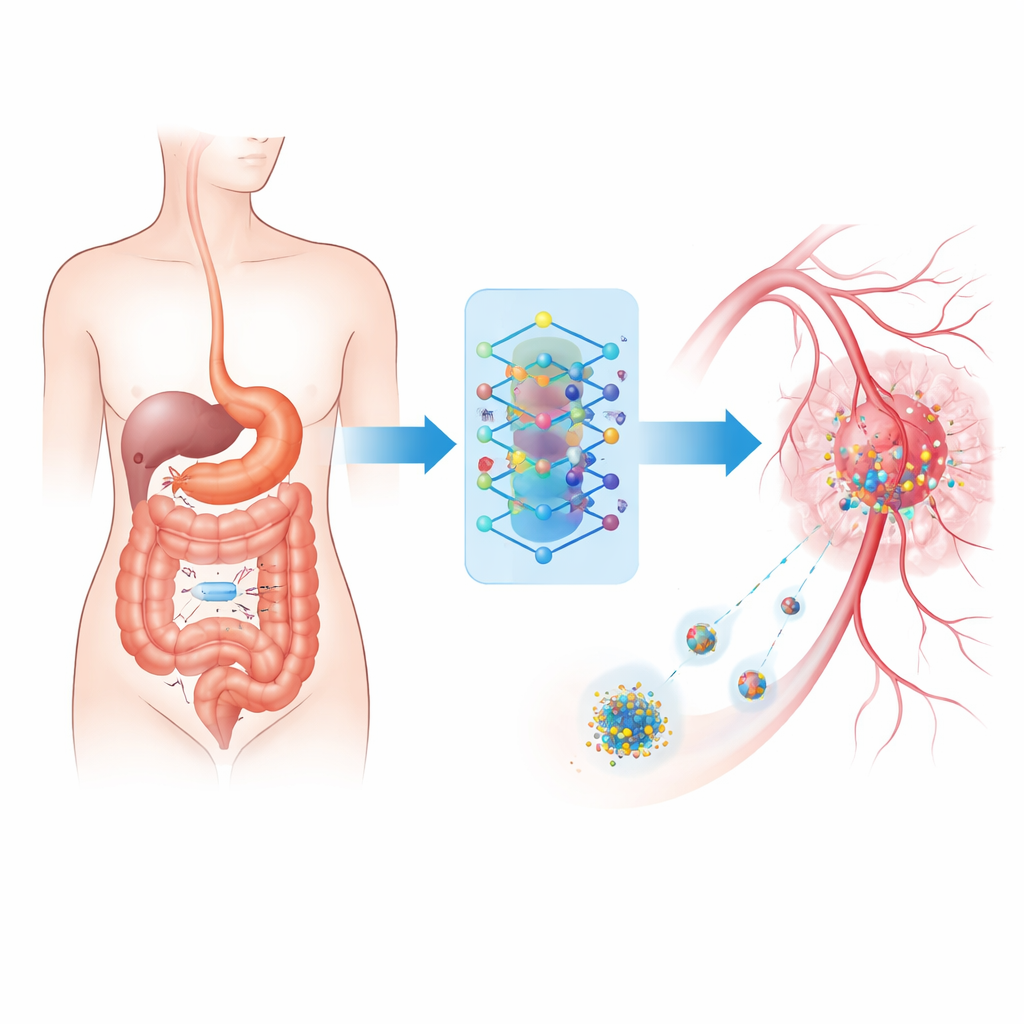
Una pequeña cámara en viaje
En el centro del sistema está un dispositivo de imagen inalámbrico ingerible: una cápsula del tamaño de una vitamina que recorre de forma natural el tracto digestivo mientras toma decenas de miles de fotografías. En lugar de depender únicamente de que un médico revise ese aluvión de imágenes, la cápsula las envía a una unidad vestible fuera del cuerpo. Allí, un ordenador compacto utiliza software avanzado de reconocimiento de patrones para separar el tejido normal de las lesiones sospechosas que podrían ser cancerosas o estar gravemente inflamadas. Esta configuración refleja la endoscopia en cápsula ya usada en hospitales, pero se mejora para funcionar en tiempo real y conectarse directamente con herramientas de tratamiento.
La inteligencia artificial como tomadora de decisiones
La unidad vestible ejecuta un modelo de análisis de imágenes cuidadosamente entrenado, basado en técnicas modernas de visión por computador. Aprendió a reconocer 25 condiciones gastrointestinales diferentes —desde pólipos y úlceras hasta inflamación severa— usando una gran colección pública de imágenes endoscópicas y de tejido. Para enfrentar el hecho de que algunas enfermedades son mucho más raras que otras, los autores entrenaron el sistema en dos etapas: primero para aprender las huellas visuales generales de cada condición, y luego para afinarlo de modo que hallazgos peligrosos pero poco comunes no sean ignorados. En las pruebas, este enfoque clasificó correctamente las imágenes en más de nueve de cada diez casos y funcionó especialmente bien en las categorías relacionadas con el cáncer.
Ver dentro de la «caja negra»
Dado que el personal médico debe confiar en cualquier diagnóstico automatizado que pueda influir en la dosis de un fármaco, los autores usaron técnicas de IA explicable para mostrar qué partes de cada imagen impulsan la decisión del modelo. Superposiciones al estilo mapa de calor resaltan las regiones exactas que el sistema consideró importantes. Estos mapas explicativos no solo se inspeccionaron visualmente; se puntuaron con pruebas cuantitativas que midieron cuánto cambiaba la confianza del modelo cuando se eliminaban o añadían las regiones resaltadas, cuán estables eran las explicaciones entre repeticiones de entrenamiento y cuánto se solapaban con contornos de lesiones dibujados por expertos. Entre varios métodos probados, uno llamado LayerCAM produjo las explicaciones más fieles y consistentes, ayudando a los médicos a verificar que el sistema está «mirando» en el lugar correcto.
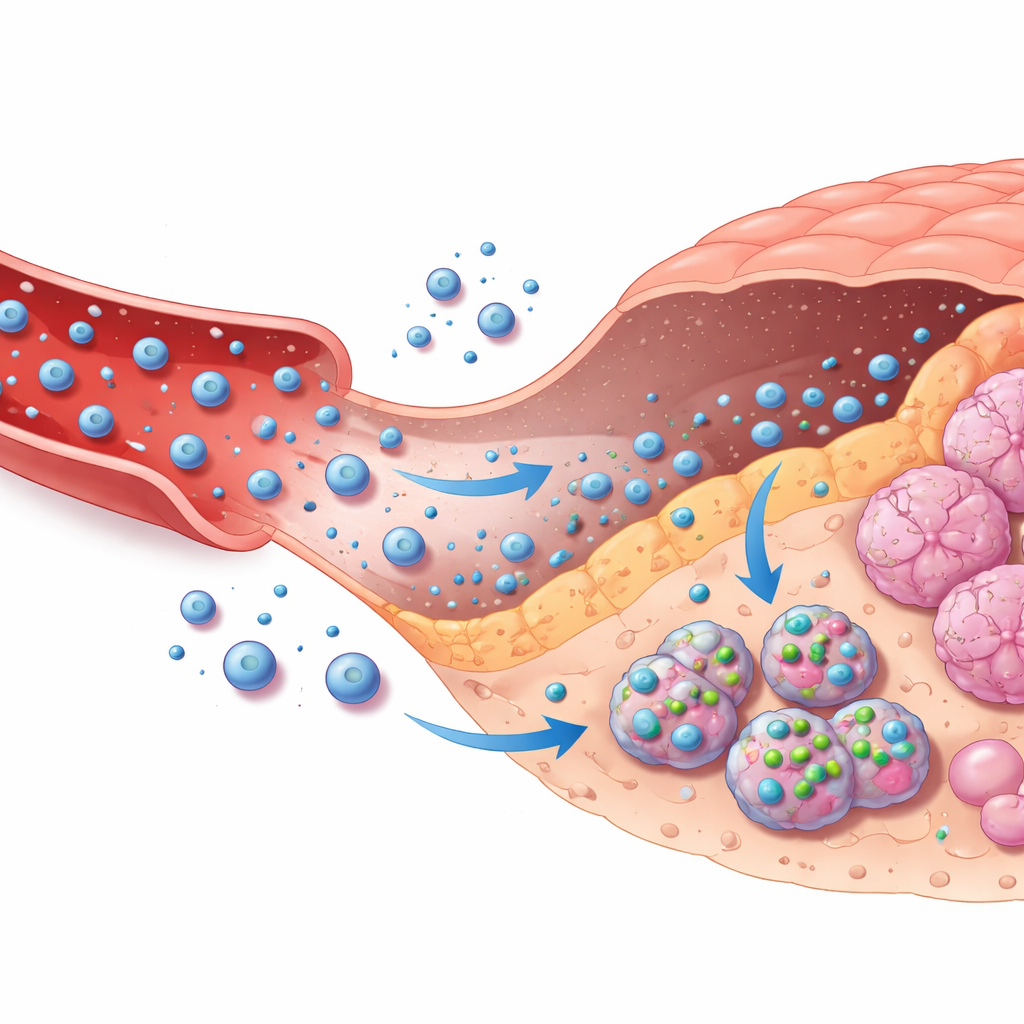
Guiando portadores de fármacos por el cuerpo
La segunda mitad del marco conecta estas decisiones basadas en imágenes con la administración dirigida de quimioterapia. Los autores modelan cómo un fármaco común contra el cáncer, la doxorrubicina, viaja desde una bomba externa por el torrente sanguíneo, se filtra en el tejido tumoral, entra en las células tumorales y finalmente se elimina. Esto se captura en un modelo matemático multicompartmental que rastrea los niveles de fármaco en la sangre, el tejido circundante y dentro de las células. Según la confianza de la IA de que una lesión es maligna y la severidad aparente, un sistema de reglas simple elige entre no tratar, tratar de forma moderada o intensiva, ajustando la velocidad a la que las nanopartículas cargadas liberan su carga y la duración de la infusión. Una capa de seguridad comprueba constantemente los niveles de fármaco predichos dentro de las células y reduce automáticamente la dosis si se aproxima un techo seguro, incluso si la IA está demasiado confiada.
Protección de la privacidad y prevención del uso indebido
Como el mismo enlace que transporta imágenes también puede llevar comandos de tratamiento, la seguridad es crítica. Los autores introducen un esquema de privacidad ligero que encripta las señales biomédicas usando un mapa matemático caótico antes de que viajen por la nano‑red del cuerpo, haciendo que los datos interceptados sean muy difíciles de interpretar. Además, la pasarela vestible autentica los dispositivos y verifica que las señales de control coincidan con patrones físicos esperados, contribuyendo a bloquear comandos falsos. Las simulaciones muestran cómo distintos ajustes de privacidad intercambian una pequeña pérdida en la precisión de detección por una protección más fuerte, e identifican puntos de operación que mantienen un alto rendimiento clínico mientras limitan drásticamente la fuga de datos. Junto con límites estrictos de dosis, reglas de desconexión de emergencia y registros de seguridad, estas medidas pretenden hacer que el sistema sea resistente tanto a accidentes como a ataques.
Qué podría significar esto para los pacientes
En pocas palabras, este trabajo dibuja cómo podría funcionar un ciclo de «ver y tratar» dentro del cuerpo: una cámara ingerible detecta puntos sospechosos, un asistente inteligente interpreta lo que ve con razonamiento transparente y un sistema de administración controlada responde con dosis cuidadosamente acotadas y centradas en el tejido enfermo. El estudio sigue siendo teórico y se basa en simulaciones, pero muestra que un diseño de bucle cerrado así puede alcanzar objetivos terapéuticos y respetar límites estrictos de seguridad, incluso cuando la IA comete errores o las condiciones varían entre personas. Si se materializa en la práctica, este tipo de sistema podría ayudar a convertir la quimioterapia poco selectiva en una herramienta mucho más precisa y personalizada para las enfermedades gastrointestinales.
Cita: Kamal, I.R., El-Zoghdy, S.F. & Soliman, R.F. Explainable AI for gastrointestinal lesion surveillance and precision targeted drug delivery. Sci Rep 16, 9807 (2026). https://doi.org/10.1038/s41598-026-40882-z
Palabras clave: imágenes gastrointestinales, IA explicable, administración dirigida de fármacos, nanomedicina, endoscopia en cápsula