Clear Sky Science · es
Separación eficaz por vórtices de Dean a caudales reducidos hacia la clasificación de células raras
Por qué importa clasificar células raras
Las células cancerosas que se desprenden al torrente sanguíneo u otros fluidos corporales son como señales tempranas de enfermedad. Sin embargo, están ampliamente superadas en número por las células sanguíneas comunes, lo que hace que sean extremadamente difíciles de detectar y estudiar. Este trabajo describe un nuevo dispositivo a microescala que utiliza flujos en remolino suaves dentro de un diminuto canal en espiral para desviar células más grandes y con aspecto canceroso respecto a glóbulos blancos más pequeños a velocidades de fluido mucho más bajas de lo habitual. Este enfoque de bajo estrés y fácil integración podría ayudar a los laboratorios a enriquecer células raras para diagnóstico y seguimiento del tratamiento sin dañarlas.
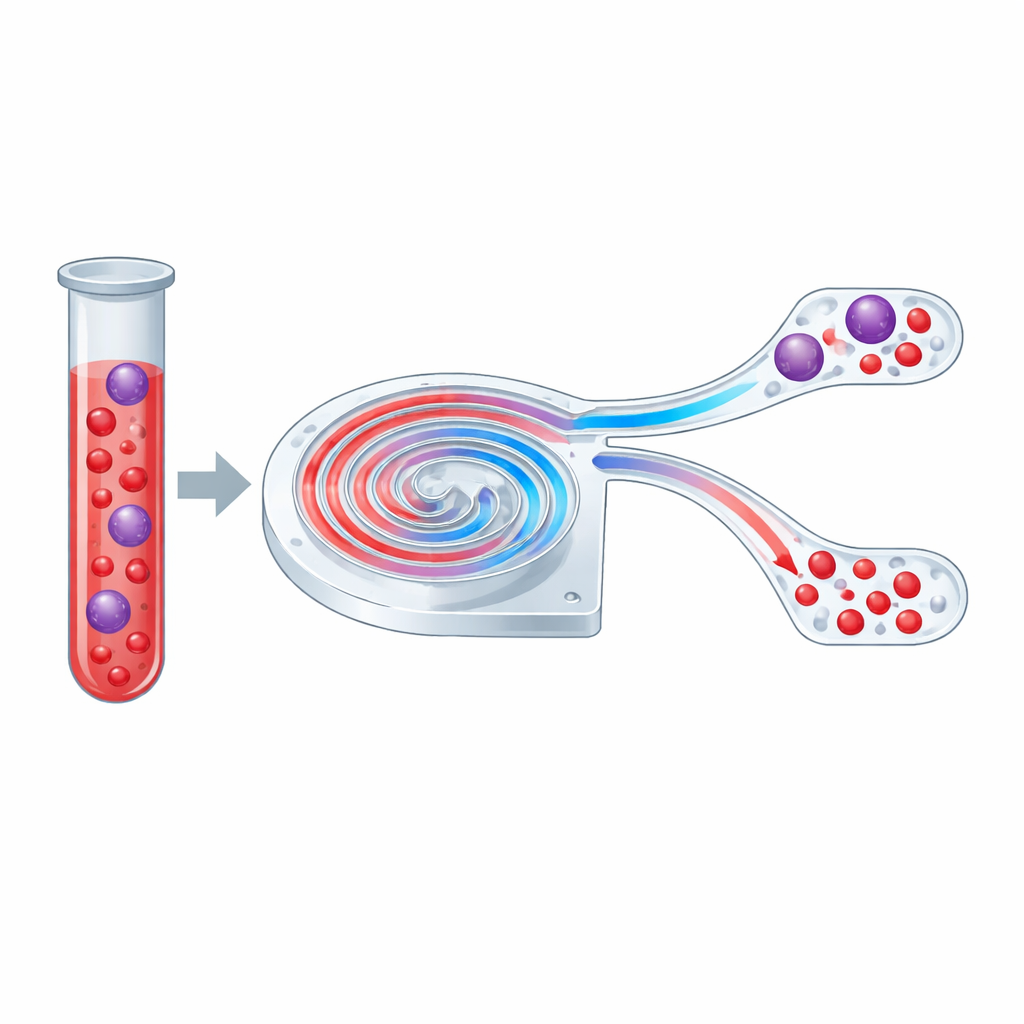
Una pequeña vía en espiral para las células
El núcleo del estudio es un microchip transparente que contiene un canal en forma de espiral más delgado que un cabello humano. Cuando el fluido circula por un canal recto, las células sienten principalmente un empuje en la dirección del flujo y un sutil empujón lateral que depende de su tamaño. En un trazado curvo y en espiral aparece un segundo efecto: el líquido forma remolinos emparejados a través de la sección transversal del canal, conocidos como vórtices de Dean. Estos remolinos arrastran objetos más pequeños a través de la corriente mientras que los más grandes quedan más cerca de un lado. Al ajustar este equilibrio, los autores diseñaron una espiral que puede dividir una mezcla de partículas o células en dos corrientes basándose fundamentalmente en el tamaño.
Hacer que las espirales funcionen a velocidades suaves
La mayoría de los dispositivos en espiral existentes filtran con eficacia solo cuando se impulsan con mucha fuerza, a caudales de cientos a miles de mililitros por hora. Tales condiciones reducen el tiempo de procesamiento pero aumentan el esfuerzo cortante sobre las células y dificultan conectar la espiral con otros pasos microfluídicos que prefieren flujos más lentos y controlados. El equipo se marcó un objetivo distinto: mantener una separación fuerte basada en tamaño alrededor de 50 mililitros por hora, un orden de magnitud más suave. Para lograrlo, variaron sistemáticamente la geometría de nueve diseños de espiral —cambiando el ancho y la altura del canal y la pendiente de la pared exterior— y combinaron experimentos con simulaciones informáticas del flujo circulante.
Seguir partículas a través de los remolinos
Para entender primero la física, los investigadores hicieron circular perlas plásticas fluorescentes de dos tamaños, 10 y 15 micrómetros, por cada espiral. A bajas velocidades, ambos tipos de perlas se concentraban cerca de la pared interior. Al aumentar el flujo, la franja focalizada se desplazó a través del canal hacia la pared exterior, pero a velocidades umbral diferentes para cada tamaño. Para un diseño representativo, las perlas más pequeñas cambiaron hacia el exterior alrededor de 30 mililitros por hora, mientras que las más grandes lo hicieron alrededor de 60 mililitros por hora. Esto creó un rango intermedio donde las perlas grandes y pequeñas salían por lados opuestos. Las simulaciones del movimiento del fluido revelaron que, a velocidades mayores, las perlas se asientan muy cerca de los centros de los vórtices de Dean, confirmando una idea largamente sostenida pero previamente no probada sobre cómo funcionan estos dispositivos.
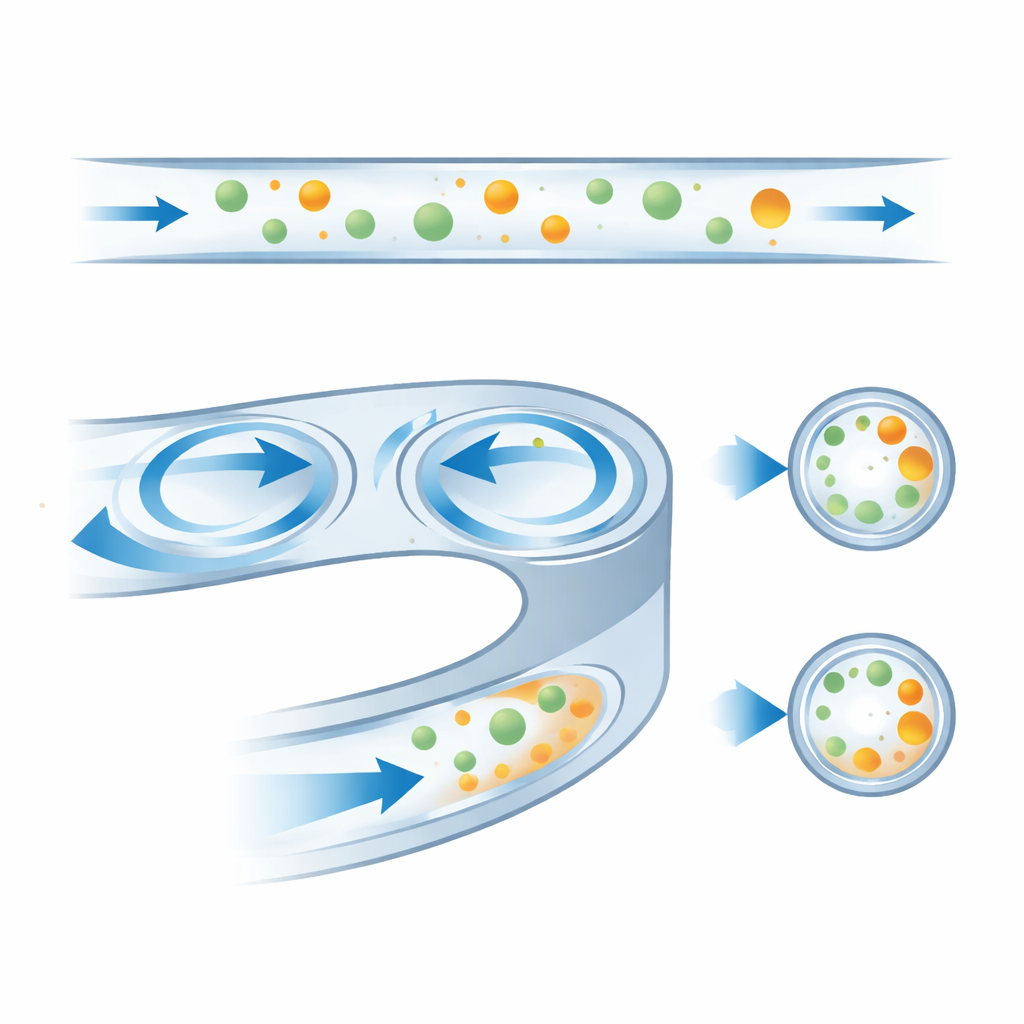
Moldear el canal para la mejor separación
Al comparar muchos diseños, los autores identificaron cómo elecciones geométricas simples controlan el rendimiento. Una pendiente más pronunciada en la pared exterior empuja los remolinos internos más hacia afuera, desplazando las posiciones estables de las perlas y cambiando el caudal al que intercambian lados. Los canales estrechos acercan los vórtices demasiado a la pared interior, haciendo que las partículas sean atraídas hacia ellos demasiado pronto, mientras que los canales muy planos exigen velocidades mayores antes de que ocurra cualquier desplazamiento. El mejor compromiso usó un canal de 250 micrómetros de ancho con una pendiente de pared y una relación de aspecto moderadas, lo que proporcionó una separación clara entre los dos tamaños de perlas a 40–60 mililitros por hora y se mantuvo robusto ante pequeñas variaciones del flujo.
De perlas plásticas a células cancerosas vivas
Con la espiral óptima en mano, el equipo pasó a muestras biológicas. Probaron varias líneas celulares cancerosas que emulan las células tumorales circulantes y compararon su comportamiento con el de glóbulos blancos procedentes de sangre preparada. A pesar de ser más blandas y más variadas en tamaño que las perlas, todos los tipos celulares se enfocaron en franjas estrechas y pasaron de la cara interior a la exterior a medida que aumentaba el flujo, de forma fuertemente dependiente del tamaño. Operando a 50 mililitros por hora, el dispositivo condujo aproximadamente el 89% de los glóbulos blancos hacia el lado de “desecho” mientras mantenía al 75–86% de las células con aspecto canceroso en el lado “enriquecido”. Es importante destacar que la supervivencia celular se mantuvo alrededor del 98%, incluso después de pasar por la espiral a distintos caudales.
Qué supone esto para futuras pruebas de cáncer
En pocas palabras, los autores han construido y descifrado un pequeño filtro en espiral que puede eliminar con suavidad la mayor parte de las células sanguíneas de fondo mientras retiene las más raras y grandes con aspecto canceroso, todo a caudales relativamente lentos y compatibles con las células. Al aclarar cómo se forman las corrientes interiores y exteriores y cómo la forma del canal las controla, el trabajo convierte una tecnología en gran medida empírica en una herramienta más predecible. Por sí solo, el dispositivo no capturará todas las células cancerosas, pero proporciona un potente paso de preenriquecimiento que se puede vincular directamente con métodos biológicos más selectivos. Esta combinación podría, en última instancia, facilitar la detección, el análisis y el seguimiento del cáncer usando pequeñas muestras de fluidos de pacientes.
Cita: Dupont, E., Artinyan, L., Brunin, C. et al. Effective dean vortex separation at reduced flow rates towards rare cell sorting. Sci Rep 16, 10422 (2026). https://doi.org/10.1038/s41598-026-40845-4
Palabras clave: clasificación microfluídica de células, microcanal en espiral, células tumorales circulantes, vórtices de Dean, biopsia líquida