Clear Sky Science · es
Un microARN derivado del empalme del exón 4 de la amelogenina regula la formación del esmalte mediante el control del empalme del exón 4 y la expresión de amelogenina
Por qué un ARN diminuto importa para unos dientes fuertes
El esmalte dental es la sustancia más dura del cuerpo humano, pero puede resultar sorprendentemente frágil cuando su formación falla. Este estudio revela cómo un fragmento muy pequeño de material genético, un microARN denominado miR‑exon4, ayuda a las células formadoras de dientes a construir un esmalte correctamente endurecido. Al mostrar que este microARN ajusta tanto la proteína principal del esmalte como la sincronía de la deposición mineral, el trabajo vincula el sutil procesamiento de ARN dentro de las células con defectos visibles en el esmalte similares a los observados en una enfermedad hereditaria llamada amelogénesis imperfecta.
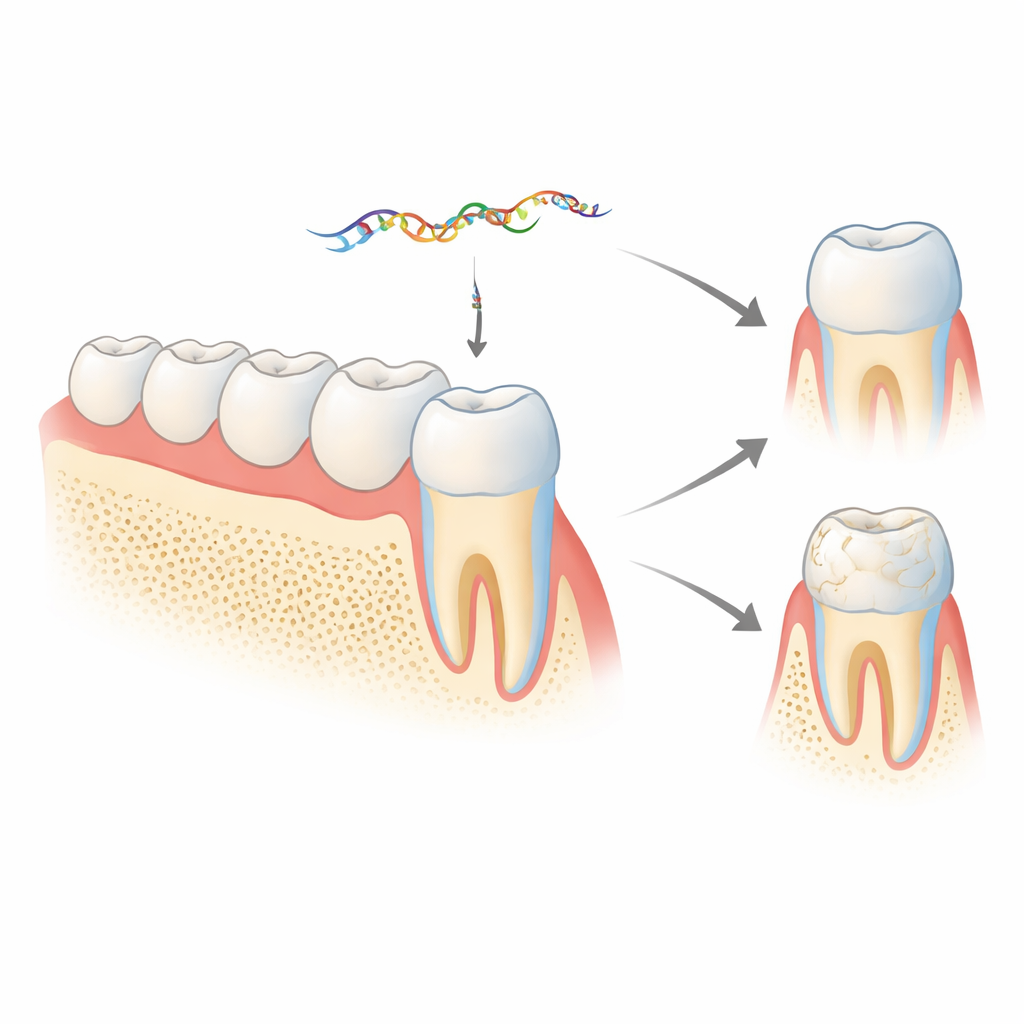
Un mensaje oculto dentro de un gen del esmalte
El esmalte se construye en gran medida a partir de una proteína llamada amelogenina, producida por células conocidas como ameloblastos. El gen de la amelogenina (Amelx en ratones) puede cortarse y pegarse de distintas maneras, creando varias versiones proteicas necesarias en diferentes etapas del desarrollo dental. Un segmento corto, denominado exón 4, suele eliminarse del mensaje final codificante. Trabajos previos de este grupo mostraron que el exón 4 descartado no es un residuo inútil: se procesa en un microARN, miR‑exon4, que puede regular otros genes importantes para el hueso y el esmalte. El nuevo estudio pregunta qué ocurre en animales vivos cuando este microARN se reduce o bloquea, y si además retroalimenta para controlar cómo se ensamblan las propias amelogeninas.
Una cadena reguladora dentro de las células formadoras de dientes
Los investigadores confirmaron primero en dientes de ratón que miR‑exon4 participa en una cadena reguladora que ya habían trazado en cultivos celulares. En órganos del esmalte normales, miR‑exon4 mantiene a raya a dos genes upstream, Nfia y Prkch. Cuando estos se mantienen bajos, aumentan los niveles de un factor de transcripción clave, RUNX2. Usando ratones que carecían del gen de la amelogenina, que recibieron miR‑exon4 adicional o que fueron tratados con un bloqueador de miR‑exon4, el equipo demostró que reducir miR‑exon4 eleva Nfia y Prkch y disminuye RUNX2, mientras que añadir miR‑exon4 produce el efecto contrario. Esto confirmó que la vía miR‑exon4–Nfia/Prkch–RUNX2 funciona in vivo dentro de los dientes en desarrollo.
De señales alteradas a un esmalte más débil
Para evaluar cómo estos cambios moleculares afectan al esmalte real, los científicos inhibieron miR‑exon4 en crías de ratón durante una semana en la fase activa de formación dental. Imágenes tridimensionales por rayos X revelaron que los animales tratados mostraban una clara disminución de esmalte altamente mineralizado tanto en incisivos como en molares. Los mapas de calor y las secciones teñidas mostraron que el inicio de la acumulación mineral a lo largo de la capa de esmalte se retrasó y que la fase temprana de mineralización se acortó, lo que condujo a superficies más rugosas y límites difusos entre el esmalte y los tejidos subyacentes. Al mismo tiempo, los niveles de la proteína RUNX2 en los ameloblastos cayeron, mientras que la proteína amelogenina —incluidas las versiones que contienen el exón 4— aumentó. Este patrón refleja modelos previos en los que la sobreproducción de una forma larga de amelogenina con exón 4 provoca defectos del esmalte, lo que sugiere que el exceso de este isoforma, desencadenado por la pérdida de miR‑exon4, puede perturbar directamente la mineralización normal.
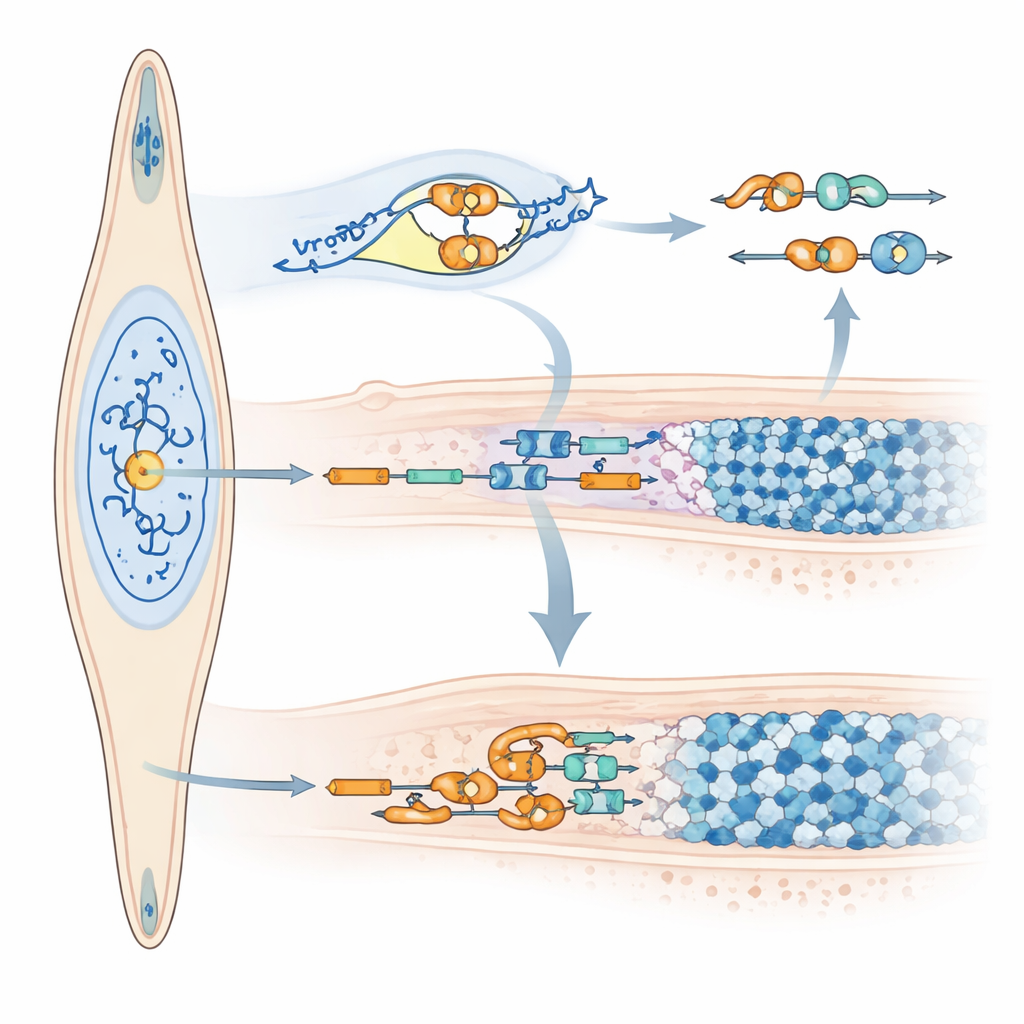
Cómo el microARN remodela el mensaje de la amelogenina
Más allá de cambiar la cantidad de amelogenina que se produce, miR‑exon4 también altera cómo se corta y empalma el mensaje de la amelogenina. El bloqueo a corto plazo de miR‑exon4 redujo las moléculas de ARN que aún contenían el exón 4 sin cambiar los niveles totales de amelogenina, lo que indica que el exón 4 se estaba eliminando con más frecuencia. El equipo relacionó este cambio con variaciones en varios genes reguladores del empalme (SRSFs), con algunos aumentados y otros disminuidos cuando se redujo miR‑exon4. En modelos celulares que portaban una versión especialmente diseñada del gen de la amelogenina que produce menos miR‑exon4, el exón 4 también se omitió con mayor frecuencia. De manera crucial, se encontró el propio microARN dentro del núcleo celular, donde ocurre el empalme, y pruebas bioquímicas mostraron que se asocia con el ARN precursor de la amelogenina en un punto de control específico del intrón adyacente. Estos hallazgos respaldan un papel dual para miR‑exon4: moldear indirectamente la elección de exones ajustando factores de empalme, y unirse directamente cerca del exón 4 para influir en si se conserva o se elimina.
Qué significa esto para la salud del esmalte
En conjunto, el estudio pinta a miR‑exon4 como un coordinador pequeño pero central de la formación del esmalte. Cuando está presente en el nivel adecuado, apoya la actividad correcta de RUNX2, mantiene en equilibrio la producción de amelogenina y ayuda a asegurar que el exón 4 se incluya o excluya en las etapas apropiadas. Cuando miR‑exon4 falta o se reduce, este equilibrio se desplaza: las vías de señalización se alteran, el exón 4 se gestiona incorrectamente, los isoformas de amelogenina se desequilibran y la mineralización temprana del esmalte se debilita. Estas ideas ayudan a explicar cómo ciertas mutaciones en el gen de la amelogenina pueden causar trastornos hereditarios del esmalte y ponen de relieve a los microARN nucleares como actores importantes en la formación del tejido más duro del cuerpo.
Cita: Shemirani, R., Duong, T., Kim, R. et al. A splicing-derived microRNA from amelogenin exon4 regulates enamel formation via control of exon4 splicing and amelogenin expression. Sci Rep 16, 11044 (2026). https://doi.org/10.1038/s41598-026-40706-0
Palabras clave: esmalte dental, amelogenina, microARN, empalme de ARN, amelogénesis imperfecta