Clear Sky Science · es
ABE9 fusionado con la nickasa SpRY Cas9 permite la generación precisa de modelos de ratón sin efectos colaterales
Herramientas más finas para construir mejores modelos de enfermedad
Muchas enfermedades graves se deben a errores de una sola letra en nuestro ADN. Para comprender y, en última instancia, tratar estas afecciones, los científicos suelen crear ratones que llevan las mismas mutaciones que los pacientes humanos. Pero reescribir el ADN de forma tan precisa es sorprendentemente difícil: los métodos anteriores pueden dejar cicatrices en el genoma, introducir mutaciones adicionales y confundir los resultados experimentales. Este estudio presenta una herramienta de edición genética refinada, llamada ABE9-SpRY, diseñada para cambiar una letra específica del ADN dejando las letras vecinas —y el resto del genoma— en gran medida intactas.
De cortes contundentes a ajustes suaves del ADN
La edición CRISPR-Cas9 tradicional funciona como unas tijeras moleculares, cortando ambas hebras del ADN. Las células reparan estas roturas de forma imperfecta, con frecuencia dejando pequeñas inserciones o deleciones que alteran genes de manera impredecible. Eso es útil para desactivar genes, pero no para imitar una mutación precisa que cause enfermedad. Los editores de bases, por el contrario, no cortan el ADN. En su lugar, empujan químicamente una letra del ADN hacia otra —aquí, cambiando A por G— mientras mantienen la doble hélice intacta. Este enfoque reduce drásticamente las grandes deleciones y reorganizaciones, pero las primeras versiones de editores de adenina seguían teniendo tres problemas clave: a veces editaban letras vecinas “espectadoras”, solo podían alcanzar sitios del ADN junto a etiquetas de secuencia cortas específicas y, ocasionalmente, causaban ediciones en lugares no deseados del genoma.
Diseñando un lápiz molecular más selectivo
Los investigadores se propusieron abordar las tres limitaciones a la vez. Comenzaron con ABE9, una variante más reciente del editor de bases que concentra su actividad en un tramo de ADN muy estrecho, reduciendo tanto la “ventana de edición” que se modifican muchas menos letras vecinas por accidente. Luego fusionaron ABE9 con una nickasa Cas9 diseñada llamada SpRY. A diferencia de la Cas9 estándar, que requiere una etiqueta estricta “NGG” junto al sitio objetivo, SpRY puede reconocer un conjunto mucho más amplio de secuencias de ADN. Esto hace posible alcanzar posiciones relacionadas con enfermedades en el genoma que antes estaban fuera de alcance. La herramienta resultante, ABE9-SpRY, pretende ser tanto altamente precisa como mucho más flexible en cuanto a dónde puede actuar.
Poniendo a prueba el nuevo editor en células y embriones
Para ver si ABE9-SpRY cumplía su diseño, el equipo lo comparó con un editor más agresivo y ampliamente usado llamado ABE8e-SpRY. Dirigieron la edición a cuatro posiciones relevantes para la enfermedad en genes que codifican canales iónicos (TPC1, TPC2 y TRPM4), que desempeñan papeles importantes en la función cardiaca y hepática. En células nerviosas de ratón cultivadas en el laboratorio, ABE8e-SpRY editó la letra objetivo con mayor eficiencia pero también modificó muchas bases cercanas. ABE9-SpRY, en contraste, produjo menos ediciones en total pero una fracción mucho mayor de resultados “limpios”: lecturas en las que solo se cambió la letra prevista, sin mutaciones adicionales en la región local. El mismo patrón se mantuvo en embriones de ratón. Cuando los investigadores inyectaron los componentes de edición en óvulos fertilizados, ABE8e-SpRY con frecuencia convirtió casi todas las copias del gen objetivo pero con muchos cambios de espectadores. ABE9-SpRY editó menos copias en general, pero donde actuó, la secuencia de ADN se corregía típicamente exactamente como se planeó.
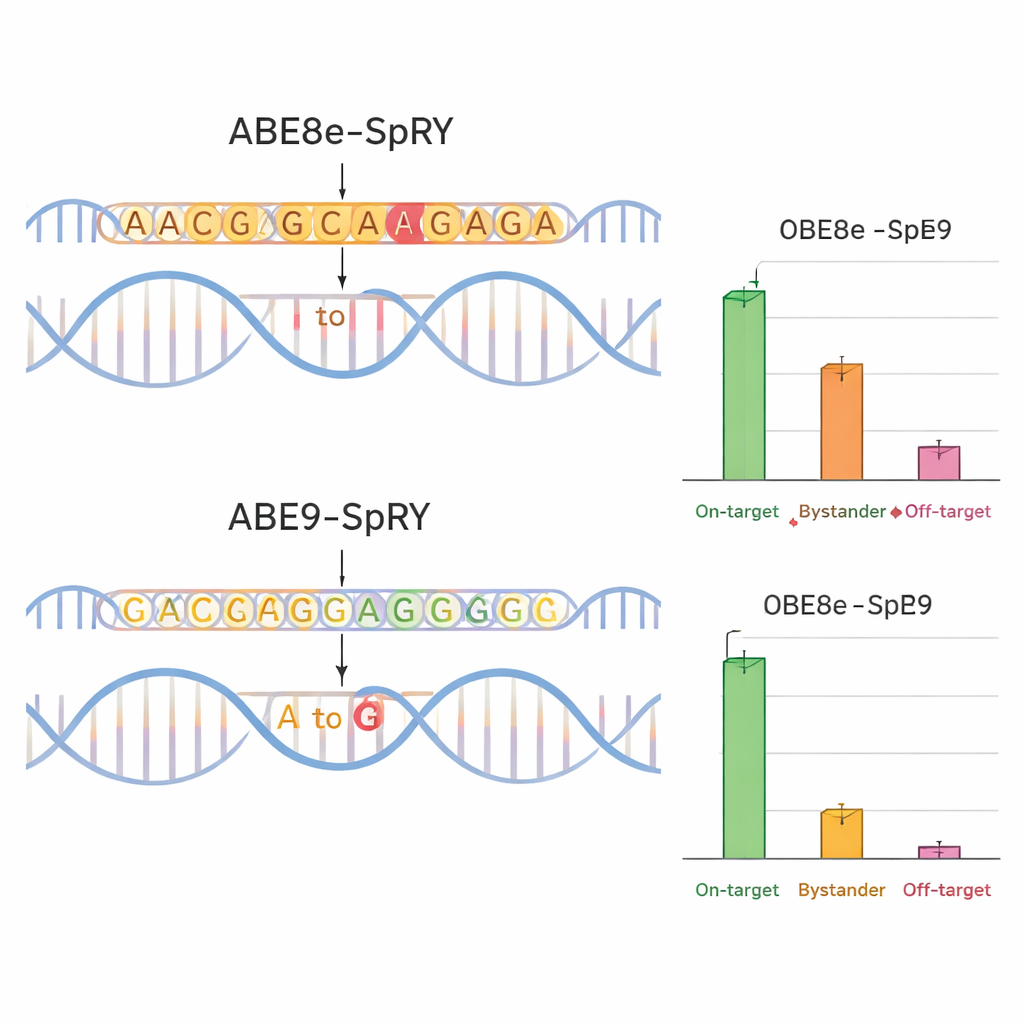
Ediciones más limpias, menos efectos secundarios
La precisión no se limita al vecindario local del ADN. El equipo también examinó si su editor alteraba regiones distantes del genoma. Usando predicciones computacionales y secuenciación dirigida, midieron cambios fuera del objetivo en sitios que podían parecerse al objetivo en embriones de ratón. ABE8e-SpRY con frecuencia introdujo cambios no deseados de A a G en estas ubicaciones, a veces en niveles sorprendentemente altos. ABE9-SpRY mostró muchos menos de estos eventos, con solo ediciones fuera del objetivo raras y ninguna actividad detectable en una prueba especializada para daño del ADN independiente de Cas9. Es importante destacar que, cuando ABE9-SpRY se utilizó solo —no en pruebas agrupadas— para introducir dos mutaciones específicas en ratones, generó muchos animales fundadores en los que la edición deseada estaba presente en altos niveles y se transmitía de forma fiable a la descendencia, nuevamente con cambios de espectadores mínimos o pequeñas inserciones y deleciones.
Extendiendo la edición precisa a células madre humanas
Dado que las células madre específicas de pacientes se usan cada vez más para estudiar enfermedades y probar fármacos, los investigadores también probaron ABE9-SpRY en células madre pluripotentes inducidas humanas. Apuntaron a la versión humana del gen TPC1 en una posición equivalente a una de las ubicaciones en ratón. Usando un reportero fluorescente para enriquecer las células editadas, encontraron que ABE8e-SpRY producía tasas de edición brutas más altas pero, de nuevo, modificaba múltiples bases cercanas. ABE9-SpRY editó menos alelos en total, pero la proporción de tramos perfectamente editados —un cambio intencionado y nada más— fue notablemente mayor, con menos inserciones o deleciones disruptivas. En trabajos con células madre, donde se expanden clones individuales para un estudio detallado, este tipo de edición “limpia” suele ser más valiosa que la eficiencia bruta.
Por qué esto importa para la investigación de enfermedades futura
Para los científicos que intentan entender cómo un cambio de una sola letra en el ADN conduce a una enfermedad, las mutaciones no deseadas adicionales pueden ser profundamente engañosas. Este estudio muestra que ABE9-SpRY, aunque algo menos potente en términos de velocidad de edición bruta, puede escribir cambios de una sola letra en los genomas de ratones y células madre humanas con una precisión llamativa y una amplia flexibilidad de orientación. Eso lo convierte en una herramienta prometedora para construir modelos animales y celulares fieles de trastornos genéticos humanos, especialmente en situaciones donde incluso una mutación accidental podría confundir la biología o descarrilar una terapia potencial.
Cita: Ong, J.K., Bhunia, S., Hilbert, B. et al. ABE9 fused to SpRY Cas9 nickase enables precise generation of bystander free mouse models. Sci Rep 16, 7463 (2026). https://doi.org/10.1038/s41598-026-40642-z
Palabras clave: edición de bases de adenina, modelos de enfermedad CRISPR, genética de ratón, efectos fuera del objetivo, edición génica en hiPSC