Clear Sky Science · es
La variante de la quimotripsina C (CTRC) asociada a pancreatitis p.R240Q perjudica selectivamente la degradación del tripsinógeno mediante la alteración de interacciones electrostáticas de largo alcance
Por qué importa para la salud pancreática
La pancreatitis crónica es una inflamación dolorosa y prolongada del páncreas que puede conducir a diabetes, problemas digestivos y una caída significativa de la calidad de vida. Este estudio analiza por qué algunas personas son más vulnerables debido a pequeños cambios heredados en sus enzimas digestivas. Al centrarse en una única variante genética de una enzima protectora, los autores muestran cómo un cambio molecular sutil puede inclinar la balanza de la protección hacia el autodaño dentro del páncreas.
Un sistema de seguridad incorporado en la digestión
Nuestro páncreas produce potentes enzimas que digieren proteínas y que normalmente se liberan en el intestino en forma inactiva. Uno de estos precursores, el tripsinógeno, a veces puede activarse prematuramente, dentro del propio páncreas. Cuando eso ocurre, puede empezar a digerir el órgano desde dentro y desencadenar inflamación. Para controlar esto, el organismo dispone de salvaguardas, incluyendo una proteína inhibidora (SPINK1) y otra enzima digestiva, la quimotripsina C (CTRC). La CTRC tiene un papel dual: ayuda a activar las enzimas digestivas donde y cuando se necesitan, pero también corta el exceso de tripsinógeno antes de que se convierta en tripsina activa y cause daño. Se sabe que las personas que heredan formas debilitadas de CTRC tienen un mayor riesgo de pancreatitis crónica.
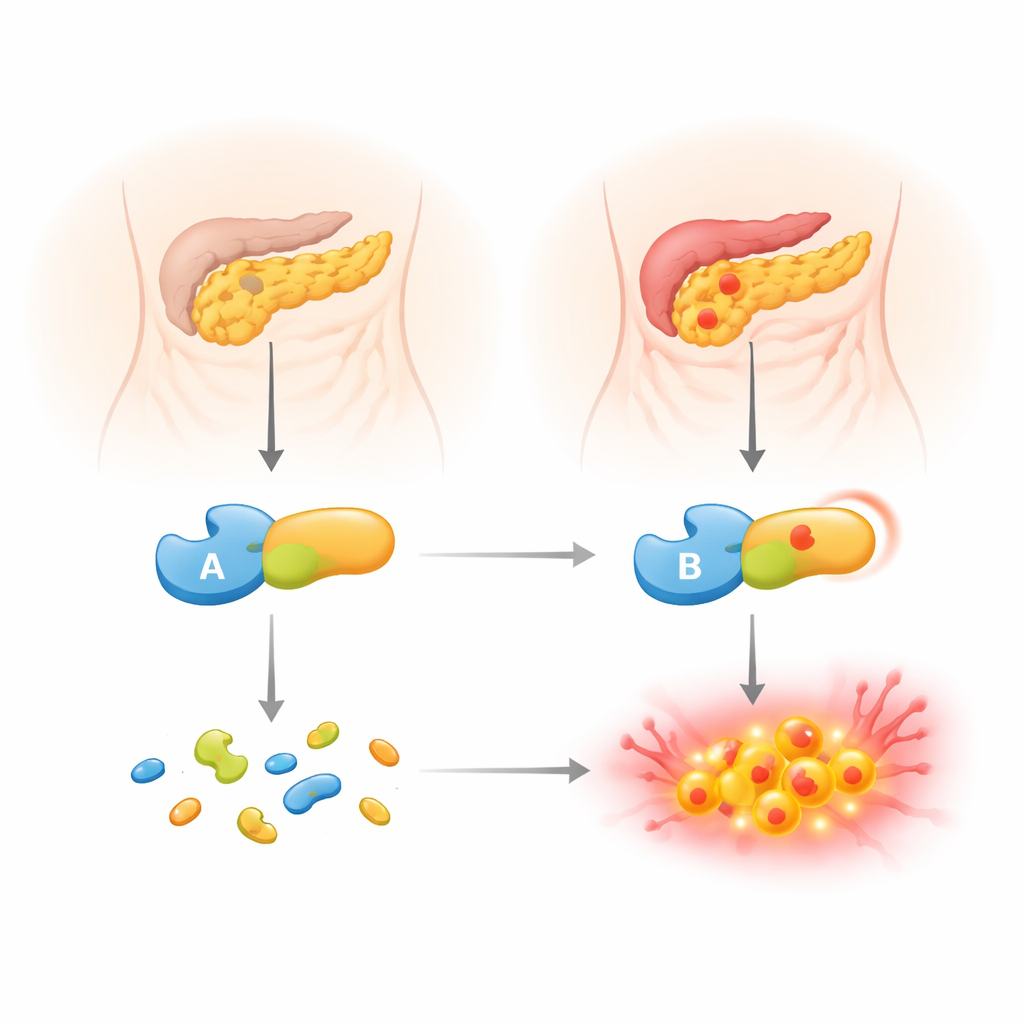
Un cambio genético raro bajo el microscopio
El equipo se centró en una variante poco común de CTRC denominada p.R240Q, encontrada en un niño de Eslovaquia con pancreatitis crónica de inicio infantil y en su padre afectado. Esta variante cambia un único bloque constructivo en la superficie de la enzima, intercambiando una unidad con carga positiva por una neutra. Grandes bases de datos genéticas la clasifican como probablemente inocua, sin embargo ha aparecido en varios pacientes jóvenes con la enfermedad. Para averiguar qué hace realmente, los autores combinaron la información genética de la familia con experimentos detallados de laboratorio. Compararon la enzima variante lado a lado con la CTRC normal, examinando cómo se produce y secreta en las células, su actividad sobre sustratos estándar y cómo interactúa con el tripsinógeno, la diana clave que debe controlar.
Fuerza normal, pero puntería desplazada
Primero, los investigadores mostraron que las células producen y secretan la enzima p.R240Q igual de bien que la versión normal, por lo que la variante no provoca plegamiento incorrecto ni fallos de producción. En ensayos de tubo de ensayo usando un pequeño péptido sintético y una proteína láctea (beta-caseína), la variante funcionó tan bien o incluso ligeramente mejor que la CTRC normal. Esto significa que su capacidad de corte está intacta. La sorpresa llegó al examinar la reacción que más importa para la pancreatitis: descomponer el tripsinógeno catiónico humano. Aquí, la enzima variante fue mucho menos eficaz: aproximadamente cuatro a cinco veces más lenta en destruir el tripsinógeno y mucho peor previniendo que el tripsinógeno se autoactive en tripsina. En experimentos de autoactivación, se necesitó mucha más CTRC variante para mantener los niveles de tripsina bajo control en comparación con la enzima normal.
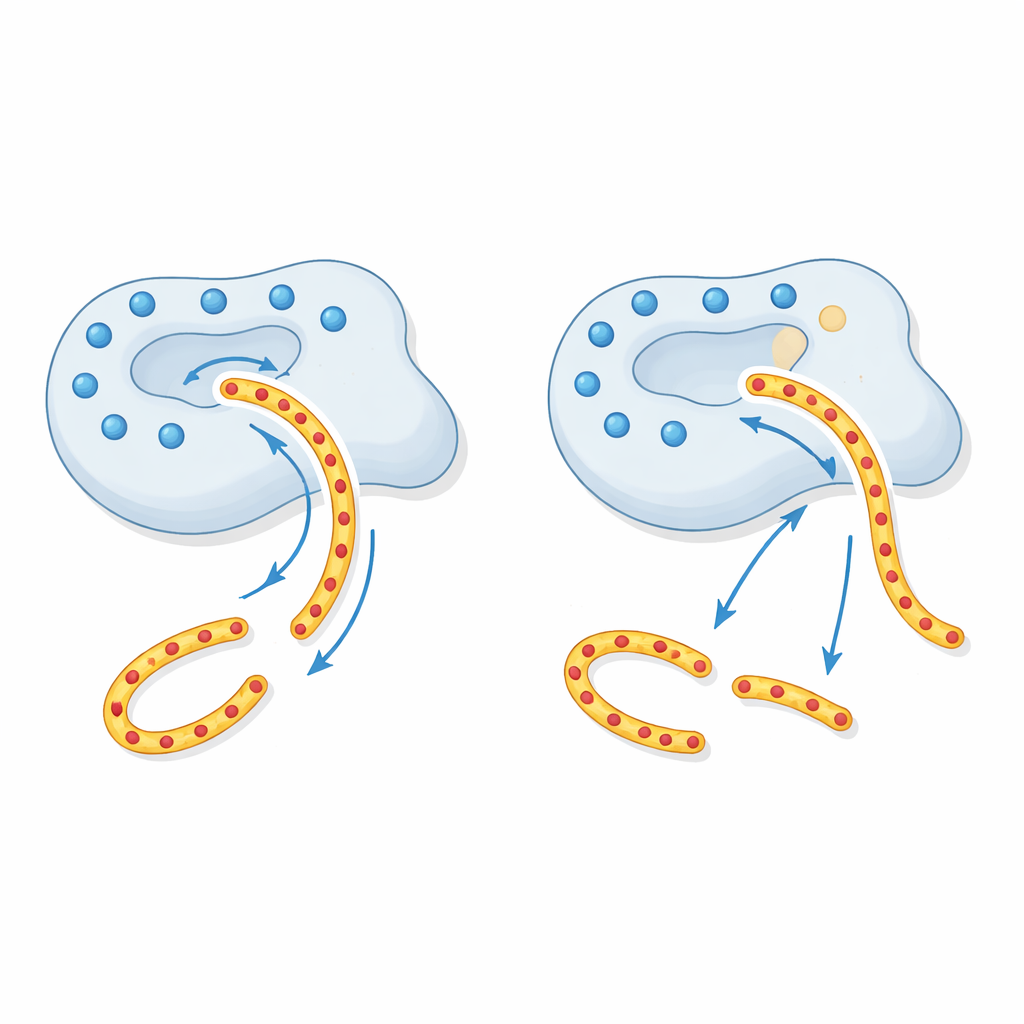
Un “rayo tractor” electrostático alterado
Para entender por qué ocurre esto, los autores recurrieron a modelos estructurales de CTRC. Alrededor del surco donde la CTRC sujeta sus sustratos, existe un anillo de carga eléctrica positiva formado por varios aminoácidos cargados, incluido el sitio alterado en p.R240Q. Las regiones del tripsinógeno que la CTRC debe cortar son fuertemente negativas, por lo que este anillo positivamente cargado actúa como un “rayo tractor” de largo alcance, guiando el tripsinógeno hacia la posición adecuada. Al neutralizar uno de estos puntos positivos, la variante p.R240Q debilita esta atracción a distancia. La enzima sigue siendo afilada, pero el sistema de guía dañado hace que el tripsinógeno no se una con la misma eficiencia, de modo que menos cantidad se degrada de forma segura. Otros sustratos que no dependen tan fuertemente de este patrón de carga se procesan con normalidad, explicando el defecto tan selectivo observado en los experimentos.
Qué significa esto para pacientes y pruebas
Clínicamente, el niño afectado y su padre también portaban una segunda variante dañina de CTRC, y el padre presentaba factores de riesgo de estilo de vida adicionales, como consumo elevado de alcohol. Esto encaja con la idea de que la pancreatitis crónica suele resultar de varias agresiones genéticas y ambientales que se suman. El trabajo demuestra que una variante que aparenta ser inocua según las herramientas predictivas comunes puede seguir siendo peligrosa de una manera muy específica. Para las pruebas genéticas, el mensaje es claro: al juzgar si una variante de CTRC aumenta el riesgo de pancreatitis, los científicos deben evaluarla sobre la diana real, el tripsinógeno, y no solo sobre sustratos genéricos de laboratorio. En términos cotidianos, este estudio revela cómo un pequeño cambio en la “superficie guía” de la enzima puede socavar silenciosamente uno de los principales seguros del páncreas, empujando a individuos susceptibles hacia la inflamación crónica.
Cita: Nagy, Z.A., Sándor, M., Hegyi, E. et al. Pancreatitis-associated chymotrypsin C (CTRC) variant p.R240Q selectively impairs trypsinogen degradation through disruption of long-range electrostatic interactions. Sci Rep 16, 8937 (2026). https://doi.org/10.1038/s41598-026-40633-0
Palabras clave: pancreatitis crónica, quimotripsina C, tripsinógeno, variante genética, enzimas digestivas