Clear Sky Science · es
La unión de baja afinidad del anticuerpo anti-B7-H3 clon MJ18 a B7-H3 murino no consigue inducir la regresión tumoral
Por qué esto importa para la investigación del cáncer
La inmunoterapia del cáncer a menudo depende de anticuerpos: proteínas fabricadas en el laboratorio diseñadas para adherirse a las células tumorales y ayudar al sistema inmune a destruirlas. Un objetivo prometedor es una molécula llamada B7-H3, abundante en muchos cánceres humanos pero escasa en tejidos sanos. Este artículo examina con rigor un anticuerpo de uso extendido en investigación, MJ18, que se suponía bloqueaba B7-H3 en estudios murinos. Los autores encuentran que MJ18 apenas se adhiere a su blanco previsto y no ralentiza el crecimiento tumoral, lo que plantea dudas sobre cómo deben interpretarse experimentos animales previos que utilizaron esta herramienta.
La promesa de una “bandera” tumoral
B7-H3 ha atraído gran interés porque actúa como un escudo molecular: los tumores ricos en esta proteína suelen tener menos células inmunes agresivas en su interior y se asocian con peores resultados clínicos. En varios modelos murinos, eliminar el gen de B7-H3 en las células tumorales desata una respuesta inmune más potente y puede hacer que los tumores se encojan o desaparezcan. Estas observaciones han impulsado esfuerzos para desarrollar fármacos, células inmunes modificadas y conjugados anticuerpo-fármaco que se dirigen a B7-H3 en cánceres humanos. Sin embargo, el modo preciso en que B7-H3 atenúa la inmunidad —e incluso a qué receptor se une en las células inmunes— sigue siendo incierto, especialmente porque las versiones murina y humana de B7-H3 difieren estructuralmente.
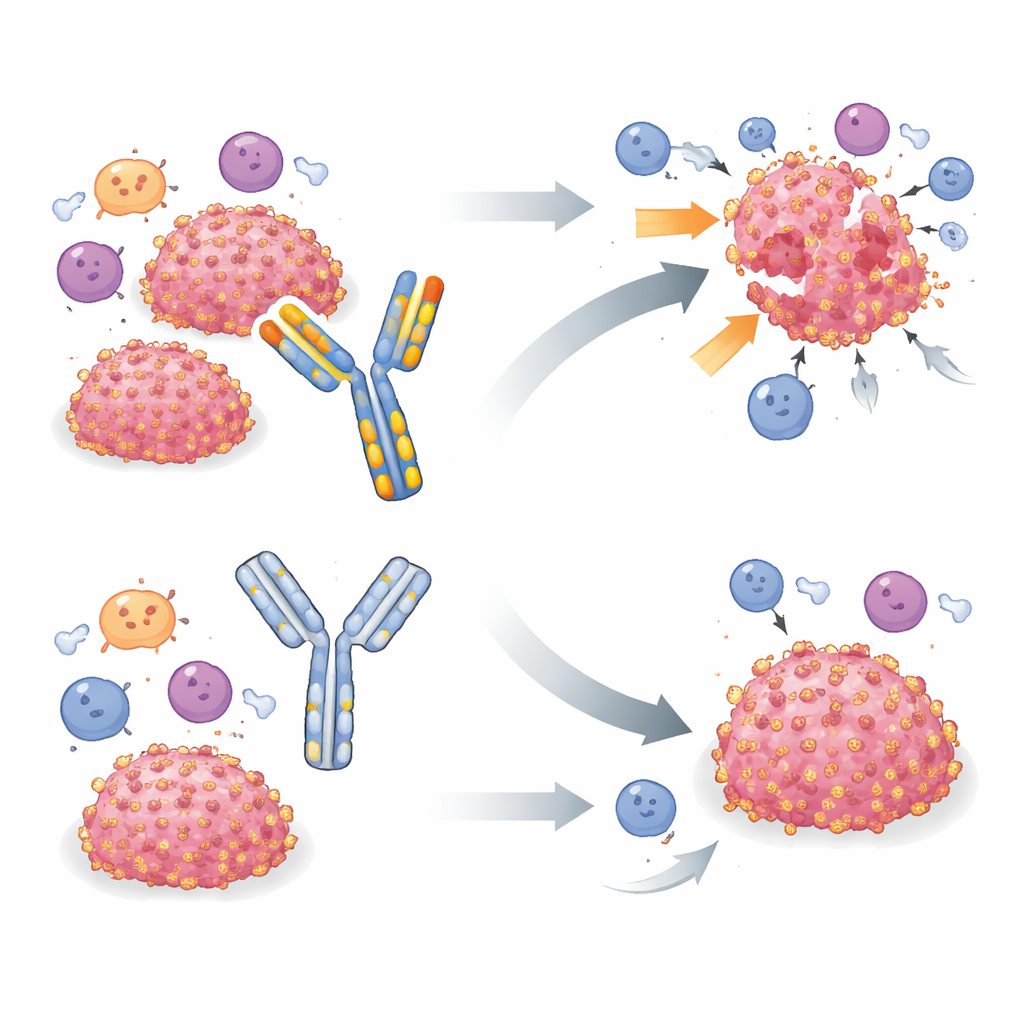
Una herramienta de uso habitual bajo la lupa
Para estudiar B7-H3 en ratones vivos, muchos grupos han confiado en un único anticuerpo derivado de rata llamado MJ18, que se informó reconocer B7-H3 murino y bloquear su actividad inmunosupresora. Estudios anteriores con MJ18 en varios modelos de enfermedad, incluidos cánceres, a menudo reportaron crecimiento tumoral más lento y mejor supervivencia. El equipo actual probó inicialmente MJ18 en un modelo murino de rabdomiosarcoma, un cáncer infantil de tejidos blandos en el que B7-H3 ya se había señalado como un mecanismo de escape importante. Cuando MJ18 no mejoró el control tumoral, los investigadores ampliaron las pruebas a otros dos tipos tumorales B7-H3 positivos —cánceres pancreático y mamario— que son claramente sensibles a la eliminación del gen B7-H3. En los tres modelos, la eliminación de B7-H3 en las células tumorales retrasó o eliminó de forma robusta los tumores, pero tratar a los ratones con MJ18 en dosis y esquemas similares a los de la literatura no tuvo impacto detectable sobre el crecimiento tumoral ni la supervivencia.
Comprobar si MJ18 realmente acierta su blanco
Los autores plantearon entonces una pregunta básica que sorprendentemente nunca se había abordado de forma rigurosa: ¿MJ18 se une realmente a B7-H3 murino, y con qué fuerza? Usando citometría de flujo compararon MJ18 con otro anticuerpo, EPNCIR122, que se sabía detectaba B7-H3. En varias líneas celulares tumorales murinas, EPNCIR122 produjo una señal clara que desapareció cuando se eliminó el gen B7-H3, confirmando su especificidad. MJ18, en cambio, no mostró una unión convincente incluso a alta concentración. Al examinar células inmunes del bazo, MJ18 sí se unió, pero el patrón no coincidía con B7-H3, y EPNCIR122 no detectó B7-H3 en esas células, lo que sugiere que MJ18 se estaba ligando a otra cosa.
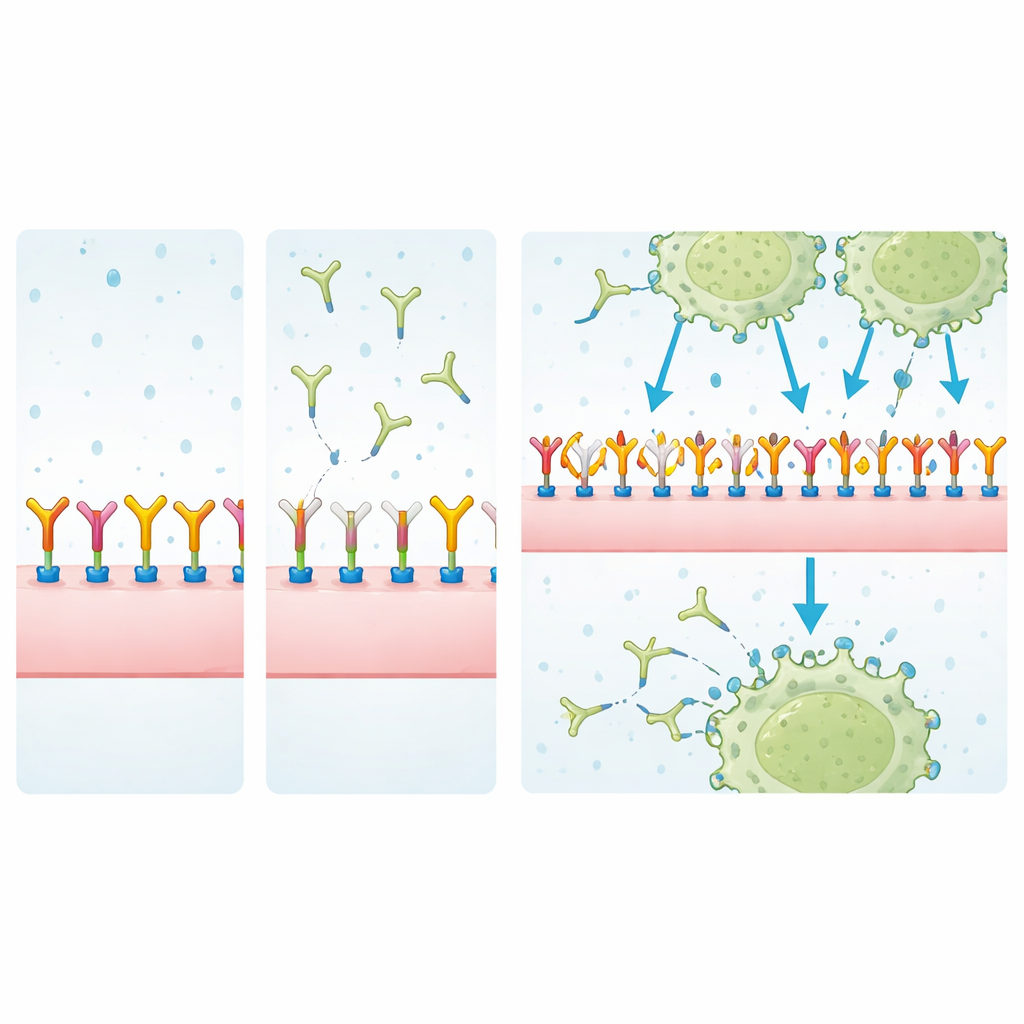
Indagando en las proteínas unidas
Para identificar qué podría reconocer realmente MJ18, los investigadores precipitaron proteínas de la superficie celular usando MJ18 o EPNCIR122 y las analizaron mediante espectrometría de masas, filtrando los contaminantes habituales. En células tumorales, EPNCIR122 enriqueció fuertemente B7-H3 frente a otras proteínas, confirmando que es un reactivo altamente específico. MJ18, sin embargo, precipitó una mezcla de proteínas en la que B7-H3 aparecía sólo débilmente y a niveles similares a los de uniones no específicas. Mediciones por resonancia plasmonónica de superficie, una técnica sensible para cuantificar interacciones moleculares, dejaron el punto claro: la afinidad de MJ18 por B7-H3 murino fue aproximadamente 7.000 veces menor que la de EPNCIR122 —muy por debajo de lo típico en anticuerpos terapéuticos.
Cuando los anticuerpos son captados por las células equivocadas
La historia no terminó con una unión débil. En células del bazo, pruebas adicionales mostraron que MJ18 y anticuerpos de rata similares eran reconocidos por receptores Fc murinos —moléculas en células inmunes que se unen de forma natural a la cola de los anticuerpos. Bloquear estos receptores redujo drásticamente la señal de MJ18, lo que implica que gran parte de su aparente unión provenía de que las propias células inmunes captaban el anticuerpo, en lugar de que MJ18 reconociera un proteinario específico en la superficie celular. Los intentos por identificar un socio proteico único para MJ18 en células inmunes sólo arrojaron candidatos a niveles indistinguibles del ruido de fondo. En conjunto, los datos sugieren que MJ18 se comporta mayormente como un anticuerpo de baja afinidad y no específico, cuyas interacciones están dominadas por el compromiso con receptores Fc más que por un reconocimiento preciso de B7-H3.
Qué significa esto de cara al futuro
Para los no especialistas, la conclusión es sencilla: aunque B7-H3 sigue siendo un blanco atractivo en muchos cánceres, el anticuerpo MJ18 no es un dardo fiable. Se une a B7-H3 en ratones sólo débilmente y no reproduce el control tumoral potente que se observa al eliminar el gen B7-H3. Estudios murinos previos que reportaron beneficios dramáticos con MJ18 pueden por tanto reflejar otros efectos —como cómo la cola del anticuerpo interactúa con los receptores de células inmunes— más que un bloqueo real de B7-H3. Los autores sostienen que el campo necesita con urgencia anticuerpos bien validados y de alta afinidad contra B7-H3 murino, y que los investigadores deberían confirmar de forma rutinaria la especificidad y la fuerza de tales herramientas. Sólo con reactivos fiables podrán confiarse las conclusiones de los modelos animales para guiar el desarrollo de terapias dirigidas a B7-H3 de nueva generación para pacientes.
Cita: Gulyás, D., Nammor, T., Frizzell, J. et al. Low-affinity binding of anti-B7-H3 clone MJ18 to murine B7-H3 fails to induce tumor regression. Sci Rep 16, 9519 (2026). https://doi.org/10.1038/s41598-026-40628-x
Palabras clave: B7-H3, inmunoterapia del cáncer, validación de anticuerpos, puntos de control inmunitario, modelos tumorales