Clear Sky Science · es
Análisis teórico de la supresión optogenética de potenciales de acción en cardiomiocitos ventriculares humanos expresando canalrhodopsinas selectivas para potasio mediante baja potencia
Una forma más suave basada en luz para calmar un corazón acelerado
Los ritmos cardíacos rápidos y caóticos pueden provocar desmayos, ictus o muerte súbita. Los tratamientos actuales—fármacos potentes, desfibriladores implantados o descargas de alta energía—pueden salvar vidas pero también resultar dolorosos e imprecisos. Este estudio explora una idea muy distinta: usar destellos tenues de luz y proteínas especialmente diseñadas para empujar silenciosamente a las células cardíacas hacia un ritmo seguro y estable, empleando mucha menos energía que los enfoques actuales.
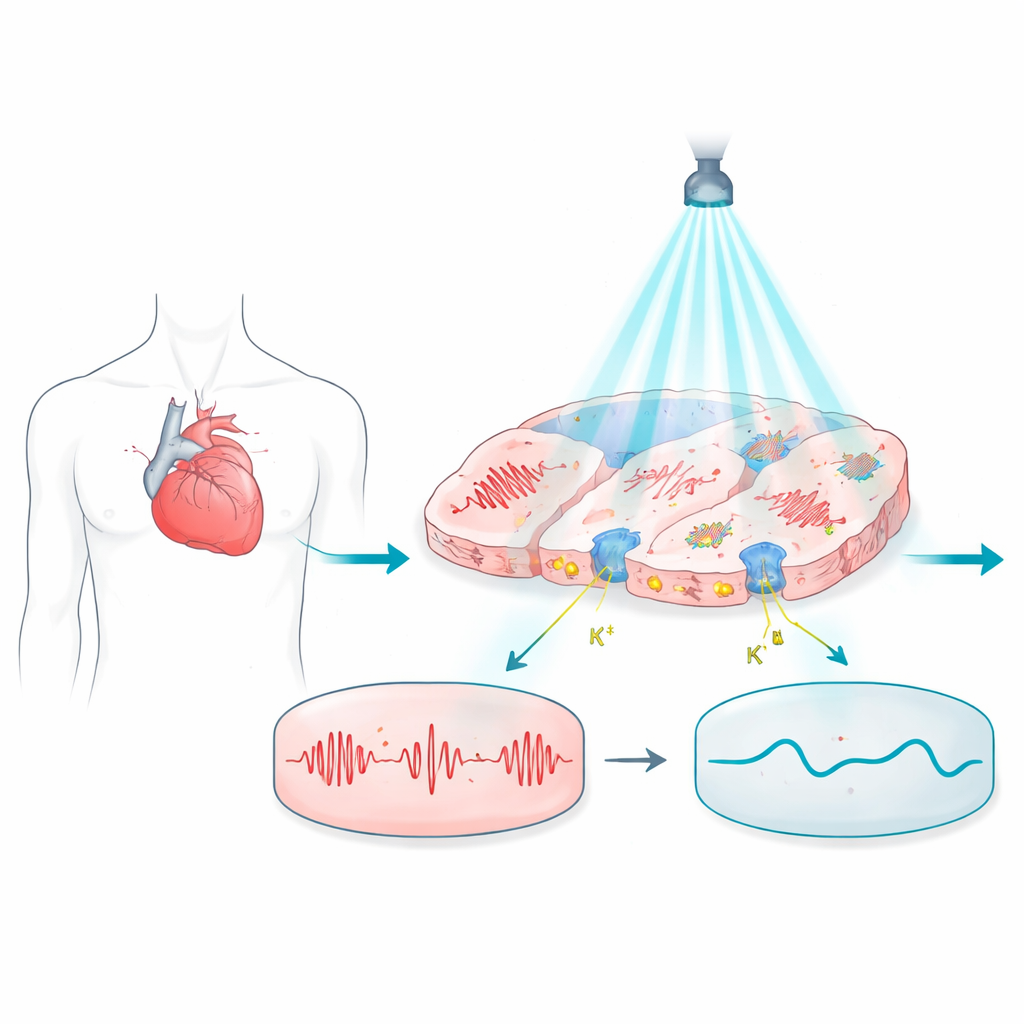
Iluminando los latidos problemáticos
El trabajo se basa en la optogenética, una técnica en la que las células se dotan de proteínas fotosensibles para que su actividad eléctrica pueda controlarse mediante destellos de luz. En el corazón, estas proteínas podrían en principio sustituir electrodos metálicos, ofreciendo control sin contacto y sin dolor. Pero la mayoría de las proteínas activadas por luz usadas hasta ahora tienden a llevar el voltaje de la célula hacia arriba, hacia un estado excitado, lo que dificulta mantener las células en reposo o ajustar con precisión la duración de cada latido. Eso limita su utilidad para apagar con seguridad ritmos peligrosos o corregir trastornos eléctricos que dependen de un temporizado sutil.
Nuevos interruptores luminosos afinados al “ajuste de reposo” del corazón
Proteínas recién descubiertas llamadas canalrhodopsinas selectivas para potasio, incluidas WiChR y HcKCR1, prometen corregir este desajuste. A diferencia de proteínas más antiguas que dejan pasar una mezcla de iones, estos canales prefieren fuertemente el potasio y atraen de forma natural el voltaje celular hacia el mismo nivel negativo que adopta en reposo. Los autores construyeron modelos computacionales detallados de células ventriculares humanas que expresan estos nuevos canales y los compararon con dos opsinas bien conocidas y más excitatorias, ChR2(H134R) y ChRmine. Al simular cómo responden estas células a diferentes colores e intensidades de luz, pudieron explorar de forma segura condiciones que serían difíciles o lentas de probar en corazones reales.
Luz suave, control contundente
Las simulaciones muestran que los canales selectivos para potasio ofrecen un control mucho más económico y estable. WiChR, en particular, podría bloquear por completo los potenciales de acción—los breves picos eléctricos que desencadenan cada latido—empleando intensidades de luz cientos a miles de veces menores que las necesarias para muchas herramientas anteriores. Bajo luz continua, WiChR y HcKCR1 mantuvieron el voltaje celular cerca de su nivel de reposo habitual, sosteniendo efectivamente a la célula en un estado tranquilo y seguro. En contraste, ChR2 y ChRmine tendieron a empujar el voltaje hacia valores más positivos, a veces bloqueando la actividad pero solo después de forzar a la célula a un estado estresado y sobreexcitado. WiChR también funcionó bien con pulsos breves de luz, impidiendo de forma fiable los picos celulares latido tras latido, lo que sugiere que podría seguir el ritmo de arritmias rápidas sin sobrecalentar el tejido ni desperdiciar energía.
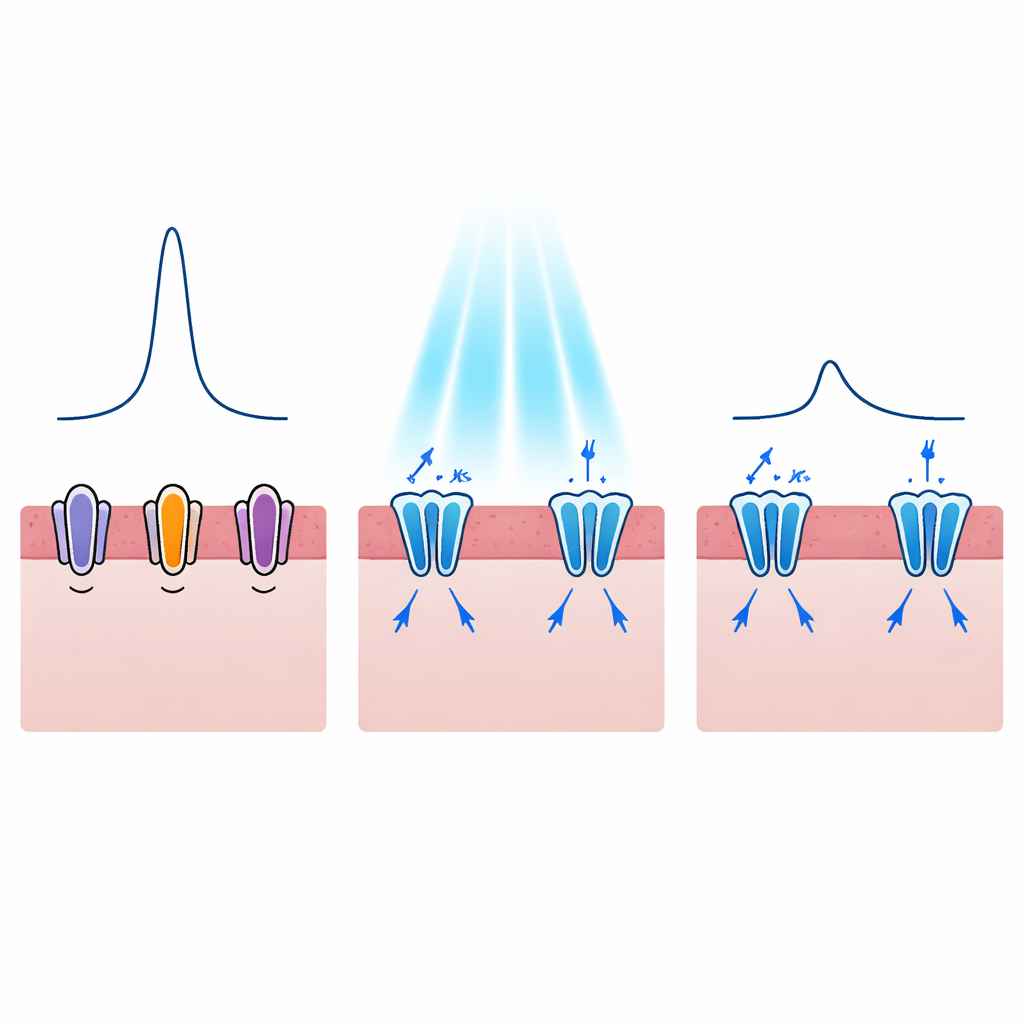
Reconfigurar cada latido, no solo detenerlo
Las arritmias peligrosas suelen relacionarse no solo con si una célula cardíaca dispara, sino también con cuánto tiempo permanece excitada. En trastornos como el síndrome de QT largo, el pulso eléctrico de cada latido se alarga, aumentando la probabilidad de derivar hacia ritmos letales. Los autores se preguntaron por tanto si los canales de potasio activados por luz podrían acortar ese pulso de manera controlada. Sus modelos mostraron que activar WiChR o HcKCR1 durante la fase de meseta del potencial de acción generó corrientes salientes de potasio fuertes que hicieron que el voltaje regresara antes. Al aumentar la intensidad lumínica, la duración del pulso eléctrico se redujo desde aproximadamente 300 milisegundos hasta cerca de la mitad, y este efecto podía lograrse incluso con destellos de luz muy cortos. WiChR tendió a producir periodos de calma más duraderos, mientras que HcKCR1 ofrecía una recuperación más rápida una vez apagada la luz, lo que sugiere distintos usos clínicos potenciales.
De modelos computacionales a terapias futuras
En conjunto, el estudio concluye que los canales fotoactivables selectivos para potasio, especialmente WiChR, son herramientas prometedoras para un control cardíaco suave y de baja potencia. Pueden tanto silenciar la actividad eléctrica desbocada como acortar latidos excesivamente largos, manteniendo el voltaje celular cercano a su estado natural de reposo. Aunque los resultados proceden de simulaciones detalladas de una sola célula y no de experimentos en corazones enteros, proporcionan orientación cuantitativa sobre cuánta luz podría necesitarse, cuándo aplicarla y qué variantes proteicas son más adecuadas para distintos fines. A largo plazo, esta línea de trabajo apunta a un futuro en el que los cardiólogos podrían usar haces de luz finamente ajustados, en lugar de descargas dolorosas, para prevenir o detener arritmias potencialmente mortales.
Cita: Dixit, N., Pyari, G. & Roy, S. Theoretical analysis of low-power optogenetic suppression of action potentials in human ventricular cardiomyocytes expressed with potassium-selective channelrhodopsins. Sci Rep 16, 9765 (2026). https://doi.org/10.1038/s41598-026-40578-4
Palabras clave: optogenética cardíaca, supresión de arritmias, canalrhodopsinas de potasio, duración del potencial de acción, síndrome de QT largo