Clear Sky Science · es
Sexado in ovo y genotipado mediante técnicas de PCR: una aportación a los principios 3R en la cría de pollos
Por qué importa lo que ocurre dentro de un huevo
Cada año, millones de pollitos macho son sacrificados poco después de la eclosión porque no sirven para la producción de huevos. Al mismo tiempo, laboratorios de investigación de todo el mundo nacen más animales de los que realmente necesitan, simplemente porque no pueden determinar el sexo o la composición genética de un embrión con suficiente antelación. Este estudio presenta una manera práctica de “leer” el sexo y los genes de un pollito mientras todavía se desarrolla dentro del huevo, usando pruebas de ADN estándar. Al hacerlo de forma temprana y delicada, el método pretende evitar la eclosión de animales sobrantes y reducir el sufrimiento, sin requerir equipos industriales costosos.
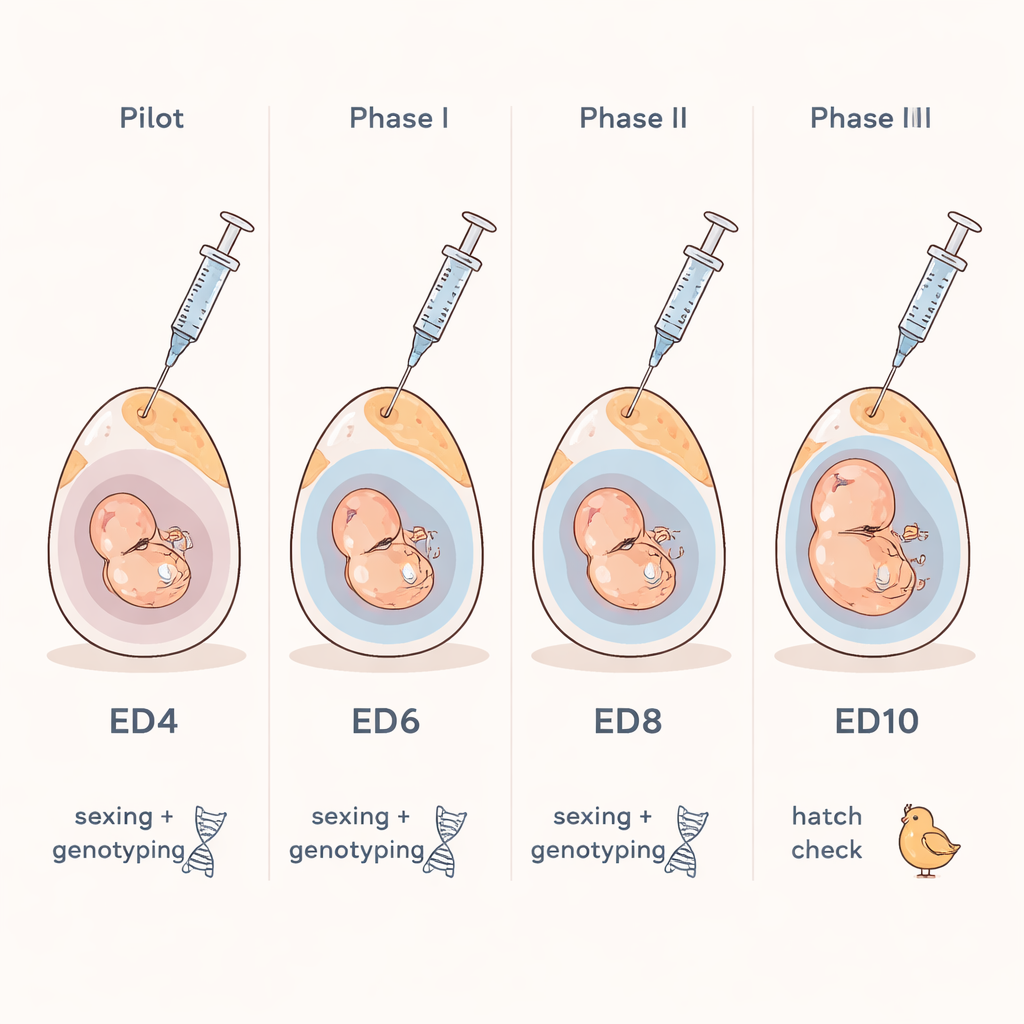
Mirar dentro del huevo sin abrirlo
Los investigadores se centraron en una pregunta sencilla: ¿podemos tomar de forma segura una pequeña muestra de fluido de un huevo fecundado y usarla para identificar el sexo del embrión y rasgos genéticos clave? Se basaron en un concepto familiar de la medicina humana, donde los médicos analizan fluidos alrededor de un feto para buscar condiciones genéticas. En las gallinas, una fina bolsa llena de líquido llamada alantoides se forma alrededor del embrión a medida que crece. Para el día siete de incubación, esta bolsa contiene suficiente fluido como para que una aguja fina pueda llegar a ella sin tocar el propio embrión. El equipo usó una luz intensa para localizar el espacio de aire en el extremo romo del huevo, hizo un orificio del tamaño de una aguja en la cáscara y extrajo solo unas pocas gotas de fluido con una jeringa diminuta.
De unas pocas gotas a una huella genética
El líquido extraído de huevos en etapas tempranas del desarrollo contiene solo cantidades mínimas de ADN. Para sortear esto, los científicos primero amplificaron todo el material genético de cada muestra, creando muchas copias sin cambiar su contenido. Luego aplicaron dos pruebas de laboratorio rutinarias: una reacción en cadena de la polimerasa (PCR) estándar y una variante llamada Kompetitive Allele Specific PCR (KASP). Ambas pruebas pueden distinguir entre los cromosomas sexuales de pollos machos y hembras y también detectar marcadores genéticos específicos, como la mutación que causa cáscaras de huevo azules o la presencia de un gen insertado en líneas de investigación especializadas. En más de 800 huevos de varias razas —incluyendo ponedoras comerciales, cruzas de Araucana de colores y una línea de investigación genéticamente modificada— estos métodos produjeron identificaciones correctas en aproximadamente el 92–100% de los casos.
Encontrar el momento más seguro para muestrear
Muestrear demasiado pronto corre el riesgo de dañar estructuras frágiles que son vitales para el embrión, mientras que muestrear demasiado tarde deja poco tiempo para actuar según los resultados. Para precisar la ventana ideal, el equipo primero crió embriones en cultivo sin cáscara para observar cómo se expanden las membranas y los espacios fluidos con el tiempo. Luego realizaron una serie de ensayos escalonados en huevos intactos. Se podía recoger fluido a partir del día cuatro, pero las tasas de éxito para las pruebas de ADN eran más bajas en esos días tempranos y el procedimiento era técnicamente más difícil. Al comparar las tasas de eclosión entre huevos perforados y controles intactos, encontraron que el día siete ofrecía el mejor equilibrio: había bastante líquido alantoideo claro, las pruebas de ADN funcionaban de forma fiable y la mayoría de los embriones sobrevivían hasta la eclosión. En ese punto aún hay varios días antes del probable inicio de la percepción del dolor en el embrión de pollo, lo que proporciona un margen ético para tomar decisiones.
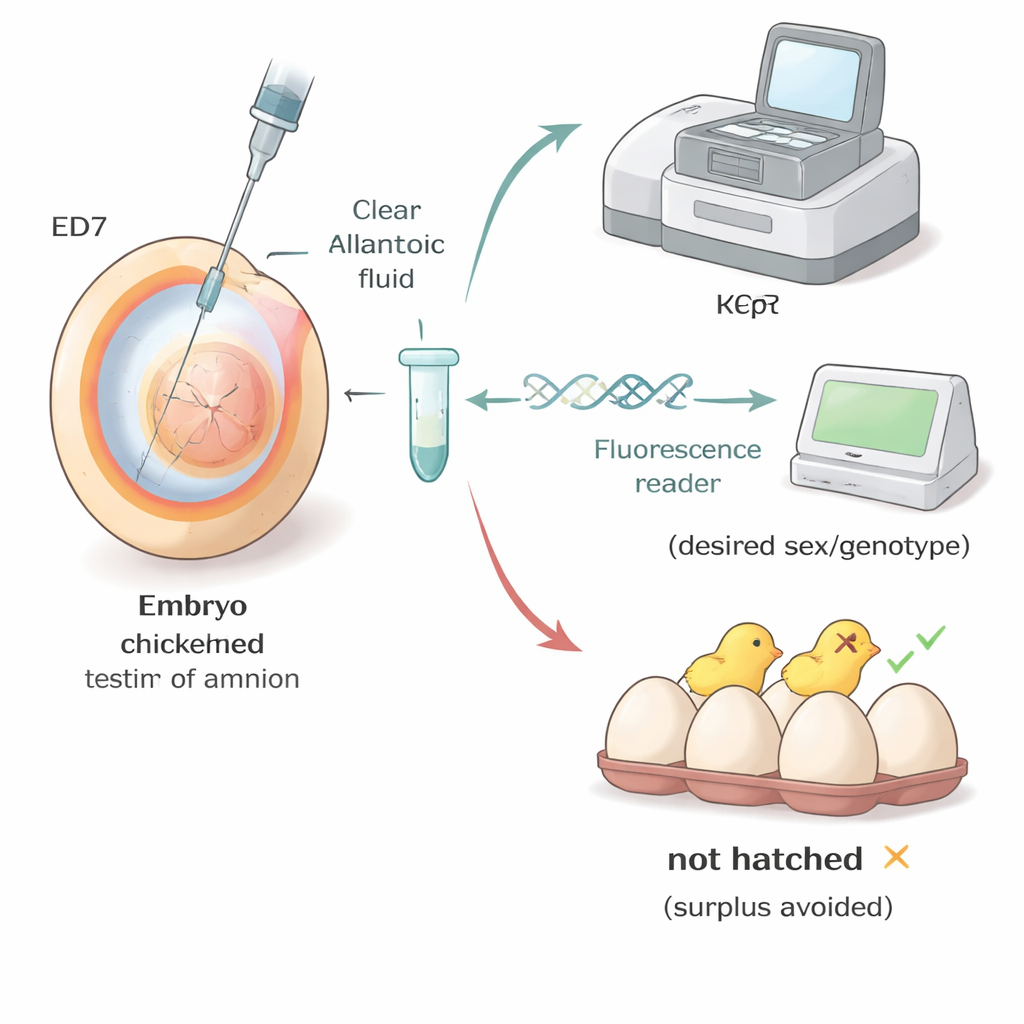
Poner el método en práctica en rebaños reales
Los investigadores probaron su flujo de trabajo en condiciones similares a las de instalaciones de cría y laboratorios universitarios. En líneas comerciales de ponedoras marrones y blancas, los huevos muestreados entre los días cuatro y siete mostraron que la eclosión generalmente mejoraba cuando el muestreo se realizaba más tarde, con los mejores resultados de nuevo en el día siete. En una línea especializada de “huésped sustituto” utilizada para genética avanzada, el equipo fue un paso más allá: sexaron y genotiparon embriones en el día siete y luego eligieron solo aquellos con la combinación de sexo y genética deseada para continuar hasta la eclosión. Casi todos los embriones seleccionados eclosionaron como pollitos saludables que crecieron según lo esperado, demostrando que la selección temprana puede reducir drásticamente el número de animales no deseados sin comprometer la calidad de los pollitos.
Qué implica esto para el bienestar animal y la investigación
Para un no especialista, el mensaje central es claro: con un pinchazo y herramientas de laboratorio rutinarias, ahora es posible saber, mientras el pollito todavía está dentro del huevo y de forma segura, si es macho o hembra y si porta determinados rasgos genéticos. El estudio muestra que realizar esto alrededor del día siete de incubación es tanto técnicamente fiable como lo suficientemente delicado como para que la mayoría de los embriones sobrevivan. Al permitir que los embriones no deseados sean retirados antes de que probablemente sean capaces de sentir dolor, el enfoque respalda los principios 3R ampliamente aceptados: reemplazar, reducir y refinar el uso de animales en la ciencia. Para incubadoras y laboratorios de investigación por igual, esta técnica ofrece una vía realista hacia menos animales sobrantes, un mejor uso de los recursos y estándares de bienestar más altos, sin necesidad de máquinas industriales complejas.
Cita: Dierks, C., Förster, A., Meunier, D. et al. In ovo sexing and genotyping using PCR techniques: a contribution to the 3R principles in chicken breeding. Sci Rep 16, 7464 (2026). https://doi.org/10.1038/s41598-026-40562-y
Palabras clave: embrión de pollo, sexado in ovo, genotipado por PCR, bienestar animal, principios 3R