Clear Sky Science · es
Niveles sanguíneos de MMP-7 y TNF-α como posibles biomarcadores pronósticos para la histiocitosis de células de Langerhans pulmonar en adultos
Por qué importa esto para las personas que fuman
La histiocitosis de células de Langerhans pulmonar (HCLP) es una enfermedad pulmonar rara que casi siempre afecta a fumadores activos, a menudo en la plenitud de la vida. Algunos pacientes se mantienen relativamente bien durante años, mientras que otros pierden rápidamente función pulmonar y pueden desarrollar problemas respiratorios graves. Actualmente los médicos no disponen de una forma sencilla de saber, en el momento del diagnóstico, qué trayectoria seguirá cada paciente. Este estudio plantea si un análisis de sangre de rutina podría ofrecer una advertencia temprana sobre quiénes tienen más probabilidad de que sus pulmones se deterioren.
Una enfermedad pulmonar rara con dos trayectorias distintas
La HCLP se caracteriza por conglomerados de células inmunitarias anómalas que invaden y dañan las pequeñas vías aéreas, creando cicatrices y quistes por todo el pulmón. Trabajos previos en una amplia cohorte francesa mostraron que la mayoría de los pacientes siguen una trayectoria “estable”: su capacidad pulmonar, medida por el volumen espiratorio forzado en un segundo (FEV1), comienza cerca de lo normal y se mantiene bastante constante con el tiempo. Un grupo menor comienza con un FEV1 más bajo y continúa empeorando año tras año, enfrentando mayores riesgos de insuficiencia respiratoria y muerte. El problema es que, en el momento del diagnóstico, las características clínicas habituales no distinguen de forma fiable entre estos dos grupos. Por ello, los autores se centraron en moléculas circulantes en sangre que podrían reflejar lo que ocurre en lo profundo de los pulmones.
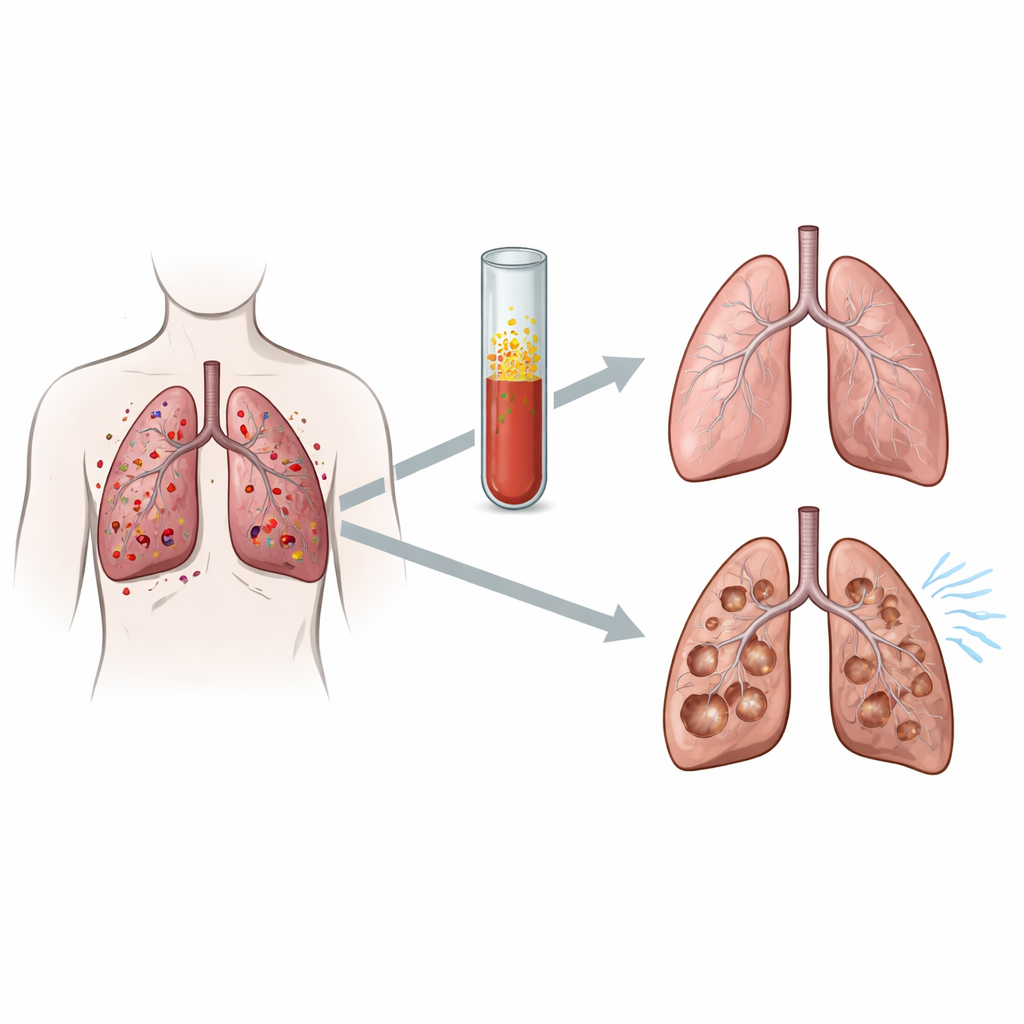
Observando más de cerca las señales en sangre
Los investigadores recurrieron a un registro nacional de adultos con HCLP en Francia. De esta cohorte más amplia, se centraron en 25 pacientes que tenían muestras de sangre almacenadas en el momento del diagnóstico y cuyo tabaquismo, edad y sexo podían emparejarse. Nueve de estos pacientes mostraron posteriormente un descenso sostenido del FEV1 durante varios años, mientras que 16 mantuvieron una función pulmonar estable. Usando inmunoensayos multiplex —pruebas de laboratorio que pueden medir muchas sustancias a la vez— evaluaron los niveles de 30 distintas moléculas implicadas en la inmunidad y en la remodelación tisular en cada muestra de sangre. Estas incluían mensajeros inflamatorios, quimioatrayentes para células inmunitarias, factores de crecimiento y enzimas capaces de degradar la estructura del tejido pulmonar.
Dos moléculas destacadas vinculadas a peor función pulmonar
Entre todos los mediadores analizados, dos moléculas sobresalieron claramente: el factor de necrosis tumoral alfa (TNF-α), una potente señal inflamatoria, y la metaloproteinasa de matriz-7 (MMP-7), una enzima que puede degradar componentes estructurales de los tejidos. Al diagnóstico, tanto TNF-α como MMP-7 fueron significativamente más altos en los pacientes que más tarde experimentaron una disminución del FEV1 que en aquellos cuya función pulmonar permaneció estable, incluso después de ajustar por edad, sexo e intensidad del tabaquismo. De manera importante, niveles más altos de MMP-7 al diagnóstico se relacionaron fuertemente con un FEV1 más bajo y una menor capacidad de transferencia de gases (DLCO) en ese mismo momento, lo que sugiere que esta enzima se corresponde con el grado de daño estructural pulmonar. TNF-α, aunque más elevado en el grupo en declive, no mostró una correlación tan estrecha con los valores numéricos de función pulmonar, lo que insinúa que puede reflejar una actividad global de la enfermedad más que una destrucción directa de las paredes de las vías aéreas.
De las lecturas sanguíneas a la predicción de riesgo
Para explorar si estos marcadores sanguíneos podrían ayudar a identificar a los pacientes en riesgo de declive futuro, el equipo utilizó herramientas estadísticas llamadas curvas ROC (de característica operativa del receptor). Identificaron valores umbral de MMP-7 y TNF-α que mejor separaban al grupo en declive del grupo estable. En particular, un nivel más alto de MMP-7 al diagnóstico se asoció con una buena probabilidad de que el paciente posteriormente perdiera función pulmonar, pero aún mejor fue la probabilidad de que los pacientes por debajo de ese umbral permanecieran estables. En otras palabras, una lectura baja de MMP-7 podría ser tranquilizadora, mientras que una lectura alta motivaría un seguimiento más estrecho y la consideración de un tratamiento temprano. Varios otros mensajeros inmunitarios mostraron diferencias sugerentes entre los grupos, pero el estudio fue demasiado pequeño para confirmar su relevancia.
Qué podría significar esto para los pacientes en el futuro
Este trabajo sugiere que una prueba de sangre simple que mida TNF-α y, sobre todo, MMP-7 podría algún día ayudar a los médicos a clasificar a los pacientes con HCLP en grupos de menor y mayor riesgo poco después del diagnóstico. Una herramienta así podría orientar la frecuencia del seguimiento, la intensidad con la que promover la cesación tabáquica y el momento de considerar terapias experimentales o dirigidas. Dado que el estudio incluyó solo a 25 pacientes, sus resultados son preliminares y necesitan confirmación en series más grandes. Aun así, los hallazgos representan un paso prometedor hacia una atención más personalizada en una enfermedad pulmonar rara relacionada con el tabaquismo, en la que la advertencia temprana del deterioro ha sido durante mucho tiempo una carencia.
Cita: Benattia, A., Porcher, R., Terry, S. et al. Blood MMP-7 and TNF-α levels as potential prognostic biomarkers for adult pulmonary Langerhans cell histiocytosis. Sci Rep 16, 10059 (2026). https://doi.org/10.1038/s41598-026-40540-4
Palabras clave: histiocitosis de células de Langerhans pulmonar, enfermedad pulmonar relacionada con el tabaquismo, biomarcadores sanguíneos, MMP-7, declive de la función pulmonar