Clear Sky Science · es
Nanotransportadores ferroso recubiertos de quitosano y sensibles a estímulos para la administración dirigida de capsaicina y bioactividad selectiva hacia HepG2 dependiente del núcleo
Una especia con un poder oculto
Los chiles aportan algo más que picante a la comida: su ardor proviene de la capsaicina, un compuesto natural que también puede eliminar células cancerosas. Sin embargo, usar capsaicina como medicamento ha resultado difícil porque se disuelve mal en agua, desaparece rápidamente del organismo y en dosis altas irrita tejidos sanos. Este estudio explora una forma de domar esa molécula ardiente alojándola dentro de partículas diminutas y “inteligentes” que pueden transportar la capsaicina de forma segura por la sangre y liberarla principalmente dentro de tumores hepáticos.
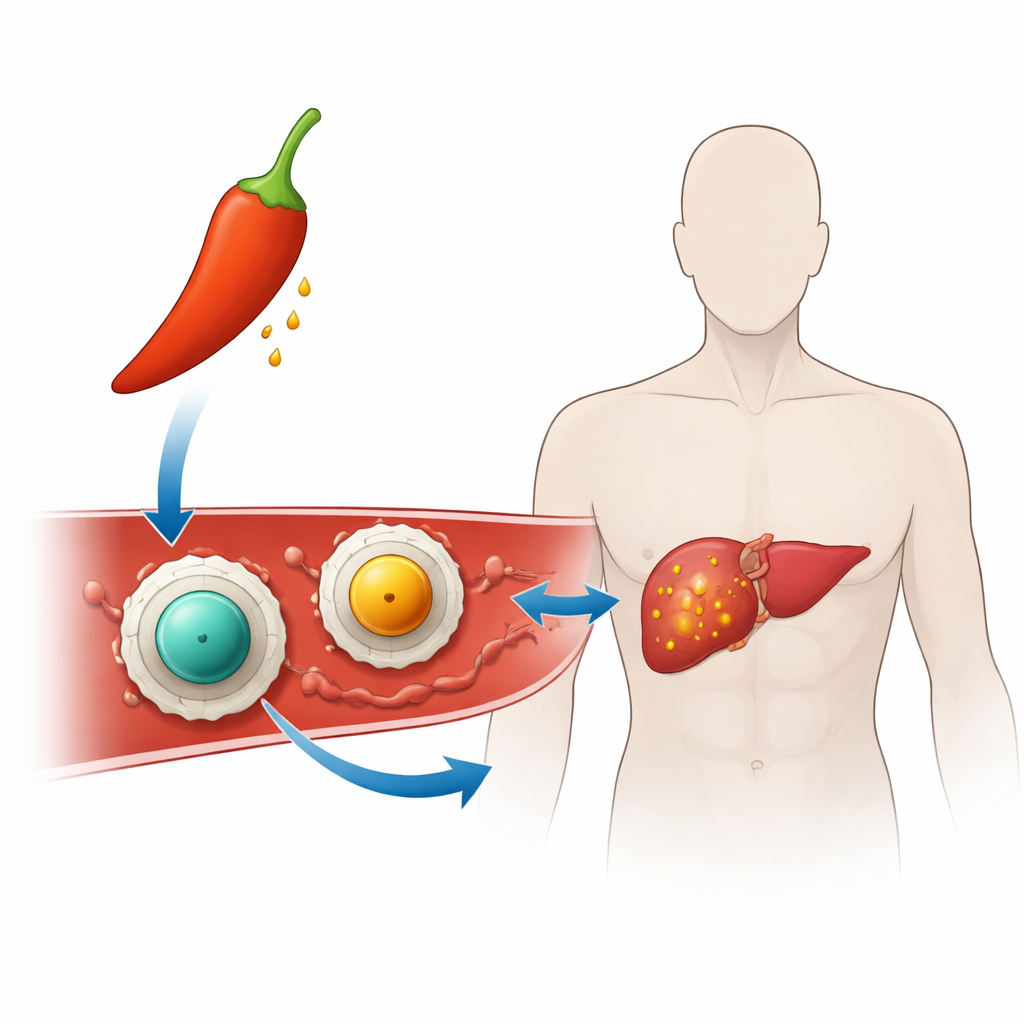
Convertir el chile en terapia dirigida
Los investigadores construyeron “nanotransportadores” – partículas miles de veces más pequeñas que un grano de arena – para llevar capsaicina hasta las células cancerosas. Cada nanotransportador tiene un núcleo sólido hecho de un mineral magnético llamado ferrita (bien ferrita de zinc o ferrita de manganeso) envuelto en una capa delgada de quitosano, una sustancia tipo azúcar derivada de crustáceos que ya se usa en productos médicos y alimentarios. Este recubrimiento facilita la suspensión de las partículas en agua y ayuda a que se adhieran a las superficies celulares y al ADN, algo importante para la acción anticancerígena. Al cargar la capsaicina en esta cáscara de quitosano, el equipo buscaba mantener el fármaco estable y oculto hasta que alcance el entorno agresivo dentro de un tumor.
Liberación inteligente en condiciones tumorales
Una característica clave de los tumores es que tienden a ser más ácidos y a tener más antioxidantes determinados, como el glutatión, que los tejidos sanos. El equipo diseñó sus nanotransportadores para detectar estas condiciones. En pruebas de laboratorio a pH sanguíneo normal, menos del 10 por ciento de la capsaicina almacenada se filtró en dos días, lo que sugiere que las partículas transportarían su carga de forma segura durante la circulación. En condiciones similares a las tumorales —más ácidas y con abundante glutatión—, las partículas liberaron alrededor de un tercio de su capsaicina. Este comportamiento de “encendido‑apagado” indica que el fármaco es más probable que se libere dentro de las células cancerosas en lugar de por el camino, lo que podría aumentar el beneficio y reducir los efectos secundarios.
Cómo los ingredientes de la partícula moldean seguridad y eficacia
Aunque los dos nanotransportadores parecían similares a simple vista, sus núcleos internos marcaron una gran diferencia. Las partículas a base de zinc tendían a ser más pequeñas y a retener la capsaicina con más fuerza, mientras que las de manganeso eran más porosas y permitían una liberación más fácil del fármaco. Ambos tipos tenían una carga superficial fuertemente positiva, lo que ayuda a interactuar con las superficies negativamente cargadas de células y ADN. Las pruebas con sangre humana mostraron muy pocos daños a los glóbulos rojos, y las partículas vacías fueron benignas para células pulmonares normales, lo que respalda su seguridad básica. Cuando se cargaron con capsaicina, ambos sistemas se volvieron más potentes contra células de cáncer hepático, pero la versión con manganeso logró el mejor equilibrio: dañó más intensamente a las células cancerosas mientras seguía siendo relativamente amable con las células normales.
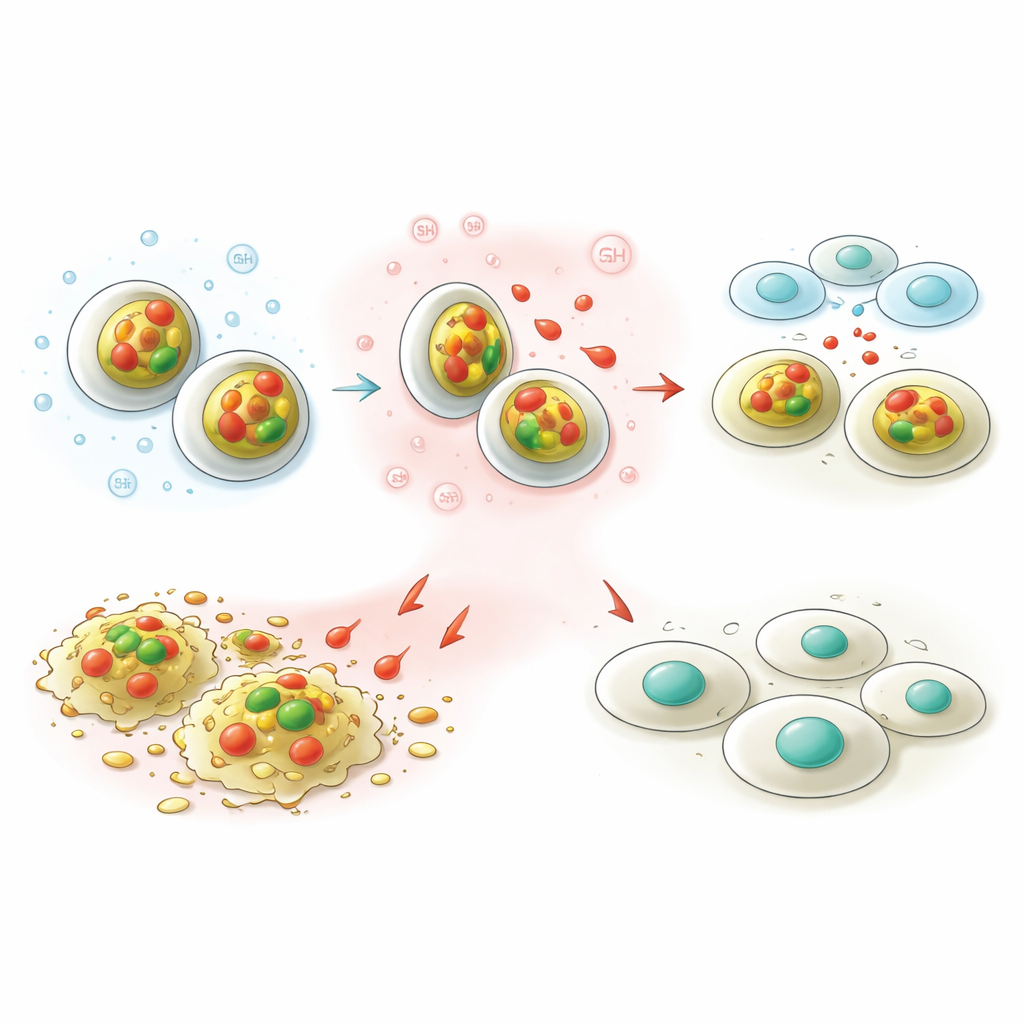
Más allá del cáncer: efectos protectores adicionales
Los nanotransportadores hicieron algo más que administrar capsaicina. También ralentizaron el crecimiento de varias bacterias patógenas con eficacia comparable a un antibiótico estándar en algunas pruebas, y ayudaron a neutralizar radicales libres nocivos, vinculados a la inflamación y el daño tisular. Medidas ópticas cuidadosas mostraron que, una vez que la capsaicina se empaquetó en las partículas ferrita‑quitosano, se unía al ADN con mayor fuerza y estabilidad. Experimentos cinéticos rápidos revelaron una interacción en dos pasos: el ADN primero se adhiere a la superficie positivamente cargada de la partícula y luego el complejo se reorganiza hacia una asociación más ajustada y duradera. Estas interacciones reforzadas probablemente ayudan a explicar por qué las partículas cargadas muestran efectos anticancerígenos, antibacterianos y antioxidantes más fuertes que la capsaicina o las partículas de ferrita por separado.
Qué podría significar esto para los pacientes
Por ahora, estos hallazgos proceden de cultivos de laboratorio, no de pacientes. Aun así, sugieren que nanotransportadores cuidadosamente diseñados pueden convertir un ingrediente picante en un arma contra el cáncer más precisa. Al elegir el material de núcleo y la cubierta adecuados, los investigadores crearon paquetes diminutos que mantienen la capsaicina estable, la transportan con seguridad en sangre y la descargan preferentemente en condiciones similares a las tumorales, especialmente en células de cáncer hepático. Entre los diseños probados, las partículas a base de manganeso ofrecieron la combinación más prometedora de efecto cancerígeno dirigido, bajo daño a células normales y beneficios antibacterianos y antioxidantes añadidos. Con más estudios en animales y de seguridad, esas partículas “inteligentes” inspiradas en el chile podrían algún día contribuir a terapias más suaves y específicas para el cáncer de hígado y potencialmente otras enfermedades.
Cita: Bakr, E., Elshami, F.I., Okba, E.A. et al. Stimuli-responsive chitosan-coated ferrite nanocarriers for targeted capsaicin delivery and core-dependent HepG2-selective bioactivity. Sci Rep 16, 8957 (2026). https://doi.org/10.1038/s41598-026-40433-6
Palabras clave: capsaicina, cáncer de hígado, nanopartículas, administración dirigida de fármacos, transportadores sensibles a estímulos