Clear Sky Science · es
MOV10, una inmunoterapia novedosa y biomarcador pronóstico, contribuye al desarrollo del glioma regulando la autofagia
Por qué importa este estudio sobre el cáncer cerebral
El glioblastoma, una forma agresiva de cáncer cerebral, es notoriamente difícil de tratar. La mayoría de los pacientes sobreviven solo meses tras el diagnóstico, incluso con cirugía, radiación y quimioterapia. Este estudio se centra en una sola molécula llamada MOV10 que está inusualmente activa en estos tumores. Al mostrar cómo MOV10 ayuda a las células cancerosas a crecer, evadir al sistema inmunitario y resistir la muerte, los investigadores identifican un nuevo posible objetivo para terapias más efectivas —y un marcador potencial para predecir el pronóstico de los pacientes.
Un aliado oculto de tumores cerebrales mortales
El equipo comenzó analizando grandes bases de datos públicas de cáncer que contienen información genética y clínica de cientos de personas con glioma, un grupo amplio de tumores cerebrales que incluye el glioblastoma. Encontraron que MOV10, una proteína implicada en el manejo del ARN dentro de las células, está activada a niveles más altos en tejidos de glioma que en el cerebro normal. Los pacientes cuyos tumores producían más MOV10 tendían a vivir menos tiempo, y esta relación se mantuvo aun al ajustar por edad, grado tumoral y características genéticas clave. Con estos factores, los investigadores construyeron un modelo matemático que muestra que los niveles de MOV10 pueden ayudar a predecir las probabilidades de supervivencia de un paciente, lo que sugiere que MOV10 podría servir como biomarcador pronóstico.
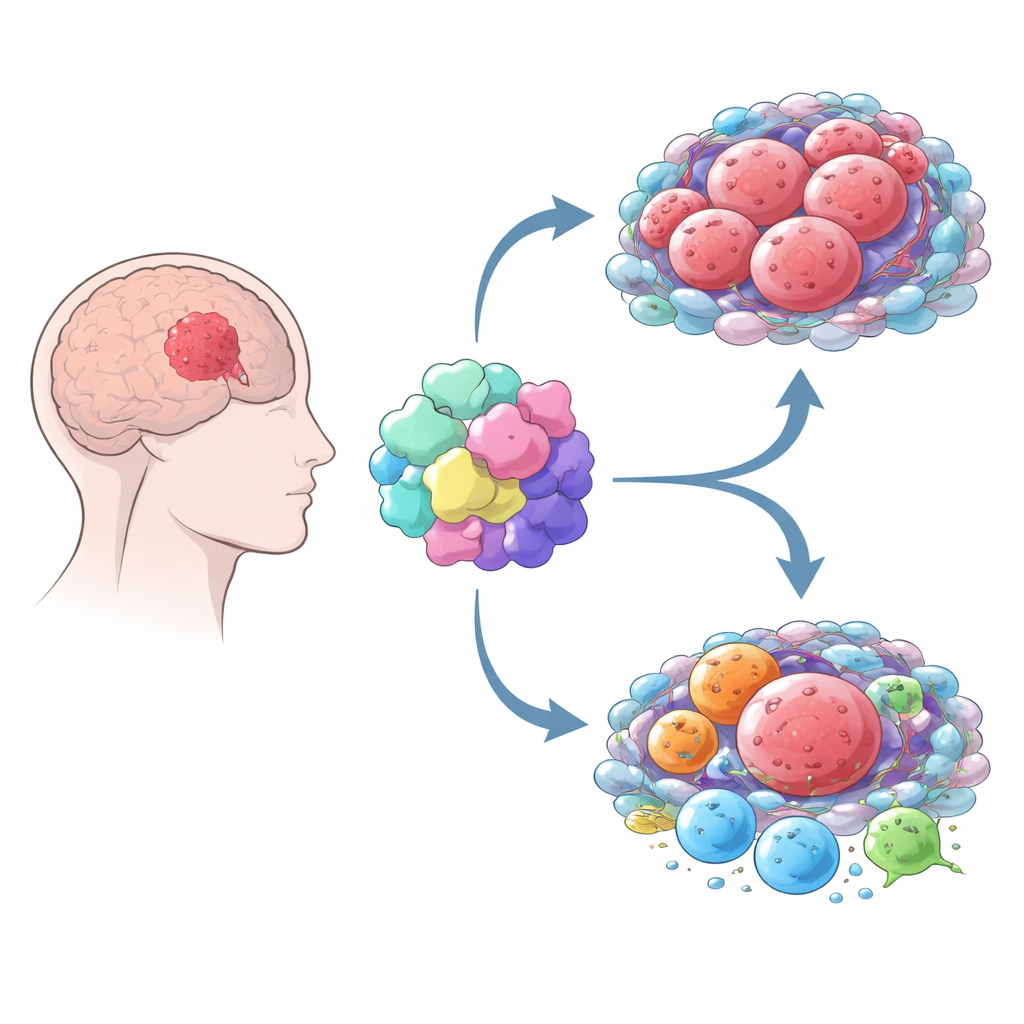
Cómo MOV10 remodela el vecindario tumoral
El cáncer no crece de forma aislada: incorpora al “vecindario” circundante de células inmunitarias y de sostén. Combinando varias herramientas computacionales, los autores mostraron que los gliomas con alto MOV10 están rodeados por una mezcla más rica de células inmunitarias y estromales que los tumores con bajo MOV10. Pero esto no es un ataque inmune eficaz. En lugar de ello, los tumores con alto MOV10 contienen más macrófagos, en particular un subtipo frecuentemente llamado M2, que típicamente apoya el crecimiento tumoral y calma las respuestas inmunitarias. Estos tumores también muestran firmas más fuertes de linfocitos T agotados y mayor actividad de los “frenos” inmunitarios que son dianas de fármacos inmunoterapéuticos populares, como PD-1 y CTLA-4. En conjunto, el patrón sugiere que MOV10 está vinculado a un ambiente inmunosupresor en el que las defensas del organismo están atenuadas.
De los macrodatos a las células en el laboratorio
Para ir más allá de las correlaciones, los investigadores examinaron MOV10 directamente en muestras de pacientes y en cultivos celulares. Confirmaron que MOV10 es más abundante en tejidos de glioma que en el cerebro normal, y que varias líneas celulares de glioma ampliamente usadas también muestran niveles altos. Cuando usaron pequeños ARN interferentes para reducir MOV10 en células de glioma cultivadas en placas, las células se dividieron más lentamente, formaron menos colonias y perdieron parte de su capacidad para moverse e invadir a través de membranas artificiales. Las proteínas que impulsan la progresión del ciclo celular y la invasión disminuyeron en abundancia, lo que respalda la idea de que MOV10 promueve activamente el comportamiento agresivo en lugar de ser un observador pasivo.
Relacionando MOV10 con células inmunitarias y vías de autorreciclaje
El estudio también exploró cómo MOV10 interactúa con dos procesos clave: el comportamiento de los macrófagos asociados al tumor y el propio sistema de “autolimpieza” celular conocido como autofagia. En muestras tumorales humanas, se encontró MOV10 en las mismas regiones que macrófagos de tipo M2. En un sistema de cocultivo, cuando las células de glioma fueron diseñadas para producir menos MOV10, menos macrófagos de tipo M2 migraron a través de una barrera hacia ellas, lo que implica que MOV10 en las células tumorales ayuda a atraer o sostener a estas células inmunitarias pro-tumorales. Al mismo tiempo, los análisis genéticos vincularon MOV10 con varios genes implicados en la autofagia. Usando marcadores fluorescentes que iluminan las estructuras de reciclaje celular, el equipo mostró que reducir MOV10 aumentó la actividad autofágica en células de glioma y desencadenó más muerte celular programada. Los cambios en proteínas clave de la autofagia y la apoptosis respaldaron estas observaciones.
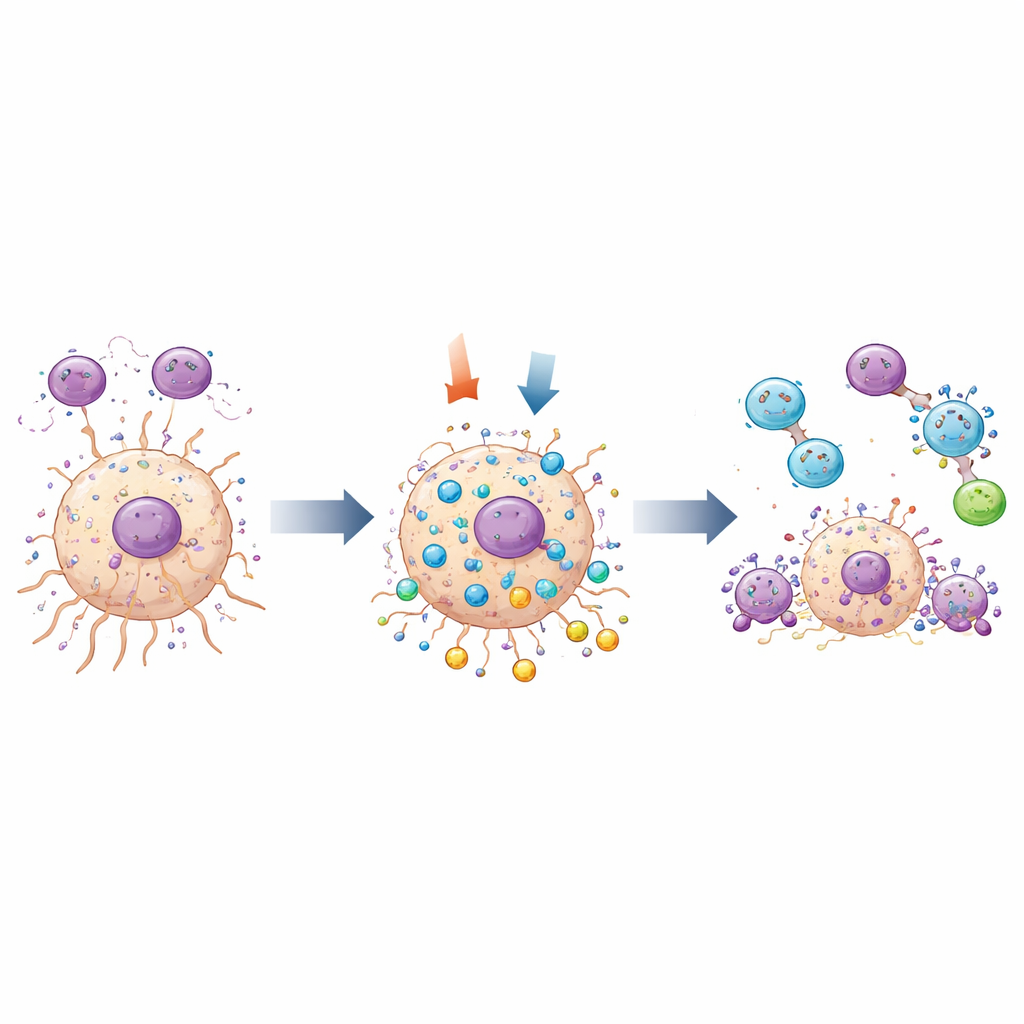
Qué implica esto para tratamientos futuros
En conjunto, los hallazgos pintan a MOV10 como un aliado polivalente del glioma: potencia el crecimiento y la invasión de las células tumorales, ayuda a construir un microambiente inmunosupresor rico en macrófagos que apoyan el tumor, y mantiene bajo control los sistemas de autodestrucción y reciclaje celular. Cuando MOV10 se silencia, las células de glioma crecen menos, mueren más fácilmente y parecen menos capaces de reclutar tipos de células inmunitarias dañinas. Para los no especialistas, el mensaje clave es que MOV10 es tanto un “termómetro” como un “interruptor”: su nivel en los tumores puede ayudar a pronosticar el curso de los pacientes, y reducirlo podría, en principio, hacer que los tumores cerebrales sean más vulnerables al tratamiento. Si bien se necesitan más estudios en animales y, eventualmente, ensayos clínicos, MOV10 destaca ahora como un objetivo prometedor en la búsqueda de mejores terapias contra uno de los cánceres cerebrales más letales.
Cita: Wang, F., Ruan, L., Yang, W. et al. MOV10, a novel immunotherapy and prognostic biomarker, contributes to glioma development by regulating autophagy. Sci Rep 16, 9501 (2026). https://doi.org/10.1038/s41598-026-40396-8
Palabras clave: glioblastoma, inmunoterapia de tumores cerebrales, proteína MOV10, microambiente tumoral, autofagia y apoptosis