Clear Sky Science · es
Splicing alternativo y expresión génica diferencial durante los cambios en la receptividad endometrial en pacientes con fallo de implantación recurrente
Por qué algunos embriones no se implantan
Muchas parejas sometidas a fecundación in vitro se enfrentan a un misterio frustrante: incluso cuando se transfieren embriones de alta calidad, puede no producirse embarazo. Este estudio examina de cerca el revestimiento del útero —el endometrio— para entender por qué algunas mujeres experimentan fallos de implantación repetidos. Al analizar cómo se activan y desactivan los genes, cómo se cortan y reordenan sus mensajeros y cómo se comportan las células inmunitarias durante la breve ventana en la que el útero está preparado para recibir un embrión, la investigación descubre nuevas pistas moleculares que podrían, en el futuro, orientar pruebas y tratamientos más precisos.
La breve ventana de acogida del útero
La implantación solo puede ocurrir durante un corto periodo de cada ciclo en el que el revestimiento uterino se vuelve “receptivo”. Los investigadores compararon muestras de tejido de 90 mujeres fértiles y 73 mujeres con fallo de implantación recurrente, todas tomadas en tres momentos clave: justo antes de que el endometrio se vuelva receptivo, durante la ventana receptiva y poco después de que se cierre. Mediante secuenciación masiva de ARN, midieron qué genes estaban activos y cómo se procesaban sus mensajes de ARN. Este diseño les permitió seguir cómo un revestimiento sano se prepara para un embrión y cómo esa preparación se altera en mujeres que fracasan repetidamente en implantar a pesar de tener buenos embriones. 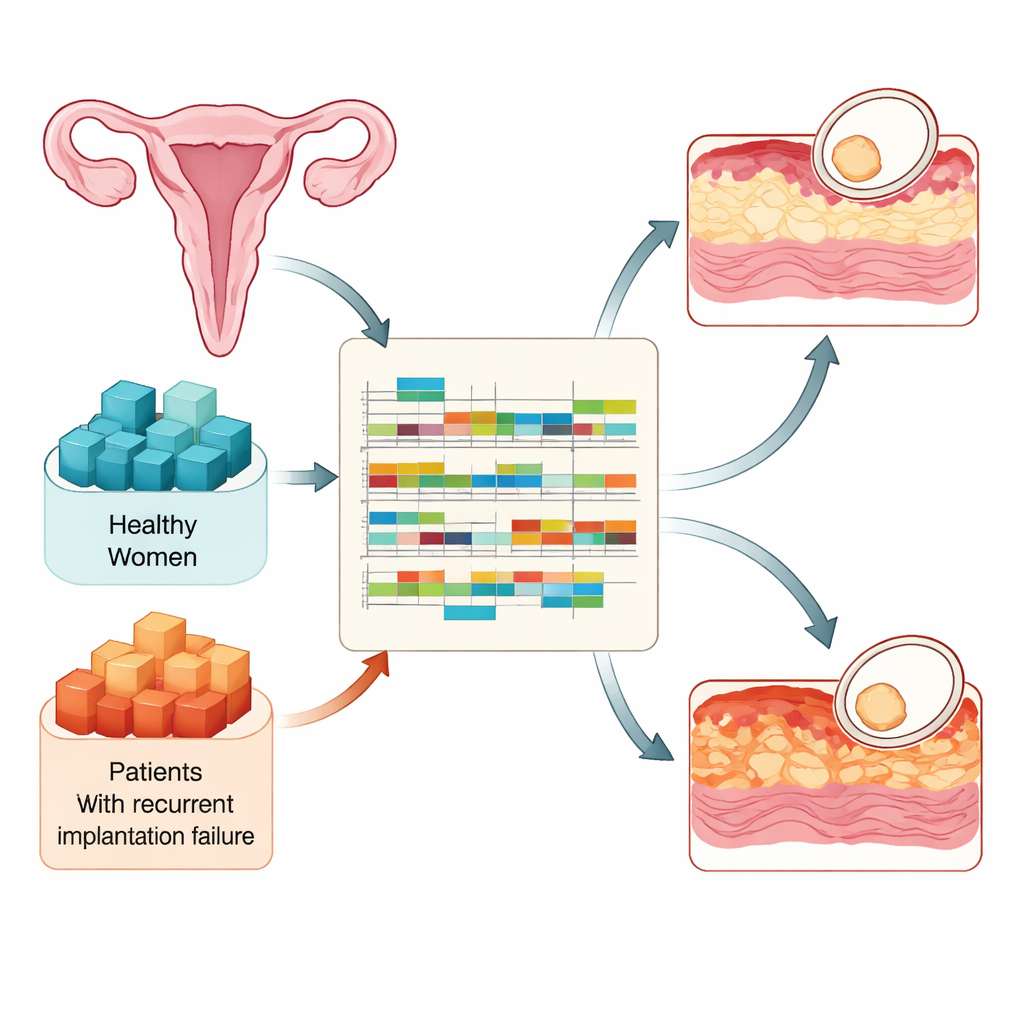
Mensajes genéticos cortados y reordenados
Más allá de simplemente contar cuánto está activo cada gen, el equipo se centró en el splicing alternativo —el proceso por el cual un único gen puede fragmentarse en distintas variantes de mensaje, dando lugar a formas proteicas diferentes. Encontraron más de un millón de eventos de splicing en las comparaciones, con dos tipos —la exclusión de segmentos completos y la elección entre segmentos mutuamente exclusivos— especialmente frecuentes. Cuando consideraron solo los cambios que eran a la vez frecuentes y estadísticamente sólidos, observaron desde cientos hasta miles de desplazamientos en el splicing a medida que el endometrio pasaba de la fase no receptiva a la receptiva, particularmente en la transición desde la etapa temprana (pre‑receptiva) hacia la ventana de implantación. Muchos de estos cambios se dieron incluso cuando la cantidad total del gen se mantenía igual, lo que significa que la forma de la proteína cambió sin una variación en la actividad génica global.
Células que se adhieren, se remodelan y se comunican con el sistema inmune
Los genes afectados por el splicing alterado y por cambios en la actividad estaban fuertemente implicados en cómo las células se adhieren entre sí, cómo se reorganiza su andamiaje interno y cómo envían y reciben señales inmunitarias. Estas funciones son cruciales cuando el revestimiento uterino se transforma de una barrera simple en una superficie capaz de acoger y anclar un embrión mientras remodela los vasos sanguíneos. En mujeres fértiles y en aquellas con fallo de implantación, la fase receptiva se caracterizó por una intensa remodelación en estas vías, pero las mujeres con fallo recurrente tendieron a exhibir cambios de splicing más frecuentes o con patrones distintos. Algunos de los genes implicados ya se han propuesto como marcadores de la ventana ideal de implantación, lo que refuerza la idea de que no solo la actividad génica, sino la forma exacta de sus productos, ayuda a definir cuándo el endometrio está verdaderamente preparado.
Células inmunitarias y un regulador clave del splicing
El equipo también estimó los tipos de células inmunitarias presentes en el tejido a partir de los mismos datos de ARN. En mujeres con fallo de implantación, la fase receptiva mostró menos células T citotóxicas y células NK en reposo, pero más monocitos y ciertos macrófagos en comparación con fases anteriores. Más tarde, después de que la ventana se cerró, los patrones volvieron a cambiar, con variaciones en las células NK activadas y en subtipos de macrófagos. Varios de estos cambios en células inmunitarias siguieron de cerca eventos específicos de splicing, lo que sugiere que el remodelado de los mensajes génicos y el equilibrio inmunitario están vinculados. Entre las proteínas que controlan el splicing, una llamada KHDRBS3 destacó como un nodo central conectado a muchos de los eventos alterados y se redujo de forma consistente cuando el endometrio se volvía receptivo, tanto en mujeres fértiles como en las afectadas. Esto sugiere que podría ayudar a impulsar el cambio en los patrones de splicing que acompaña la apertura de la ventana de implantación. 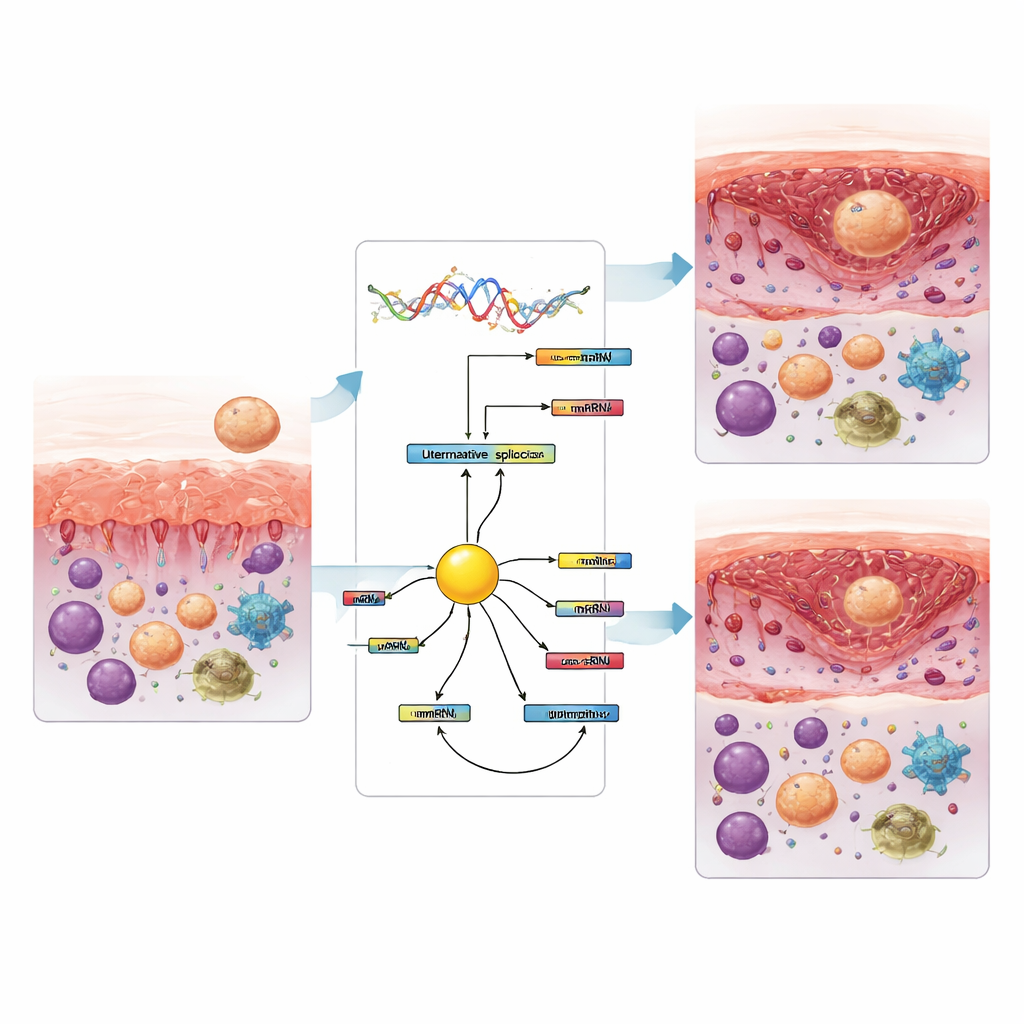
Señales hacia futuras pruebas y tratamientos
Para traducir estos patrones moleculares en posibles terapias, los investigadores se preguntaron si pequeños fármacos existentes podrían contrarrestar las firmas de splicing anómalas que observaron. Al comparar sus listas de genes con grandes bases de datos de respuesta a fármacos, identificaron varios compuestos aprobados o experimentales que actúan sobre genes vinculados a la implantación, incluidos agentes que influyen en respuestas inmunitarias o en vías relacionadas con hormonas. Aunque están lejos de estar listos para uso clínico en este contexto, ofrecen un mapa inicial para ensayos de laboratorio.
Qué significa esto para las pacientes
En conjunto, el estudio muestra que el fallo de implantación no es simplemente una cuestión de tener los «genes equivocados», sino de cómo esos genes se editan en distintos mensajes y de cómo el entorno inmunitario del útero se ajusta con el tiempo. El trabajo destaca a KHDRBS3 y factores relacionados como reguladores prometedores de este proceso y revela cambios coordinados en las células inmunitarias que pueden ayudar o dificultar el intento de un embrión por asentarse. A largo plazo, estos hallazgos podrían conducir a pruebas más refinadas que determinen el momento y la calidad reales de la ventana receptiva de una mujer, así como a tratamientos dirigidos que ajusten de forma sutil el mensajero génico o el equilibrio inmunitario para dar a los embriones una mejor oportunidad de implantarse.
Cita: Wang, Ml., Lu, Bj., Lu, X. et al. Alternative splicing and differential gene expression during changes in endometrial receptivity in patients with recurrent implantation failure. Sci Rep 16, 9754 (2026). https://doi.org/10.1038/s41598-026-40386-w
Palabras clave: receptividad endometrial, fallo de implantación recurrente, splicing alternativo, células inmunitarias uterinas, reproducción asistida