Clear Sky Science · es
Selección adaptativa de ejemplos para detección explicable de mitosis basada en prototipos en patología digital
Por qué esto importa para la atención del cáncer
Cuando los patólogos examinan muestras de cáncer al microscopio, contar cuántas células tumorales se están dividiendo activamente ayuda a decidir cuán agresivo es un tumor y qué tratamientos elegir. La inteligencia artificial puede ahora identificar estas células en diapositivas digitales con rapidez, pero sus decisiones suelen ser un misterio incluso para los expertos. Este artículo presenta un método llamado Selección Adaptativa de Ejemplos (AES) que permite a un sistema de IA “mostrar su razonamiento” señalando casos reales previos que respaldan o contradicen cada decisión, haciendo la detección automática de mitosis más transparente y clínicamente confiable.
El desafío de detectar células en división
Las células tumorales en división, conocidas como figuras mitóticas, son diminutas, raras y visualmente diversas. Con la tinción habitual rosa y púrpura, pueden parecerse mucho a estructuras inocuas como células en muerte o ciertos tipos de células inmunitarias. Los expertos humanos deben revisar enormes diapositivas digitales para encontrarlas, un proceso lento, fatigoso y propenso a desacuerdos. Los sistemas modernos de aprendizaje profundo pueden igualar o superar el rendimiento experto en esta tarea, pero funcionan como cajas negras: generan una puntuación para cada célula sospechosa sin explicar claramente por qué. En medicina, donde las decisiones terapéuticas pueden cambiar vidas, esta falta de claridad es un obstáculo serio para usar IA en la práctica clínica diaria.
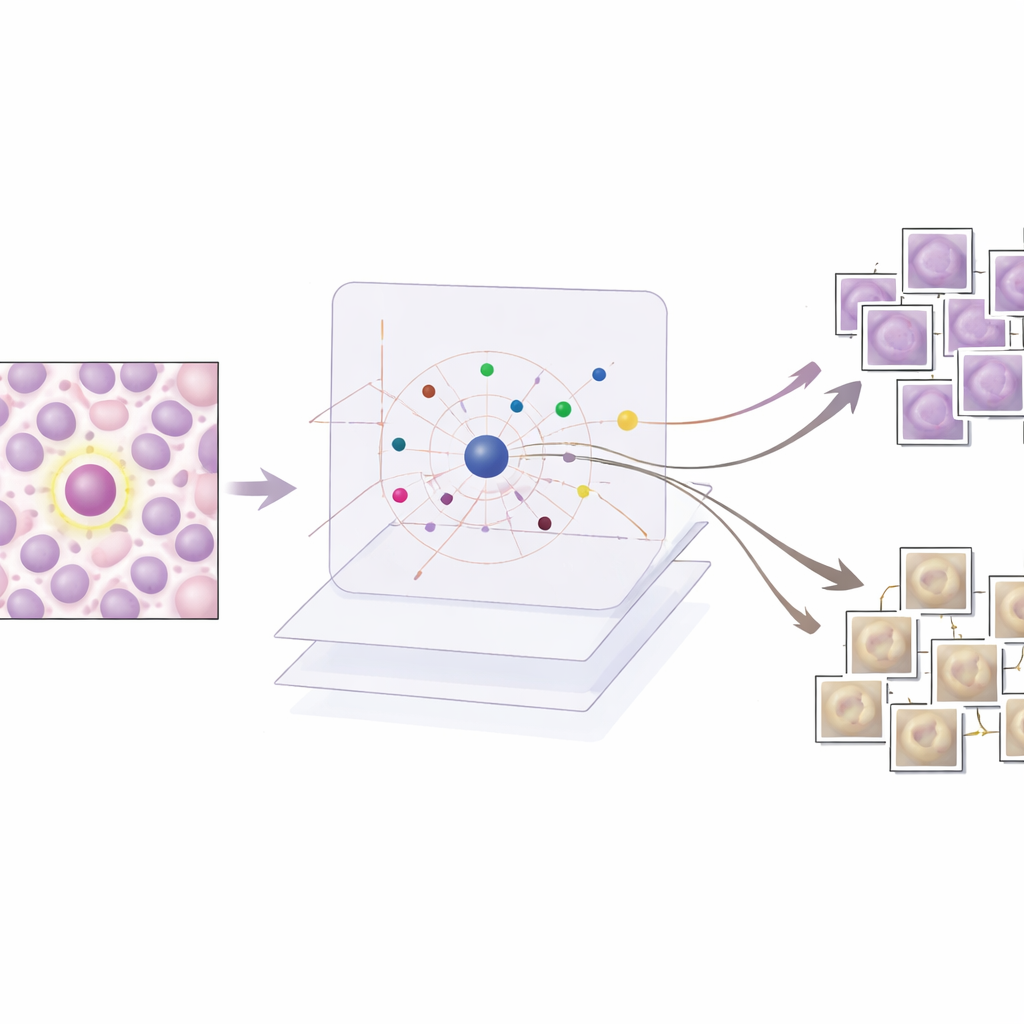
Construir un detector potente pero opaco
Los autores primero entrenan una red de detección de objetos de última generación, basada en la arquitectura Faster R-CNN, para localizar figuras mitóticas en un gran y diverso conjunto de datos llamado MIDOG++. Estas imágenes provienen de tumores humanos y caninos, de varios tipos de cáncer y laboratorios, e incluyen más de once mil células en división etiquetadas cuidadosamente. Para preservar el detalle fino, las diapositivas se dividen en pequeños parches y se aumentan intensamente para imitar las variaciones reales en la tinción y la adquisición de imágenes. El detector resultante alcanza un rendimiento sólido entre tipos tumorales, con puntuaciones F1 de hasta 0,84, lo que confirma que es preciso pero complejo: precisamente el tipo de sistema que necesita mejores explicaciones antes de que los clínicos puedan confiar en él.
Enseñar a la IA a explicarse con ejemplos
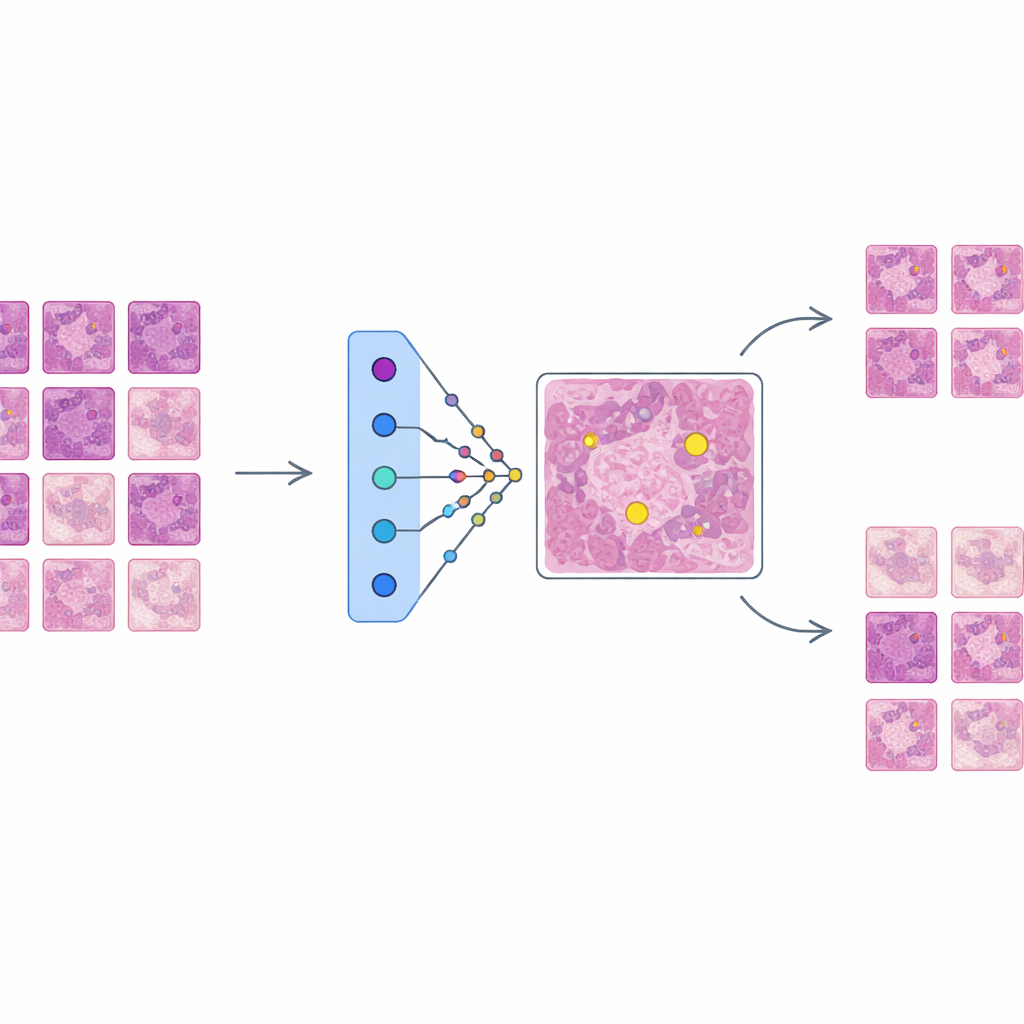
AES se sitúa sobre este detector entrenado como una capa de interpretabilidad en lugar de cambiar el funcionamiento del detector. Para cada región candidata que el detector marca como posiblemente mitótica, AES busca en una biblioteca de parches de tejido reales extraídos de los datos de entrenamiento. De esta biblioteca selecciona un pequeño conjunto de ejemplos “que apoyan” que se parecen a mitosis verdaderas y un conjunto de ejemplos “que contradicen” que se asemejan más a células no mitóticas. Detrás de escena, AES trata las puntuaciones de confianza del detector como un paisaje suave y utiliza una herramienta matemática llamada funciones base radial para aproximar cómo cambia esa confianza cerca de cada caso. Solo se conservan prototipos que influyen de forma significativa en la confianza local, por lo que la explicación de una sola decisión suele implicar alrededor de diez ejemplos cuidadosamente elegidos en lugar de cientos de casos apenas relevantes.
Lo que los ejemplos revelan sobre las decisiones de la IA
Los investigadores evalúan AES tanto en cifras como en ejemplos ilustrativos. Cuantitativamente, muestran que un diccionario compacto de unos 190 prototipos de imagen puede imitar las puntuaciones de confianza del detector con muy alta precisión, manteniendo al mismo tiempo el número de ejemplos mostrados por caso lo suficientemente bajo como para que un humano los revise. Cualitativamente, examinan tres escenarios frecuentes. Cuando el detector está claramente en lo correcto, AES devuelve solo prototipos mitóticos que apoyan fuertemente la decisión, lo que resulta tranquilizador para los clínicos. En las falsas alarmas, el método saca a la luz prototipos mitóticos similares que muestran por qué el detector fue engañado por texturas o patrones de cromatina parecidos, a menudo junto con prototipos no mitóticos más débiles que insinúan incertidumbre. En los mitosis perdidos, AES tiende a devolver principalmente prototipos no mitóticos o ejemplos ambiguos, señalando puntos ciegos en los datos de entrenamiento y sugiriendo dónde son necesarios ejemplos nuevos o mejor etiquetados.
De caja negra a herramienta colaborativa
Al fundamentar cada predicción en un puñado de parches de tejido reales y etiquetados, AES hace que un detector de IA complejo se comporte más como un colega humano que justifica decisiones recordando casos previos. El sistema no solo informa si una célula probablemente se está dividiendo, sino que también muestra por qué y con qué grado de confianza, a través de la mezcla e influencia de prototipos que apoyan y contradicen. Este diseño permite a los patólogos confirmar rápidamente predicciones sólidas, centrar la atención en regiones límite o confusas e identificar patrones de error sistemáticos que pueden guiar un entrenamiento adicional. Aunque fue desarrollado para la detección de mitosis, el mismo enfoque podría extenderse a otras tareas en patología digital, ayudando a mover la IA desde una automatización opaca hacia un asistente interpretable, basado en casos, que los clínicos puedan interrogar, confiar y perfeccionar.
Cita: Banik, M., Kreutz-Delgado, K., Mohanty, I. et al. Adaptive example selection for prototype based explainable mitosis detection in digital pathology. Sci Rep 16, 9481 (2026). https://doi.org/10.1038/s41598-026-40283-2
Palabras clave: IA explicable, patología digital, detección de mitosis, modelos basados en prototipos, diagnóstico del cáncer