Clear Sky Science · es
Fuente pulsada de radiación ionizante ultraintensa basada en la aceleración directa por láser de electrones para estudiar el efecto FLASH
Por qué importan los pulsos de radiación ultrarrápidos
La radioterapia contra el cáncer es un acto de equilibrio: administrar suficiente radiación para eliminar tumores sin causar daño duradero al tejido sano. Una idea reciente y prometedora, llamada efecto FLASH, sugiere que administrar la radiación en un estallido ultra-corto y ultra-intenso puede proteger el tejido normal mientras sigue atacando el cáncer. Este estudio presenta un nuevo tipo de fuente experimental de radiación basada en un láser potente que genera estallidos extremadamente breves de electrones de alta energía, y la usa para observar cómo el oxígeno en agua y líquidos biológicos se consume de forma súbita durante la irradiación —un proceso que se considera central en el efecto FLASH. 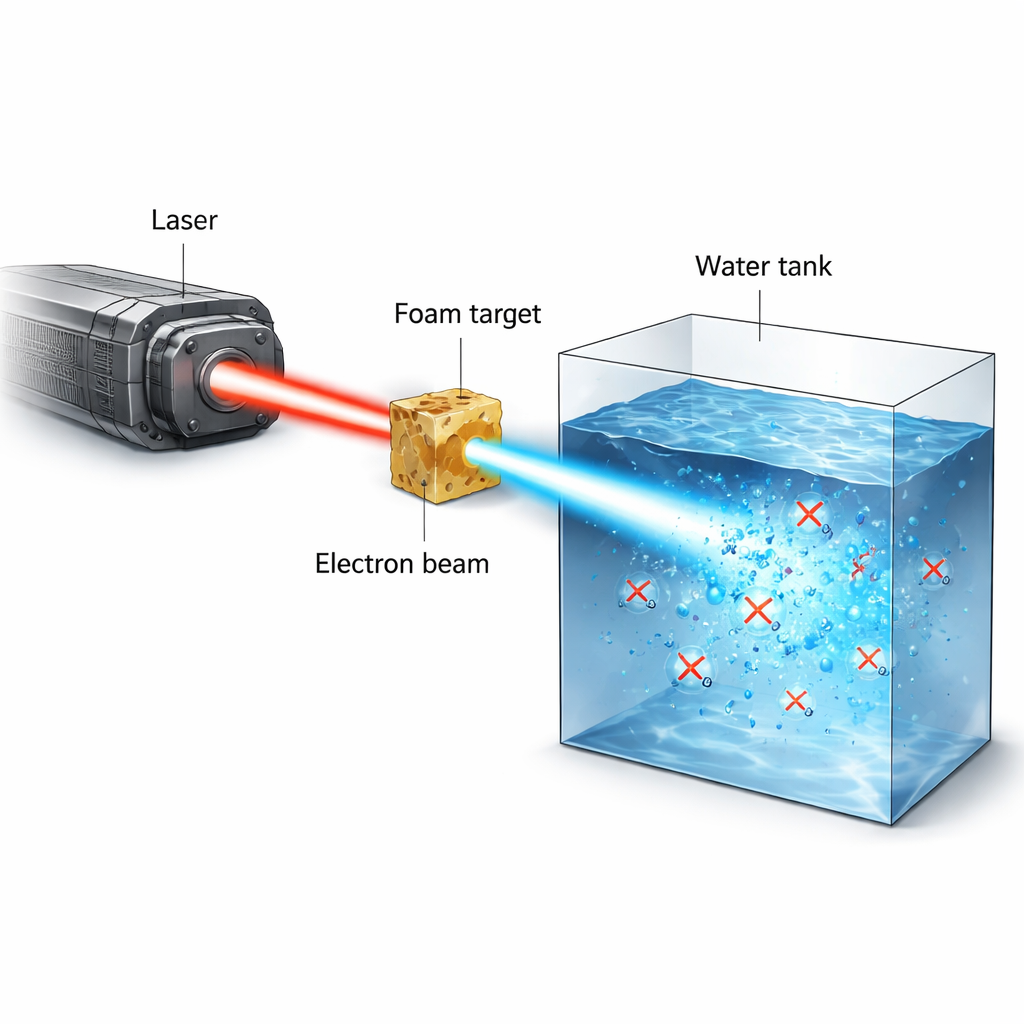
De las máquinas hospitalarias a haces impulsados por láser
La radioterapia convencional utiliza rayos X, electrones o protones procedentes de grandes aceleradores. Estas máquinas normalmente administran la dosis en milisegundos a segundos y, aunque son muy precisas, siguen dañando el tejido sano porque la radiación rompe indirectamente el ADN al fragmentar moléculas de agua y generar especies reactivas de oxígeno. El oxígeno en tejido sano bien vascularizado empeora en realidad este daño —el denominado efecto del oxígeno. La radioterapia FLASH pretende cambiar esta dinámica administrando la dosis terapéutica completa en una fracción de segundo a tasas de dosis ultra-altas, lo que parece proteger temporalmente el tejido normal en estudios animales sin proteger los tumores. Sin embargo, los aceleradores médicos estándar tienen dificultades para alcanzar estas tasas de dosis extremas, lo que motiva la búsqueda de fuentes alternativas como los láseres de alta potencia.
Convertir espuma y luz en un estallido potente de electrones
Los investigadores utilizaron el láser de alta potencia PHELIX para crear haces estrechos y de alta corriente de electrones con energías de varios millones de electronvoltios (MeV). El láser primero ioniza una espuma polimérica de baja densidad convirtiéndola en un plasma casi crítico. En un segundo pulso ultra-corto, de menos de un billonésimo de segundo, el láser empuja y atrapa electrones dentro de un canal de plasma, acelerándolos directamente hasta altas energías. Este proceso, llamado aceleración directa por láser, produce un haz fuertemente colimado que puede transportar decenas de nanoculombios de carga en un estallido de escala de picosegundos. Cuando este haz impacta agua o un material similar al agua, puede depositar entre 20 y 50 gray en una sola toma, con tasas de dosis instantáneas por encima de 10¹³ gray por segundo —muy por encima de lo que pueden lograr las máquinas convencionales.
Observando cómo el oxígeno desaparece en un instante
Para sondear cómo afectan esos estallidos intensos a la química en condiciones semejantes a las tisulares, el equipo construyó tanques sellados de agua que podían operar en vacío y llenarse con agua pura, medio de cultivo celular o células lizadas, todos completamente oxigenados de antemano. El haz de electrones se modeló y filtró de modo que los electrones de alta energía dominaran la dosis dentro del tanque, mientras que los protones y los rayos X se suprimieron en gran medida o se contabilizaron cuidadosamente mediante capas de blindaje y películas radio-crómicas. Un sensor óptico colocado en la pared interior del tanque monitorizó el oxígeno disuelto midiendo cómo las moléculas de oxígeno amortiguan la luminiscencia de una mancha de tinte. Tras cada irradiación de un único pulso, el sensor registró una caída súbita en la concentración de oxígeno que luego se relajó lentamente a medida que el oxígeno se difundía dentro de la región del sensor. Combinando los datos de las películas, simulaciones y la conocida potencia de frenado de los electrones, los autores reconstruyeron la dosis entregada al volumen irradiado y la vincularon directamente con la pérdida de oxígeno medida. 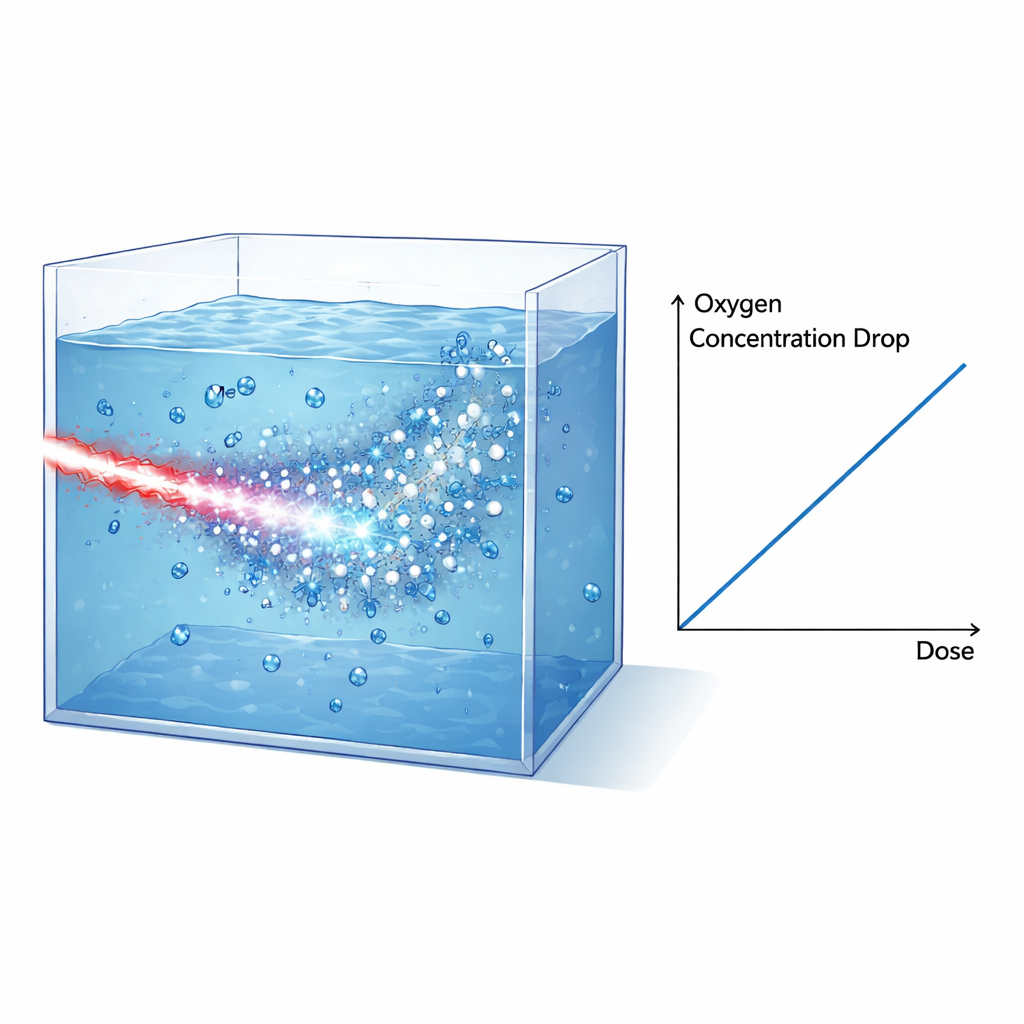
Vinculando experimento y teoría
El hallazgo clave es que la disminución del oxígeno disuelto es proporcional a la dosis entregada tanto en agua como en medio de cultivo, con pendientes muy similares. Tras corregir por una pequeña dosis adicional de rayos X, el consumo de oxígeno medido en agua es de aproximadamente 0,32 micromoles por litro y por gray. Este valor coincide sorprendentemente bien con las predicciones de detalladas simulaciones de estructura de pista Monte Carlo (TRAX-CHEM), que siguen las trayectorias de los electrones en agua y modelan la rápida química que se desarrolla en los microsegundos posteriores a la irradiación. De forma crucial, en este montaje impulsado por láser, casi toda la dosis se entrega en alrededor de un picosegundo —mucho más corto que los tiempos característicos de las reacciones químicas subsiguientes. Eso significa que el experimento reproduce de forma fiel las condiciones ideales asumidas en estas simulaciones, proporcionando una prueba rigurosa de los modelos subyacentes.
Construir un banco de pruebas mejor para la ciencia FLASH
Más allá de validar la teoría, los autores usan sus resultados para diseñar una disposición experimental mejorada. Al simplificar la geometría, eliminar imanes y colocar simétricamente agua y películas medidoras de dosis alrededor del haz, los montajes futuros podrían medir directamente la dosis dentro del tanque sin reconstrucciones complejas, a la vez que suprimen aún más las contribuciones indeseadas de protones y rayos X. Las simulaciones muestran que modificar el blanco —por ejemplo, añadiendo capas delgadas de plástico o oro— permite ajustar la dosis por disparo entre aproximadamente 40 y 80 gray, ofreciendo una plataforma flexible para explorar una amplia gama de condiciones relevantes para FLASH.
Lo que esto significa para tratamientos futuros del cáncer
Para no especialistas, el mensaje principal es que esta fuente basada en láser crea pulsos de electrones extremadamente intensos y ultracortos que imitan —y en algunos aspectos superan— las condiciones previstas para la radioterapia FLASH. El estudio muestra que estos pulsos consumen rápidamente el oxígeno disuelto en agua y medios biológicos de una manera que concuerda con predicciones teóricas avanzadas. Dado que el agotamiento del oxígeno y la química radicalaria relacionada son candidatas principales para explicar por qué FLASH podría preservar el tejido sano, disponer de una fuente controlable y bien caracterizada como esta es un avance importante. Proporciona un banco de pruebas potente para refinar modelos y, en última instancia, para orientar el diseño de futuras máquinas clínicas que podrían tratar el cáncer de forma más efectiva y con menos efectos secundarios.
Cita: Gyrdymov, M., Bukharskii, N., Fabian, V. et al. Ultra-intense pulsed source of ionizing radiation based on direct laser acceleration of electrons for studying the FLASH effect. Sci Rep 16, 7164 (2026). https://doi.org/10.1038/s41598-026-40281-4
Palabras clave: Radioterapia FLASH, electrones impulsados por láser, tasa de dosis ultraalta, agotamiento de oxígeno, radiolisis del agua