Clear Sky Science · es
La depuración selectiva de anticuerpos monoclonales mediante el receptor de la manosa depende del apareamiento de glicanos
Por qué importan los patrones de azúcares en los medicamentos
Muchos de los fármacos más vendidos hoy en día son anticuerpos monoclonales: proteínas diseñadas que pueden permanecer en el torrente sanguíneo durante semanas y dirigirse con precisión a enfermedades como el cáncer y los trastornos autoinmunes. Pero no todos los anticuerpos se comportan igual una vez inyectados. Este estudio plantea una pregunta aparentemente sencilla con consecuencias importantes: ¿cómo decide el fino “patrón de azúcares” unido a un anticuerpo la rapidez con la que el organismo lo elimina, y podría esto también influir en efectos secundarios como las reacciones inmunitarias?
Pequeños azúcares como señales de tráfico
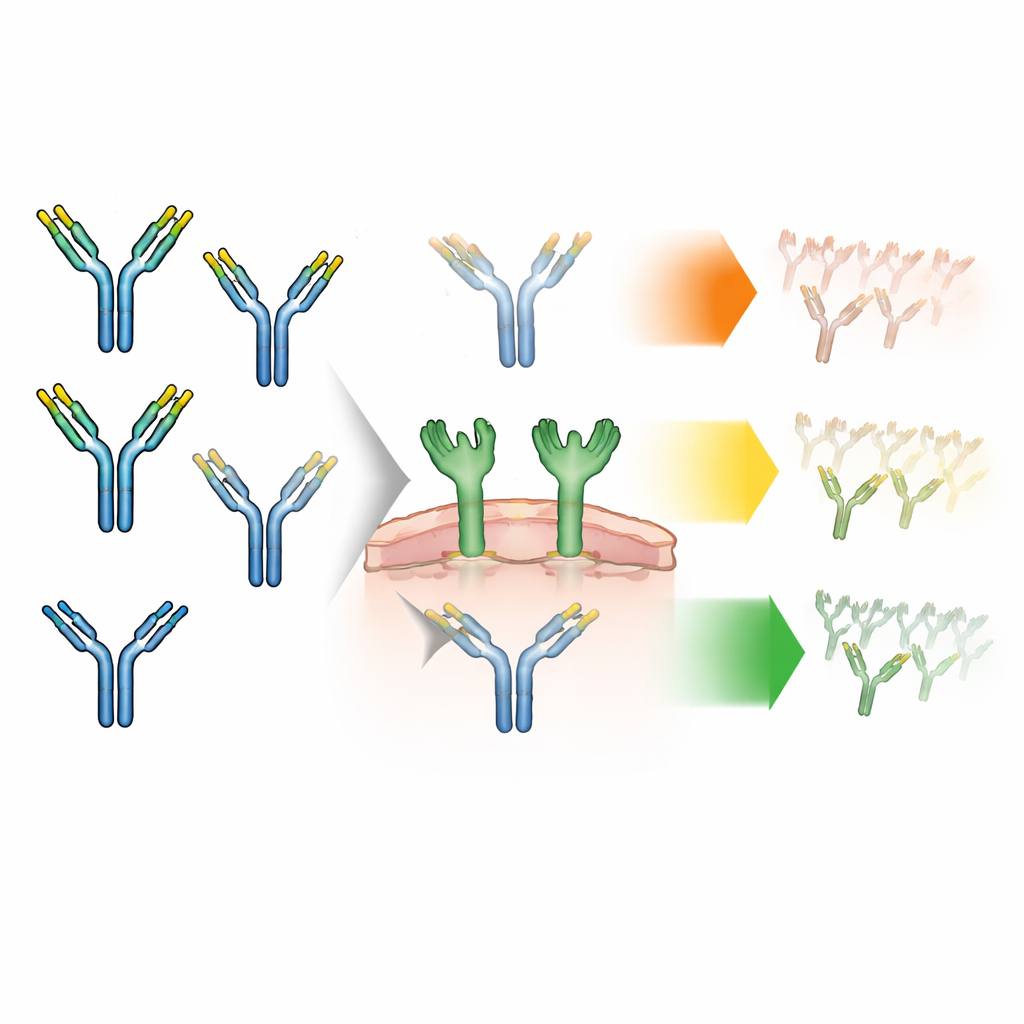
Los anticuerpos llevan de forma natural pequeñas cadenas de azúcares, llamadas glicanos, en su esqueleto. Estos glicanos existen en distintas variantes. La mayoría tienen formas “complejas”, pero una minoría son de tipo “alto en manosa”, más simples, que trabajos previos habían vinculado a una eliminación más rápida de la sangre. Cada anticuerpo tiene dos sitios de azúcar que actúan en pareja, y estos pueden coincidir (pares simétricos) o diferir (pares asimétricos). Hasta ahora, los fabricantes de fármacos contaban sobre todo cuántos de cada tipo de azúcar había en total, sin indagar cómo se apareaban los dos azúcares en el mismo anticuerpo. Los autores sospechaban que este patrón de apareamiento podría cambiar la intensidad con la que los anticuerpos interactúan con una proteína especial que detecta azúcares en las células inmunitarias, llamada receptor de la manosa, y por tanto la rapidez con la que el organismo elimina el fármaco.
Clasificar anticuerpos por sus pares de azúcares
Para explorar esto, el equipo diseñó anticuerpos enriquecidos en glicanos altos en manosa y luego los separó físicamente en tres grupos principales: anticuerpos con dos glicanos complejos, con un glicano complejo y otro alto en manosa (asimétricos), o con dos glicanos altos en manosa (simétricos). Verificaron cuidadosamente que estos grupos fueran casi idénticos en todo lo demás: mismo tamaño, forma, carga y estabilidad, y unión similar al receptor de reciclaje que normalmente protege a los anticuerpos de la degradación. Eso significaba que cualquier diferencia observada posteriormente en experimentos celulares o en animales podía atribuirse exclusivamente al apareamiento de glicanos, y no a daños ocultos o impurezas.
Observar cómo las células internalizan los anticuerpos
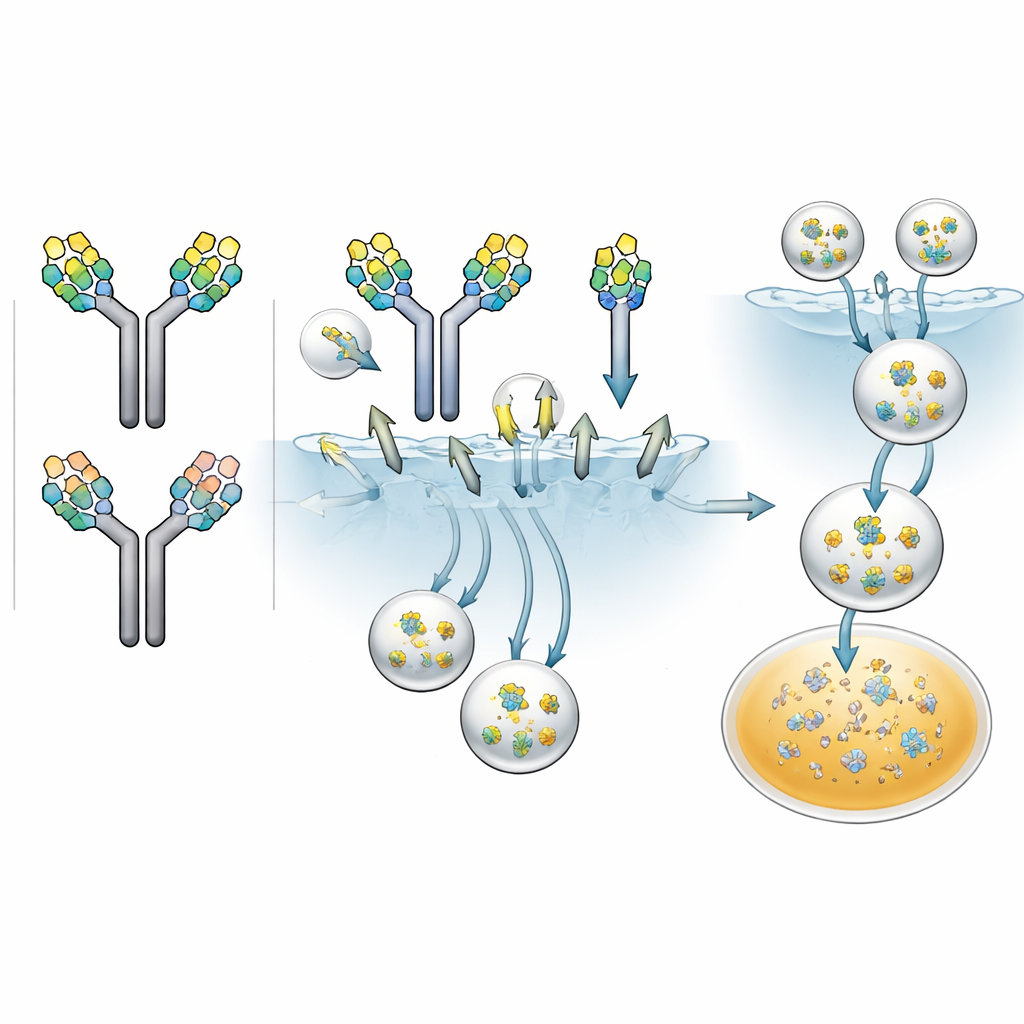
A continuación, los investigadores midieron qué tan deprisa cada patrón de azúcares permitía que las células que portan el receptor de la manosa engulleran los anticuerpos. Marcóron las distintas fracciones de anticuerpos con una etiqueta fluorescente e incubaron con células humanas diseñadas para expresar este receptor. Durante casi tres días siguieron el brillo dentro de las células como medida de la captación. Todos los anticuerpos fueron internalizados en cierta medida, pero las tasas difirieron: los que tenían dos glicanos altos en manosa se internalizaron más rápido, los que tenían un glicano alto en manosa tuvieron una tasa intermedia, y los que solo tenían glicanos complejos fueron los más lentos. Cuando el equipo añadió manano—un azúcar natural que compite por el receptor de la manosa—la captación de los anticuerpos altos en manosa disminuyó drásticamente, confirmando que ese receptor era responsable de gran parte de la internalización rápida.
Seguir anticuerpos marcados por azúcares en animales vivos
La prueba crucial fue si estas diferencias celulares se traducirían en un comportamiento real del fármaco. Los científicos formularon un producto farmacéutico rico tanto en pares simétricos como asimétricos altos en manosa, junto con pares solo complejos, y lo inyectaron en ratas. Usando métodos sensibles de espectrometría de masas, pudieron rastrear no solo el nivel total de anticuerpo durante dos semanas, sino también cómo disminuía cada apareamiento de glicanos con el tiempo. El patrón fue llamativo: los anticuerpos con dos glicanos altos en manosa desaparecieron más rápido, con una vida media de aproximadamente 2,4 días; los que tenían un glicano alto en manosa duraron más, alrededor de 7,2 días; y los que solo tenían glicanos complejos persistieron aproximadamente 17,4 días. La exposición a lo largo del tiempo—el área bajo la curva de concentración—se redujo al 38% para el par doble alto en manosa y al 73% para el par mixto en comparación con el par solo complejo. En esencia, cada glicano extra alto en manosa actuó como una bandera adicional de “clárame” para el receptor de la manosa.
Qué significa esto para fármacos más seguros y duraderos
Para los pacientes, estos resultados aclaran por qué dos fármacos basados en anticuerpos que parecen similares en el papel pueden comportarse de forma distinta en el organismo. El estudio muestra que no solo la presencia, sino el apareamiento de glicanos altos en manosa dirige con fuerza la rapidez con la que se eliminan los anticuerpos, probablemente mediante la captación y degradación impulsadas por el receptor de la manosa en las células inmunitarias. Dado que la misma vía también puede aportar antígenos a la maquinaria que desencadena respuestas inmunitarias, estos patrones de azúcares podrían influir en el riesgo de anticuerpos anti-fármaco y reacciones alérgicas. Los autores sostienen que los fabricantes deberían vigilar y controlar el apareamiento de glicanos—no solo la composición global de azúcares—al diseñar y probar terapias con anticuerpos. Hacerlo podría ayudar a garantizar dosis más previsibles, beneficios más duraderos y menor probabilidad de respuestas inmunitarias no deseadas.
Cita: Baumeister, J., Meudt, M., Wei, W. et al. Selective clearance of monoclonal antibodies via the mannose receptor is dependent on glycan pairing. Sci Rep 16, 8489 (2026). https://doi.org/10.1038/s41598-026-40268-1
Palabras clave: anticuerpos monoclonales, glicosilación, receptor de la manosa, farmacocinética, inmunogenicidad