Clear Sky Science · es
Una plataforma modular para el cultivo automatizado de organoides y la imagen longitudinal
Mini órganos en un chip
Imagínese poder observar versiones diminutas y cultivadas en el laboratorio de órganos humanos desarrollarse en tiempo real, como una película en cámara lenta de cómo crecen nuestros tejidos, se enferman o responden a medicamentos. Esa es la promesa de los organoides: cúmulos celulares 3D que imitan órganos reales. Este artículo describe una nueva plataforma de sobremesa que puede mantener automáticamente organoides cerebrales vivos, alimentados y cuidadosamente vigilados durante días, sin necesidad de un incubador voluminoso. Abre la puerta a modelos de enfermedad más fiables, pruebas de fármacos más inteligentes y, finalmente, a una medicina más personalizada.
Por qué es tan difícil cultivar mini órganos
Los organoides se han convertido en herramientas poderosas para estudiar el cerebro, el intestino, el riñón y otros órganos, porque reproducen muchas de las estructuras y tipos celulares presentes en órganos reales. Pero mantenerlos saludables resulta sorprendentemente complicado. Los métodos estándar dependen de que las personas cambien manualmente el líquido que alimenta las células y de colocar matraces en plataformas de agitación dentro de incubadores cálidos y húmedos. Este procedimiento requiere mucho trabajo y puede ser inconsistente entre laboratorios. Peor aún, el entorno estrecho y húmedo dentro de un incubador dificulta colocar cámaras y otros dispositivos electrónicos cerca, por lo que los investigadores normalmente no pueden observar de forma continua cómo cambia el tejido con el tiempo. Los sistemas microfluídicos existentes mejoran el control del líquido nutritivo, pero la mayoría aún funcionan dentro de esos mismos incubadores, lo que limita la imagen a largo plazo.
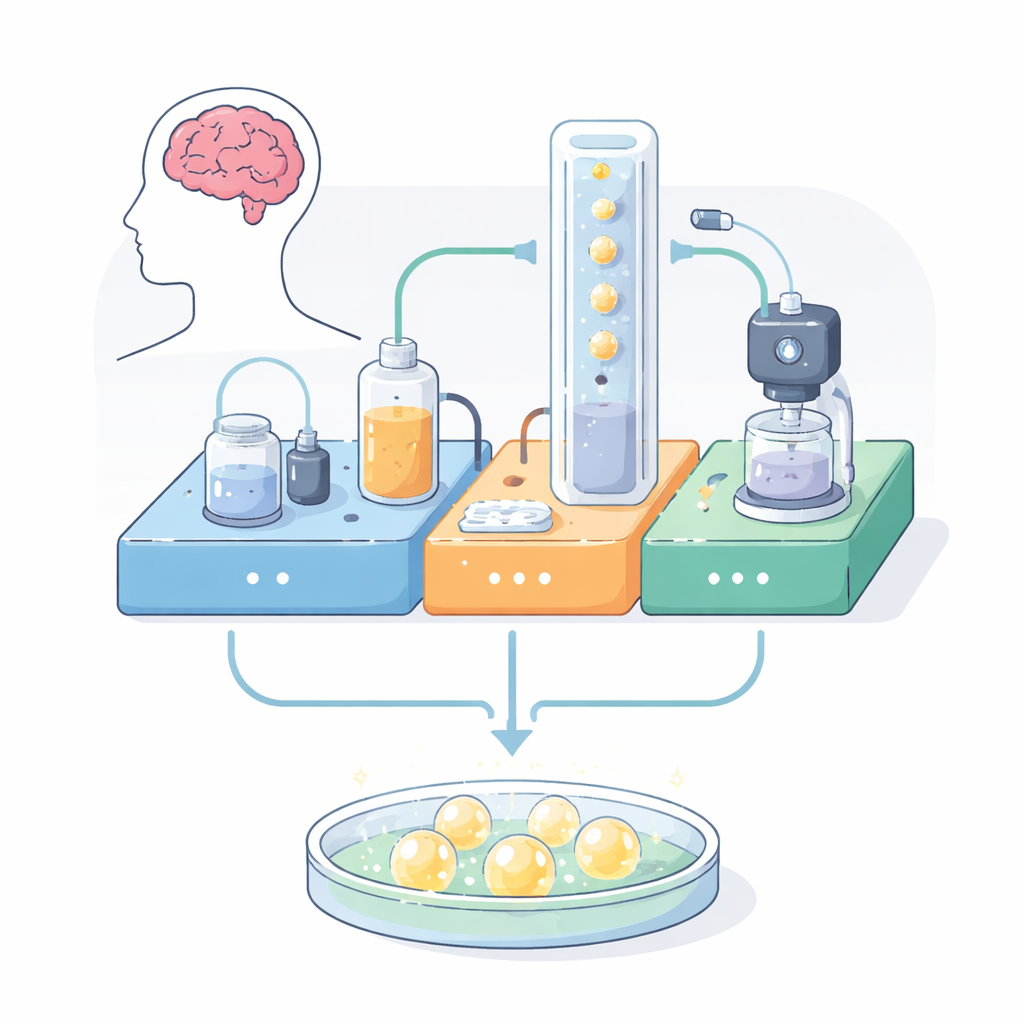
Un sistema de soporte vital autónomo
Los autores construyeron una plataforma modular que reúne tres funciones normalmente dispersas en distintos equipos: alimentación automatizada, imagen en vivo y control ambiental. Todo está montado en una placa metálica perforada y compacta usando soportes impresos en 3D y piezas comerciales. Un módulo bombea líquido nutritivo templado en un circuito cerrado, recirculándolo junto a los organoides mientras filtra impurezas. Un segundo módulo ajusta constantemente la temperatura y la acidez, usando un calentador y burbujas de dióxido de carbono controladas para mantener condiciones similares a las del cuerpo. Un tercer módulo alberga un pequeño microscopio digital cerca de la cámara de cultivo, capturando imágenes en campo claro y fluorescencia e incluso detectando etiquetas verdes y rojas comunes dentro de las células. Los tres módulos se comunican entre sí mediante electrónica sencilla, lo que permite ejecuciones largas y desatendidas.
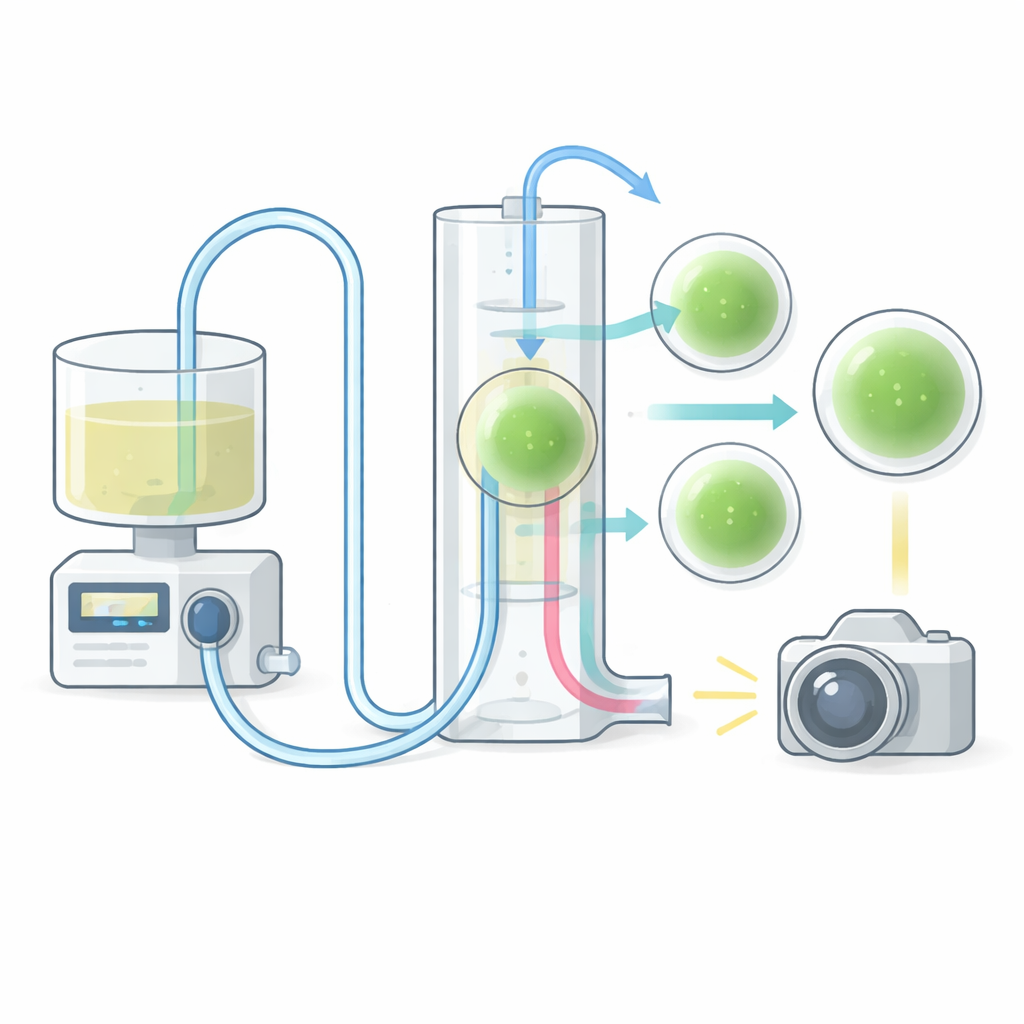
El chip vertical que lo muestra todo
En el corazón del sistema hay una cámara de cultivo personalizada: un pozo de silicona transparente unido a un portaobjetos de vidrio. A diferencia de las placas planas tradicionales, este chip está montado en posición vertical. Esa orientación inusual permite a los investigadores observar cómo fluye realmente el líquido alrededor y más allá de cada organoide, en lugar de limitarse a una vista cenital. El pozo incluye canales de entrada y salida colocados lo bastante altos para evitar que las muestras se laven, y la abertura es lo bastante grande como para cargar organoides con una pipeta de laboratorio estándar, a la vez que permite el intercambio gaseoso. El chip puede fabricarse en menos de un día usando moldes impresos en 3D y materiales económicos, y puede configurarse como un único pozo grande o en versiones multi‑pozo que albergan varios organoides en serie o en paralelo. Esta flexibilidad facilita escalar los experimentos o comparar distintos patrones de flujo.
¿Se mantienen sanos los mini cerebros?
Para comprobar si la plataforma realmente soporta tejido vivo, el equipo cultivó organoides cerebrales de ratón y los dividió entre condiciones estándar de incubador y el nuevo dispositivo. Tras seis días, tiñeron los organoides con un colorante que marca membranas de células vivas y examinaron su estructura con anticuerpos contra una proteína específica de neuronas. Los organoides en la plataforma fueron igual de viables y estructuralmente organizados que los del incubador, en todos los diseños de chip. También midieron nutrientes y sales clave—como glucosa, sodio, potasio, calcio y cloruro—en el líquido de cultivo. Los niveles se mantuvieron estables y sin diferencias estadísticamente significativas respecto a los controles en incubador, demostrando que el flujo automatizado no estresó el tejido. Las imágenes en lapso de tiempo revelaron un crecimiento constante del tamaño del organoide, y los chips multi‑pozo redujeron las fusiones indeseadas entre organoides vecinos, un problema común en los cultivos tradicionales.
Observando el movimiento de nutrientes en tiempo real
La plataforma no es solo un sistema de soporte vital; también es una ventana sobre cómo se mueven las moléculas a través del tejido 3D. En un experimento, los investigadores impulsaron un colorante fluorescente a través del chip y siguieron su incorporación en distintas regiones de un organoide durante varios minutos. Los patrones de brillo resultantes coincidieron con simulaciones por ordenador del flujo de fluidos y la difusión, confirmando que el dispositivo puede capturar procesos dinámicos de transporte con gran detalle. Esta capacidad de alinear películas reales de penetración de colorantes o fármacos con modelos predictivos podría ayudar a optimizar cómo se administran las terapias y cómo se aplican señales formadoras de patrones durante experimentos semejantes al desarrollo.
Qué significa esto en el futuro
En términos sencillos, este trabajo entrega un «mini‑incubador sobre una placa» compacto y asequible que puede cultivar organoides cerebrales automáticamente mientras los filma y mide su entorno. Supera la habitual contradicción entre mantener tejidos en un estado realista y bien controlado y poder observar lo que ocurre dentro de ellos. Aunque el estudio actual se centra en tejido cerebral de ratón durante aproximadamente una semana, el mismo enfoque podría extenderse a organoides humanos y experimentos más largos, proporcionando una plataforma más fiel e informativa para estudiar el desarrollo cerebral, las enfermedades neurológicas y nuevos fármacos.
Cita: Torres-Montoya, S., Hernandez, S., Seiler, S.T. et al. A modular platform for automated organoid culture and longitudinal imaging. Sci Rep 16, 9717 (2026). https://doi.org/10.1038/s41598-026-40231-0
Palabras clave: organoides, modelos cerebrales, microfluídica, imagen celular en vivo, cultivo celular automatizado