Clear Sky Science · es
Caracterización multimodal del inicio y crecimiento de trombos inducidos por el flujo en oxigenación por membrana extracorpórea
Por qué importan los coágulos en las máquinas de soporte vital
La oxigenación por membrana extracorpórea, u ECMO, es una forma de derivación corazón‑pulmón que puede mantener con vida a pacientes críticos mientras sus órganos se recuperan. Pero hacer circular la sangre por bombas y tubos de plástico la expone a fuerzas mecánicas severas para las que nuestro cuerpo no está diseñado. Estas fuerzas pueden desencadenar coágulos peligrosos dentro del circuito, que a su vez aumentan el riesgo de ictus, daño orgánico o fallo del dispositivo. Este estudio se propuso descubrir cómo, exactamente, el flujo de sangre a través de una bomba de ECMO influye en el nacimiento y crecimiento de estos trombos, con el objetivo a largo plazo de hacer la ECMO más segura y eficaz.
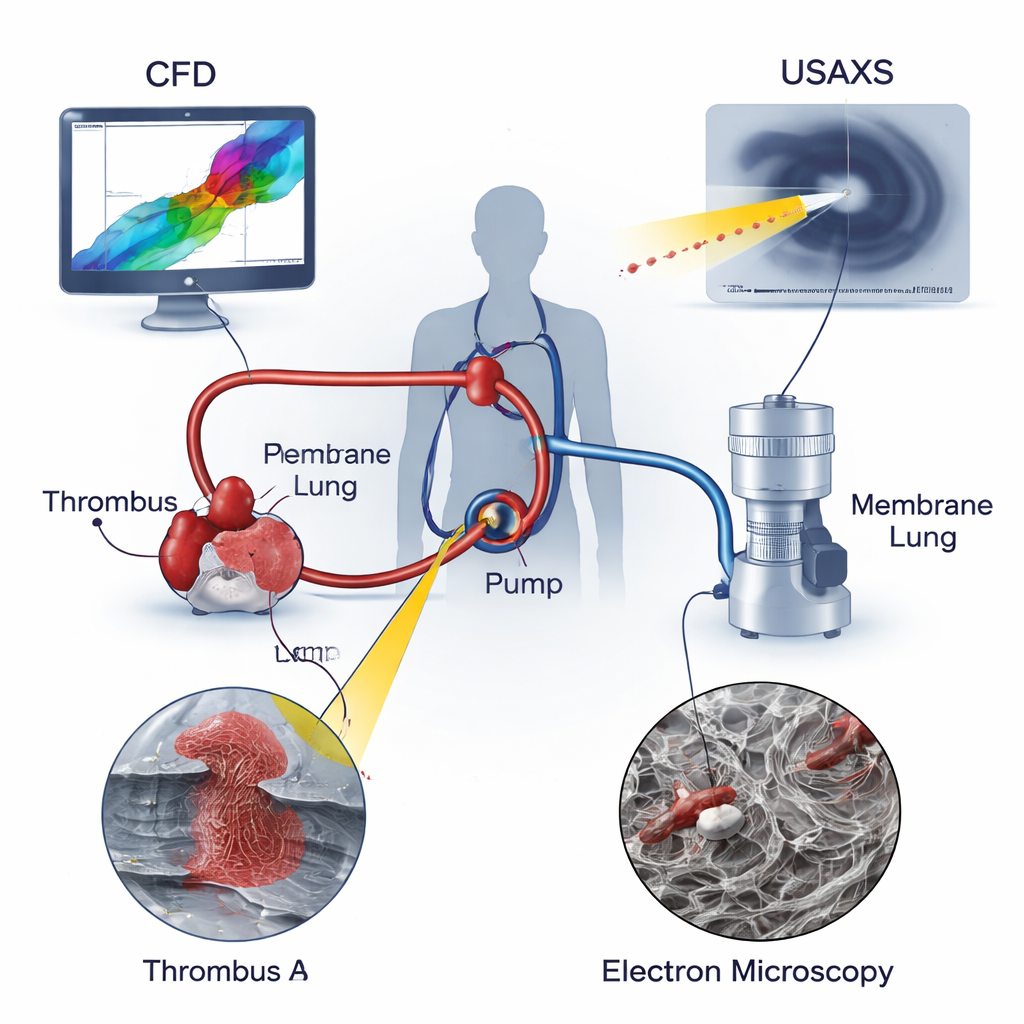
Cómo la ECMO mantiene a los pacientes con vida
En ECMO, la sangre se extrae de una vena o arteria de gran calibre, se impulsa mediante una bomba centrífuga a través de un “pulmón de membrana” que aporta oxígeno y elimina dióxido de carbono, y luego se devuelve al paciente. A diferencia del flujo sanguíneo uniforme en los vasos naturales, el flujo en un circuito de ECMO incluye condiciones extremas: corrientes muy rápidas, cambios bruscos de dirección y bolsillos casi estancados donde la sangre permanece. Estos entornos son conocidos por dañar las células sanguíneas y estimular la coagulación. Los modelos médicos clásicos se centran en el flujo lento o bloqueado en los vasos, pero no explican completamente el intenso cizallamiento y estiramiento que la sangre experimenta dentro de una bomba giratoria. Los autores sostienen que, para entender realmente el riesgo de trombosis en ECMO, es necesario estudiar tanto las fuerzas mecánicas en el dispositivo como la estructura microscópica de los trombos que emergen.
Mirando los coágulos desde tres ángulos
Los investigadores combinaron tres herramientas potentes para analizar dos trombos reales extraídos de circuitos de ECMO usados en niños: un trombo en la entrada de la bomba (Trombo A) y otro en la tubería justo aguas abajo de la bomba (Trombo B). La dinámica de fluidos computacional (CFD) simuló cómo se movía la sangre a través de la bomba, revelando regiones de recirculación y flujo en remolino y señalando dónde se alcanzaban los picos de esfuerzo cortante y estiramiento. La dispersión de rayos X a muy pequeño ángulo (USAXS) penetró profundamente en cada trombo, midiendo qué tan compacta y direccionalmente alineada estaba la andamiaje de fibrina —la malla proteica que mantiene unidos los coágulos— a lo largo de la muestra. La microscopía electrónica de barrido (SEM) proporcionó imágenes altamente magnificadas de las superficies de los trombos, mostrando las formas de los eritrocitos, leucocitos, plaquetas y las fibras de fibrina circundantes. Superponiendo estas tres perspectivas, el equipo pudo vincular las condiciones locales de flujo con la arquitectura interna de cada trombo.
Una zona de recirculación forma un trombo rígido y alineado
CFD mostró que el área cerca de la entrada de la bomba, donde se formó el Trombo A, contenía una zona de recirculación: la sangre era empujada hacia atrás y hacia arriba a lo largo de la carcasa antes de reincorporarse al flujo principal. Esta región permitió que los componentes sanguíneos permanecieran más tiempo y también experimentaran diferencias de velocidad marcadas en el límite entre el flujo recirculante y el entrante. Dentro del Trombo A, USAXS indicó un alto contenido de fibrina—al menos un 70 por ciento—y una fuerte alineación general de las fibras en una dirección preferente, lo que sugiere un andamiaje denso y rígido. Las imágenes SEM confirmaron una red de fibrina muy tejida, intercalada con eritrocitos de forma anómala y fragmentos de plaquetas. Los autores proponen que la combinación de tiempos de residencia prolongados y fuerte cizallamiento local favoreció el crecimiento de un coágulo compacto y altamente organizado capaz de resistir las tensiones mecánicas de la bomba.
El flujo en remolino da forma a un trombo más laxo y torsionado
En contraste, el Trombo B, tomado de la tubería tras la bomba, creció en una región dominada por un flujo de salida en remolino. CFD reveló estructuras de flujo rotatorias, tipo espiral, que emergían de la salida de la bomba, y los datos de USAXS mostraron una red de fibrina que seguía siendo dominante pero menos densa y menos fuertemente alineada en conjunto. La dirección principal de orientación de la fibrina cambió gradualmente a través del trombo, de un ángulo de inclinación a otro, reflejando el patrón de flujo torsionado. Las imágenes SEM mostraron hilos de fibrina de grosor variable y numerosos eritrocitos y leucocitos atrapados, incluida evidencia de daño celular e inflamación. De forma importante, las simulaciones también identificaron pequeñas pero significativas porciones del volumen de la bomba donde las fuerzas de estiramiento eran lo bastante altas como para desplegar el factor von Willebrand, una proteína sanguínea clave que se vuelve adhesiva bajo estrés y puede reclutar plaquetas rápidamente. Estas zonas se concentraban cerca de las palas del impulsor y de la salida, lo que las convierte en lugares probables para los eventos iniciales de activación que condujeron al Trombo B.
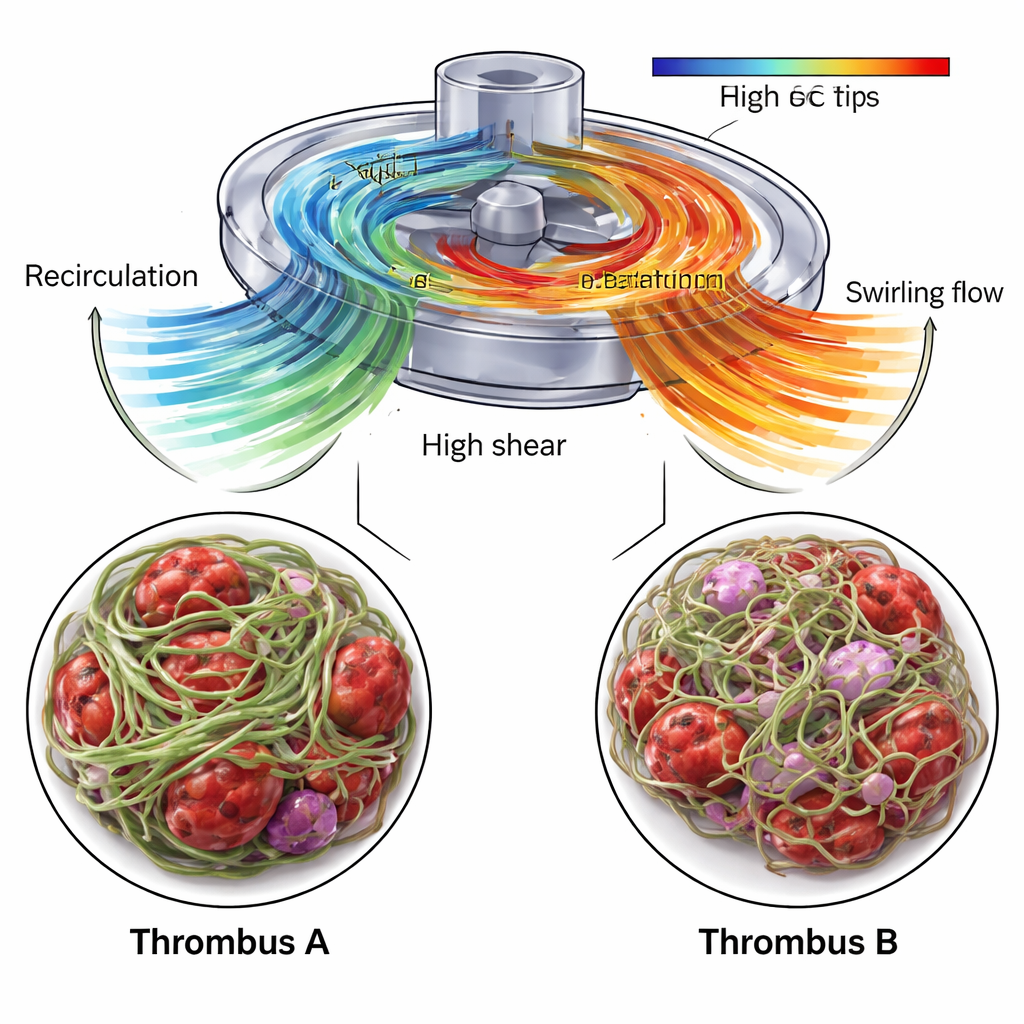
Hacia máquinas de soporte vital más seguras
Al combinar simulaciones detalladas del flujo sanguíneo con mediciones por rayos X y microscopía electrónica de trombos reales de ECMO, este trabajo muestra que el “grano” interno y la densidad de un trombo reflejan el entorno mecánico en el que se formó. El flujo recirculante cerca de la entrada de la bomba se relacionó con un andamiaje de fibrina denso y muy alineado, mientras que el flujo de salida en remolino se asoció con una red más torsionada y abierta que aun así atrapó muchas células sanguíneas e inmunitarias. Estos conocimientos señalan regiones específicas en bombas y tuberías de ECMO donde cambios de diseño o ajustes dirigidos de la anticoagulación podrían reducir con mayor eficacia el riesgo de trombosis. A largo plazo, ese mapeo multiescala—desde la geometría de la bomba y los patrones de flujo hasta la disposición de las proteínas—podría orientar diseños de dispositivos más seguros y ayudar a los clínicos a equilibrar mejor los peligros gemelos de la hemorragia y la trombosis durante el soporte vital con ECMO.
Cita: Nilsson, F., Sochor, B., Henriksson, S. et al. Multimodal characterization of flow-induced thrombus initiation and growth in extracorporeal membrane oxygenation. Sci Rep 16, 7166 (2026). https://doi.org/10.1038/s41598-026-40177-3
Palabras clave: ECMO, coagulación sanguínea, esfuerzo cortante, bomba centrífuga de sangre, estructura de fibrina