Clear Sky Science · es
Respuestas de las células gliales de Müller y microgliales acopladas a la recuperación de los fotorreceptores cono tras una ablación limitada de conos en la retina de pez cebra
Por qué importa la reparación ocular en peces
La parte posterior del ojo, llamada retina, convierte la luz en visión. En las personas, una vez que esas células fotosensibles sufren un daño importante, rara vez se regeneran, lo que provoca pérdida visual permanente. Los peces cebra son diferentes: pueden reparar de forma natural partes de sus retinas. Este estudio examina qué ocurre cuando solo una pequeña fracción de las células sensibles al color del pez cebra sufre estrés o se pierde de forma temporal, revelando cómo las células de soporte y las células inmunitarias se activan para ayudar a la retina a recuperarse. Comprender esta coreografía podría algún día inspirar nuevas formas de proteger o reparar la visión humana.
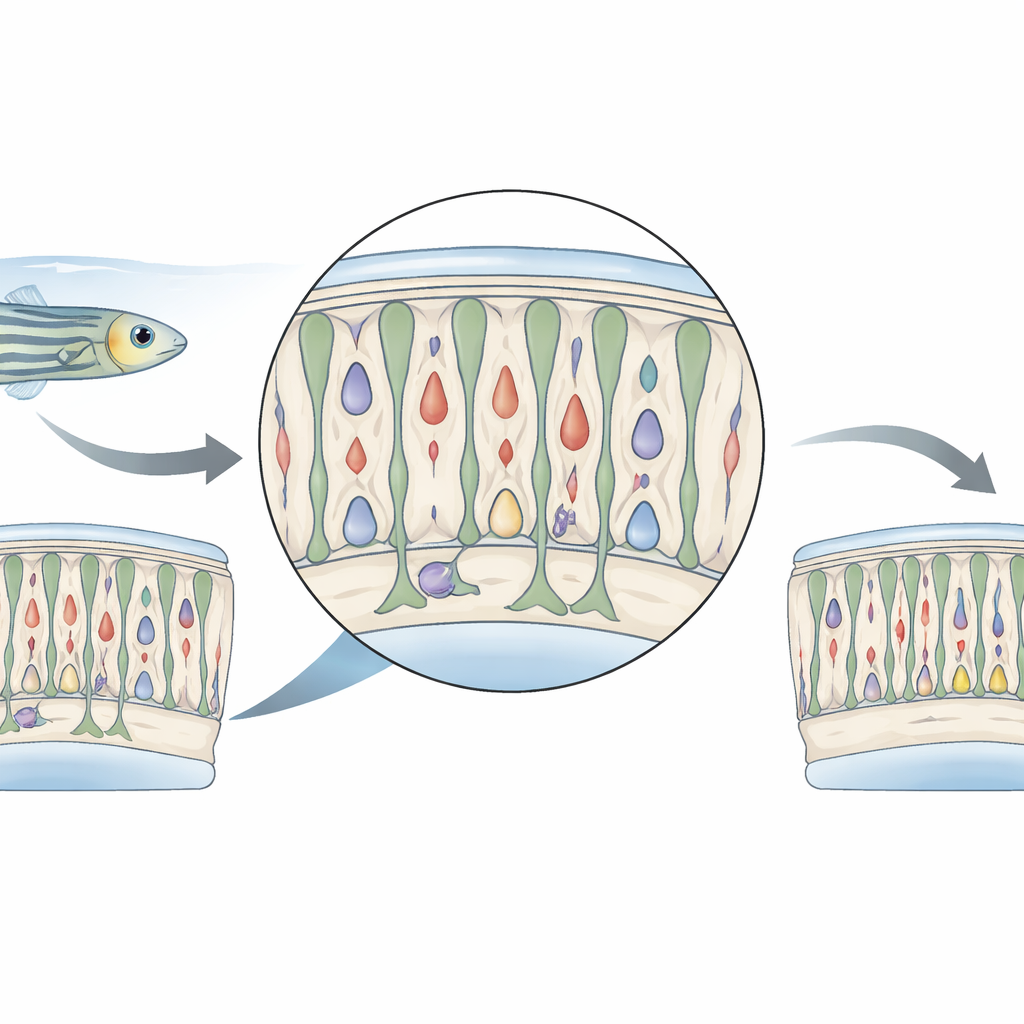
Un empujón suave al ojo
Los investigadores trabajaron con peces cebra genéticamente modificados cuyos fotorreceptores cono —las células que detectan el color y la luz diurna— contienen una enzima que puede convertir un fármaco inocuo en una toxina, pero solo dentro de esos conos. Los peces adultos se sumergieron durante 24 horas en el fármaco metronidazol y luego se devolvieron a agua limpia. En lugar de eliminar grandes cantidades de conos, este tratamiento mató solo a un pequeño subconjunto. La mayoría de los conos sobrevivieron pero mostraron signos de daño temporal: su apariencia cambió, su señal fluorescente se debilitó y un gen clave de los conos, gnat2, se expresó menos. Los propios peces se comportaron como si su visión estuviera disminuida inmediatamente después del tratamiento, pero estos problemas se desvanecieron en pocos días a medida que la retina comenzaba a recuperarse.
Células de color bajo estrés
Para ver qué ocurría dentro de células individuales, el equipo utilizó secuenciación de ARN de célula única, que lee qué genes están activados en miles de células individuales a la vez. Se centraron en los dos a cinco días posteriores a la retirada del fármaco, una ventana en la que los conos parecían recuperarse en lugar de morir. Los conos supervivientes disminuyeron la expresión de muchos genes relacionados con la detección de la luz y el procesamiento de señales, lo que sugiere que entraron temporalmente en un modo de “apagado” de su maquinaria visual. Al mismo tiempo, aumentaron la expresión de genes vinculados al manejo de subproductos reactivos del oxígeno y al mantenimiento de la calidad proteica. Este patrón apunta a un modo de respuesta al estrés en el que los conos se concentran en el control de daños y la restauración en lugar de en el rendimiento visual máximo.
Las células de soporte entran en modo reparación
Las principales células de soporte de la retina, llamadas glía de Müller, respondieron con fuerza a pesar de que solo se detectó una muerte limitada de conos. Estas células gliales se extienden desde la parte inferior hasta la superior de la retina, tocando directamente a las células fotosensibles, y se sabe que en el pez cebra actúan como fuente de nuevas neuronas tras una lesión. En este estudio, la glía de Müller aumentó la expresión de genes típicamente asociados con reactividad y remodelado tisular, y muchas de ellas volvieron a entrar en el ciclo celular, una señal de que comenzaron a dividirse. Los autores observaron la aparición de nuevas células de tipo progenitor en la capa media de la retina, que luego se trasladaron hacia la capa externa que alberga a los fotorreceptores. Algunas de estas respuestas de reparación iban acompañadas de conmutaciones en genes que suelen estar activos en células madre, lo que indica que la glía de Müller recuperó parcialmente un estado más flexible y regenerativo, a pesar de que la pérdida neta de células fue modesta.
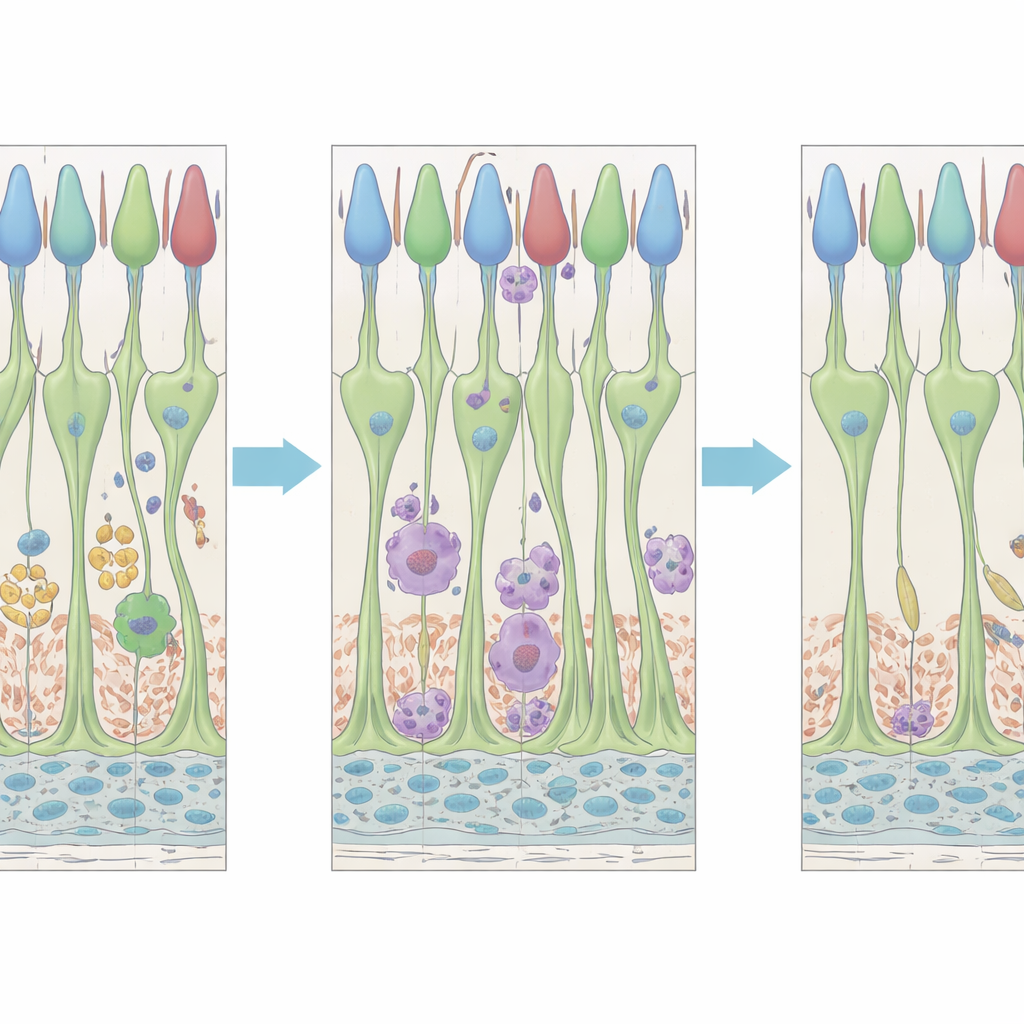
Células inmunitarias con dos olas de acción
Las células inmunitarias residentes en la retina, llamadas microglía y otras células mieloides estrechamente relacionadas, también mostraron una respuesta en dos etapas. A las aproximadamente dos días después del tratamiento, la microglía cambió de forma, agrupándose alrededor de los conos moribundos y probablemente ayudando a eliminar los restos. Más tarde, en torno a los cuatro o cinco días, surgió una segunda ola de comportamiento microglial alterado: las células aparecieron cerca de los segmentos externos de los conos y en el espacio próximo a la capa pigmentaria detrás de la retina, en un momento en que los conos mostraban señales fuertes de recuperación. Los patrones de expresión génica sugirieron que existen al menos dos subpoblaciones microgliales con firmas moleculares distintas, lo que insinúa que algunas células inmunitarias pueden especializarse en limpiar células moribundas, mientras que otras pueden centrarse en apoyar a las neuronas estresadas pero supervivientes.
Qué significa esto para proteger la visión
Este trabajo muestra que en el pez cebra, incluso una perturbación limitada y breve de las células sensibles al color es suficiente para movilizar una respuesta coordinada tanto de las células de soporte como de las inmunitarias. Los conos reducen temporalmente su función visual mientras activan programas internos de reparación. La glía de Müller se vuelve reactiva, se divide y produce células progenitoras, y la microglía responde en oleadas temporizadas relacionadas primero con la muerte celular y luego con la recuperación del estrés. En conjunto, estas respuestas parecen ayudar a la retina a restaurar su estructura y función tras un daño leve. Para las enfermedades oculares humanas que implican daño lento y crónico en lugar de lesiones súbitas, comprender cómo los peces cebra movilizan a la glía y a las células inmunitarias ante estrés subletal podría señalar terapias que potencien la propia capacidad del ojo para estabilizar o incluso reconstruir fotorreceptores vulnerables.
Cita: Weimar, H.V., Farre, A.A., Rumford, J.E. et al. Müller glial and microglial responses coupled to recovery of cone photoreceptors following limited cone ablation in zebrafish retina. Sci Rep 16, 9058 (2026). https://doi.org/10.1038/s41598-026-40141-1
Palabras clave: retina de pez cebra, fotorreceptores cono, glía de Müller, microglía, regeneración retiniana