Clear Sky Science · es
La integración transcriptómica guiada por aprendizaje automático identifica a GFM1 como un posible biomarcador relacionado con la lactilación en la disección aórtica
Por qué importa esta amenaza oculta en la aorta
La disección aórtica es una emergencia médica en la que una rotura en la arteria principal del cuerpo puede provocar hemorragias internas potencialmente mortales en cuestión de horas. Los cirujanos suelen poder salvar a los pacientes con intervención urgente, pero todavía no existen pruebas sanguíneas fiables que avisen pronto del peligro ni fármacos que ralenticen la enfermedad. Este estudio explora si cambios sutiles en la forma en que las células de la arteria gestionan la energía y las señales químicas podrían revelar nuevas señales de aviso, centrando la atención en un gen poco conocido llamado GFM1 que podría vincular el metabolismo celular con el debilitamiento de la pared aórtica.
Descifrando el código de una rotura peligrosa
En la disección aórtica, la sangre irrumpe en la pared de la aorta, separando sus capas. Por qué las aortas de algunas personas fallan de este modo aún no se comprende por completo. Los autores analizaron patrones de actividad génica en muestras de personas con disección aórtica y de individuos con aortas sanas. Prestaron especial atención a genes relacionados con la “lactilación”, una forma recientemente descrita en la que las células usan lactato —más conocido por acumularse en los músculos durante el ejercicio intenso— para ajustar proteínas y la regulación génica. Dado que la lactilación se ha vinculado a la inflamación y a la remodelación tisular, el equipo sospechó que los genes ligados al lactato podrían estar implicados en el daño de la pared aórtica.
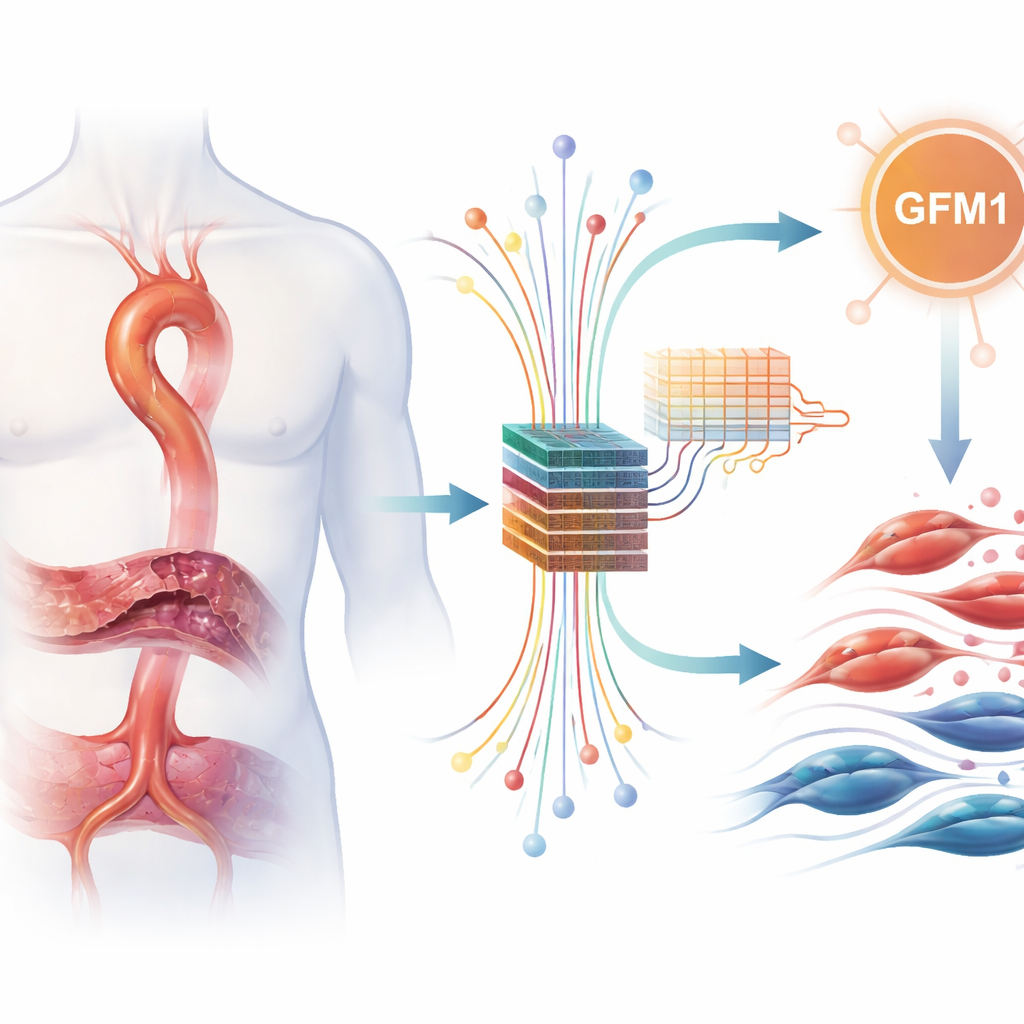
Minar grandes datos con algoritmos inteligentes
Para comprobar esta idea, los investigadores agregaron varios conjuntos de datos públicos que registran qué genes están activados o silenciados en tejido aórtico. Corregieron cuidadosamente las diferencias técnicas entre estudios y luego buscaron genes cuya actividad difería de forma consistente entre muestras enfermas y sanas. De entre miles de genes, hallaron 217 con cambios claros, muchos de los cuales apuntaban a reacciones inmunitarias y a la remodelación del andamiaje tisular que sostiene la aorta. A continuación, se centraron en una lista seleccionada de genes relacionados con el manejo del lactato y la lactilación e identificaron 11 que estaban a la vez alterados en la disección aórtica y formaban parte de estos programas vinculados al lactato.
Dejar que las máquinas voten por un sospechoso clave
Encontrar 11 genes interesantes seguía siendo demasiados para estudiar en profundidad en el laboratorio, por lo que el equipo recurrió a métodos de aprendizaje automático como un sistema de “votación” objetivo. Alimentaron los datos de estos genes en tres modelos distintos —LASSO, Random Forest y XGBoost— que se usan habitualmente para identificar patrones que mejor separan a pacientes de controles. Cada método destacó sus favoritos, pero solo un gen, GFM1, fue elegido con fuerza y de forma consistente por los tres. Este enfoque de verificación cruzada hizo que GFM1 emergiera como un marcador candidato especialmente robusto, aunque los modelos se utilizaron para clasificar y priorizar, no para construir una prueba diagnóstica lista para su uso clínico.
Acercándose a las células musculares de la arteria
GFM1 contribuye a controlar cómo las mitocondrias, las fábricas de energía dentro de las células, sintetizan sus propias proteínas. Dado que el equilibrio energético es crucial para el comportamiento de las células de la pared arterial, los autores examinaron GFM1 con más detalle. Confirmaron que los niveles de GFM1 eran mayores en tejido de pacientes con disección aórtica que en aortas no enfermas. Luego pasaron a un sistema de cultivo celular controlado usando células musculares lisas vasculares de ratón —las células con características musculares que dan fuerza a la aorta. Cuando estas células se estimularon con angiotensina II, una hormona vinculada a la hipertensión y al estrés vascular, mostraron mayor tendencia a proliferar y a migrar, imitando cambios dañinos observados en arterias enfermas. Cuando los investigadores redujeron GFM1 en estas células mediante ARN interferente, el crecimiento y la migración impulsados por angiotensina se redujeron notablemente, lo que sugiere que GFM1 contribuye a promover esos comportamientos de riesgo.
Qué implica esto y qué todavía no demuestra
En conjunto, los hallazgos sugieren que GFM1 podría actuar como un puente entre el metabolismo celular alterado y el comportamiento agresivo de las células de la pared arterial en la disección aórtica. En términos sencillos, una mayor actividad de GFM1 parece asociarse con una aorta más inestable y propensa al daño, y reducirlo en células cultivadas las hace menos propensas a proliferar y migrar en exceso. Sin embargo, los autores insisten en que este trabajo aún está en una fase temprana de generación de hipótesis. No midieron directamente la lactilación en los tejidos ni probaron que GFM1 esté modificado químicamente de esta manera, y la capacidad predictiva de los modelos no se ha validado en grupos independientes de pacientes. Estudios futuros deberán confirmar estos resultados en cohortes más amplias y explorar exactamente cómo GFM1 y los cambios metabólicos relacionados debilitan la pared aórtica. Si esos esfuerzos tienen éxito, GFM1 o sus vías podrían eventualmente convertirse en dianas para nuevas pruebas sanguíneas o tratamientos destinados a prevenir esta rotura, a menudo fatal, antes de que ocurra.
Cita: Chen, J., Jiang, N., Guo, Z. et al. Machine-learning–guided transcriptomic integration identifies GFM1 as a lactylation-related candidate biomarker in aortic dissection. Sci Rep 16, 9033 (2026). https://doi.org/10.1038/s41598-026-40139-9
Palabras clave: disección aórtica, células musculares lisas vasculares, metabolismo del lactato, función mitocondrial, descubrimiento de biomarcadores