Clear Sky Science · es
Ciprofol atenúa la lesión por isquemia‒reperfusión cerebral en ratas al inhibir la ferroptosis mediante la regulación al alza de AMPK
Por qué importa proteger el cerebro tras un ictus
Cuando una persona sufre un ictus isquémico, los médicos corren para reabrir el vaso sanguíneo obstruido y restablecer el flujo de sangre al cerebro. Paradójicamente, este paso que salva vidas puede causar daño adicional, un fenómeno conocido como lesión por reperfusión. El cerebro, repentinamente inundado de oxígeno y nutrientes después de un periodo de privación, desencadena una cascada de reacciones químicas que pueden matar a las neuronas más vulnerables. Este estudio investiga si el ciprofol, un nuevo anestésico ya utilizado para sedación, también puede actuar como protector del cerebro durante esta ventana crítica al mitigar algunos de los procesos más dañinos que se desencadenan cuando vuelve el flujo sanguíneo.
De la obstrucción del flujo sanguíneo al daño cerebral
Para reproducir lo que ocurre en un ictus humano, los investigadores bloquearon temporalmente una arteria cerebral importante en ratas y luego restablecieron el flujo sanguíneo, creando lo que se conoce como lesión por isquemia–reperfusión cerebral. Algunas ratas solo fueron sometidas al procedimiento, mientras que otras recibieron ciprofol poco después de reiniciarse el flujo sanguíneo. El equipo evaluó la capacidad de movimiento y la respuesta táctil de los animales, y examinó sus cerebros en busca de áreas de tejido muerto y daños estructurales en las neuronas. Las ratas que recibieron ciprofol presentaron zonas de lesión cerebral más pequeñas, neuronas de apariencia más saludable y mejores puntuaciones en pruebas motoras y sensoriales que los animales no tratados, lo que sugiere que el fármaco atenuó las peores consecuencias del daño.
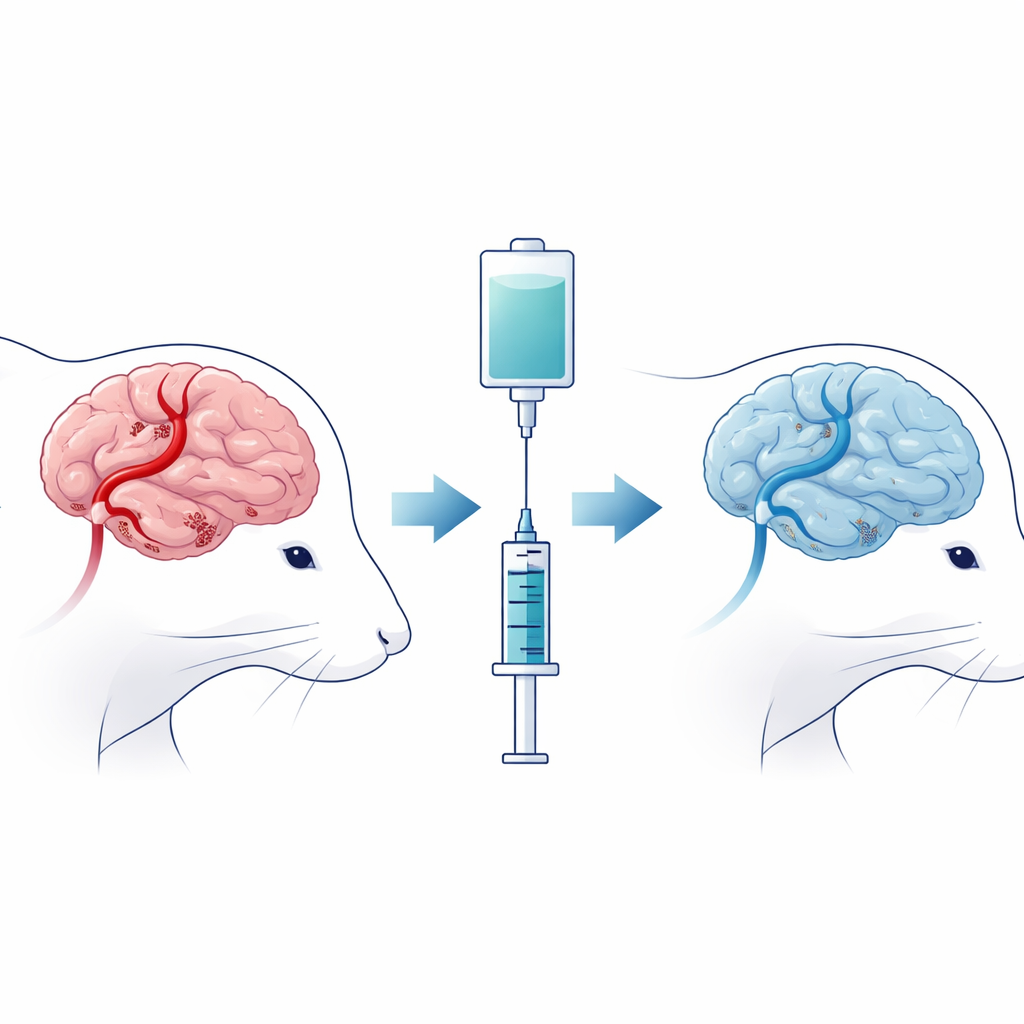
Una forma oculta de muerte celular impulsada por el hierro
Más allá del daño tisular visible, los autores se centraron en un tipo de muerte celular reconocido recientemente llamado ferroptosis, que se alimenta del hierro y de reacciones químicas descontroladas que atacan los componentes lipídicos de las membranas celulares. En las ratas modelo de ictus no tratadas, el tejido cerebral de la zona vulnerable alrededor del núcleo de la lesión contenía más hierro, niveles más altos de un subproducto de daño lipídico y mitocondrias neuronales que parecían hinchadas y estructuralmente dañadas al observarlas con microscopía electrónica. Las pruebas moleculares mostraron que las proteínas protectoras que normalmente detoxifican los subproductos lipídicos dañinos estaban reducidas, mientras que las proteínas que favorecen este proceso destructivo aumentaban. El ciprofol revirtió en gran medida estos cambios: disminuyeron el hierro y el daño lipídico, el equilibrio de proteínas clave se desplazó hacia la protección y las mitocondrias conservaron formas y estructuras internas más normales.
Un sensor de energía celular como interruptor de control
El estudio examinó después cómo produce ciprofol estos efectos protectores. La atención se centró en AMPK, una proteína que actúa como sensor de energía celular y respondedor al estrés. En los cerebros lesionados de las ratas no tratadas, la actividad de AMPK estaba deprimida. El ciprofol aumentó la forma activada de AMPK, en paralelo con las reducciones del daño relacionado con la ferroptosis. Para probar si este sensor energético realmente ocupa una posición upstream en la cadena de eventos protectores, los investigadores utilizaron otro fármaco, el Compuesto C, que bloquea AMPK. Cuando los animales recibieron tanto ciprofol como este inhibidor de AMPK, los beneficios del ciprofol se perdieron parcialmente: los marcadores relacionados con la ferroptosis volvieron a acercarse a niveles perjudiciales, la acumulación de hierro reapareció y la señal de actividad de AMPK descendió incluso más que en los animales con ictus no tratados. Este patrón respalda la idea de que activar AMPK es un paso clave en la forma en que el ciprofol protege a las células cerebrales.
Amortiguar la tormenta inflamatoria cerebral
La lesión relacionada con el ictus no es solo una cuestión de muerte celular dentro de las neuronas; la respuesta inmune del cerebro también desempeña un papel importante. El equipo midió varias moléculas mensajeras inflamatorias que típicamente se disparan tras la isquemia–reperfusión. En los animales no tratados, estas señales se elevaron notablemente, reflejando una intensa reacción inflamatoria. El ciprofol redujo los tres principales marcadores inflamatorios medidos, lo que sugiere que no solo suprime el daño de membrana impulsado por el hierro, sino que también mitiga la tormenta inflamatoria subsiguiente. Cuando AMPK se bloqueó con el Compuesto C, estos efectos calmantes sobre la inflamación se debilitaron, vinculando de nuevo los beneficios del ciprofol con esta vía central de detección de energía.
Qué podría significar esto para la atención futura
En conjunto, los resultados señalan al ciprofol como algo más que un sedante: en este modelo en ratas, parece limitar el daño cerebral relacionado con el ictus activando AMPK, lo que a su vez frena la muerte celular impulsada por el hierro y atenúa la inflamación. Dado que el ciprofol ya se usa en clínicas para anestesia y sedación de procedimientos, su potencial añadido como agente neuroprotector resulta especialmente intrigante. Aun así, el trabajo tiene limitaciones importantes, incluida la dependencia de un solo modelo animal y la posibilidad de que el fármaco bloqueador de AMPK tenga efectos secundarios propios. Serán necesarios más estudios, incluidos en otras especies y, finalmente, en pacientes humanos, para confirmar si el ciprofol puede ayudar de forma segura a proteger el cerebro durante y después del tratamiento del ictus.
Cita: Zeng, H., Yu, X., Zheng, Z. et al. Ciprofol attenuates cerebral Ischemia‒reperfusion injury in rats by inhibiting ferroptosis through upregulating AMPK. Sci Rep 16, 9282 (2026). https://doi.org/10.1038/s41598-026-40104-6
Palabras clave: accidente cerebrovascular isquémico, lesión por reperfusión, ciprofol, ferroptosis, neuroprotección