Clear Sky Science · es
El mecanismo antitumoral de oclacitinib en el linfoma canino
Por qué esto importa para los perros y sus familias
El linfoma es uno de los cánceres más frecuentes en perros de compañía y, aunque la quimioterapia puede ayudar a muchos pacientes, no siempre funciona y puede causar efectos secundarios importantes. Oclacitinib, una pastilla ampliamente prescrita para perros con picor por dermatitis alérgica, ha mostrado recientemente beneficios sorprendentes en algunos perros con linfoma cutáneo. Este estudio plantea una pregunta simple pero importante: ¿cómo, exactamente, podría este fármaco para la alergia actuar contra las células cancerosas, y podemos predecir qué perros tienen más probabilidades de beneficiarse?
De medicamento para la alergia a combatiente del cáncer
Oclacitinib se desarrolló para calmar señales inmunitarias sobreactivadas que impulsan la dermatitis atópica. Lo hace bloqueando una familia de interruptores moleculares llamados JAK, especialmente JAK1, que transmiten mensajes desde moléculas inflamatorias en la superficie celular hasta el núcleo. Los veterinarios empezaron a observar que algunos perros con una forma de linfoma cutáneo mejoraban al recibir oclacitinib, pero las razones eran poco claras y las respuestas eran inconsistentes. Los investigadores se propusieron estudiar esto de forma controlada, usando células de linfoma canino cultivadas en laboratorio, junto con muestras de pacientes caninos reales, para ver cuándo y cómo oclacitinib puede realmente matar células cancerosas en lugar de solo calmar la piel. 
Probando células de linfoma en el laboratorio
El equipo examinó una línea celular de linfoma cutáneo canino y ocho líneas adicionales de linfoma de alto grado que representaban tanto cánceres de células T como de células B. Cuando expusieron estas células a oclacitinib en concentraciones similares a las alcanzadas en perros tratados, aproximadamente la mitad de las líneas celulares mostró una clara desaceleración del crecimiento y varias sufrieron muerte celular. Las células sensibles se acumularon en una fase de reposo del ciclo celular y mostraron señales características de muerte celular programada, incluida la activación de una proteína ejecutora llamada caspasa-3. En contraste, otras líneas de linfoma casi no respondieron en el mismo rango de concentración, lo que pone de manifiesto que el linfoma en perros no es una única enfermedad sino un conjunto de cánceres biológicamente distintos.
Enfocando una vía de señalización vulnerable
Para descubrir qué separaba a los tumores sensibles de los resistentes, los científicos se centraron en la vía de señalización JAK/STAT, una ruta de supervivencia común en muchos cánceres hematológicos. Encontraron que solo las líneas celulares de linfoma que respondieron a oclacitinib mostraban una fuerte activación basal de dos protagonistas clave: JAK1 y STAT5. Cuando estas células sensibles fueron tratadas con oclacitinib, la actividad de STAT5 cayó bruscamente, mientras que los niveles globales de las proteínas permanecieron iguales. Un segundo fármaco bloqueador de JAK1 usado en medicina humana, filgotinib, produjo un patrón similar de inhibición del crecimiento y apagado de STAT5. Un perfil profundo de actividad génica reveló que oclacitinib atenuó conjuntos de genes vinculados con la señalización JAK/STAT y redujo la expresión de c-Myc, un impulsor maestro del crecimiento que con frecuencia es secuestrado en los cánceres, lo que ayuda a explicar la detención del ciclo celular y la muerte celular observadas. 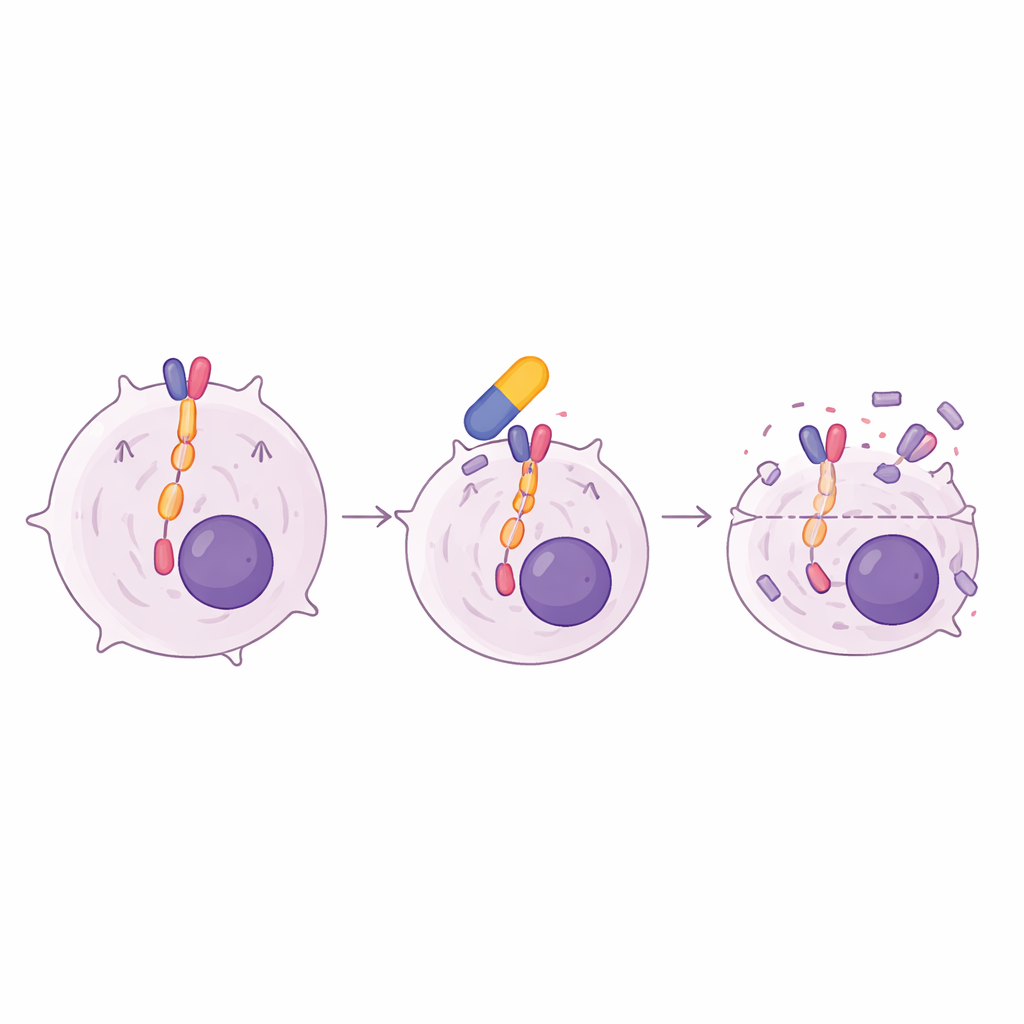
Vinculando los hallazgos de laboratorio con pacientes caninos reales
Los investigadores se dirigieron luego a muestras de biopsia de perros con linfoma cutáneo que habían sido tratados con oclacitinib en clínicas. Utilizando métodos de tinción que revelan proteínas activadas, encontraron que los perros cuyos tumores mostraban JAK1 y STAT5 activados tenían más probabilidades de experimentar respuestas parciales o completas al fármaco. Algunos no respondedores aún mostraban estas señales activadas, lo que sugiere que rutas de escape adicionales pueden sostener ciertos tumores, pero el patrón general apuntó a una asociación fuerte. De forma importante, muchas muestras de linfoma de ganglios linfáticos e intestinal de otros perros también mostraron este mismo patrón de activación JAK1/STAT5, lo que plantea la posibilidad de que los beneficios de oclacitinib puedan extenderse más allá del linfoma cutáneo a un conjunto más amplio de linfomas caninos agresivos.
Qué podría significar para tratamientos futuros
En conjunto, el trabajo muestra que oclacitinib puede inhibir directamente y, en ocasiones, matar ciertas células de linfoma canino al desconectar una vía de supervivencia clave centrada en JAK1 y STAT5 y reducir la actividad de genes que promueven el crecimiento como c-Myc. Linfocitos normales de perros sanos se vieron mucho menos afectados a dosis clínicamente relevantes, aunque concentraciones altas sí ralentizaron la expansión de células inmunitarias activadas, subrayando la necesidad de equilibrar los efectos anticancerígenos con la posible supresión inmune. El estudio sugiere que analizar los tumores en busca de JAK1 y STAT5 activados podría ayudar a los veterinarios a identificar a los perros con mayor probabilidad de beneficiarse de oclacitinib y fármacos similares. Si bien hacen falta más ensayos clínicos, este medicamento para la alergia, ampliamente disponible, podría formar parte de un conjunto de tratamientos dirigidos para el linfoma canino, guiado por marcadores moleculares sencillos.
Cita: Harada, M., Inanaga, S., Sakurai, M. et al. The antitumor mechanism of oclacitinib in canine lymphoma. Sci Rep 16, 8427 (2026). https://doi.org/10.1038/s41598-026-40066-9
Palabras clave: linfoma canino, oclacitinib, vía JAK1 STAT5, terapia contra el cáncer dirigida, oncología veterinaria