Clear Sky Science · es
MyoFuse es un flujo de trabajo totalmente basado en IA para la cuantificación automática de la fusión de células musculares esqueléticas in vitro
Por qué importa contar las células musculares
Cuando hacemos ejercicio, nos recuperamos de una lesión o desarrollamos enfermedades como la diabetes, nuestros músculos esqueléticos se remodelan constantemente. En el laboratorio, los científicos imitan este proceso cultivando células musculares en una placa y observando cómo células individuales se fusionan en fibras largas y multinucleadas. Un número simple llamado índice de fusión les indica qué tan bien está ocurriendo esa fusión. Pero hoy en día ese número suele obtenerse mediante el recuento manual por parte de personas de miles de diminutos núcleos celulares en una pantalla: un trabajo lento, inconsistente y propenso a errores. Este estudio presenta MyoFuse, un flujo de trabajo totalmente basado en IA que automatiza esta tarea de conteo, con el objetivo de hacer la investigación muscular más rápida, fiable y menos sesgada.
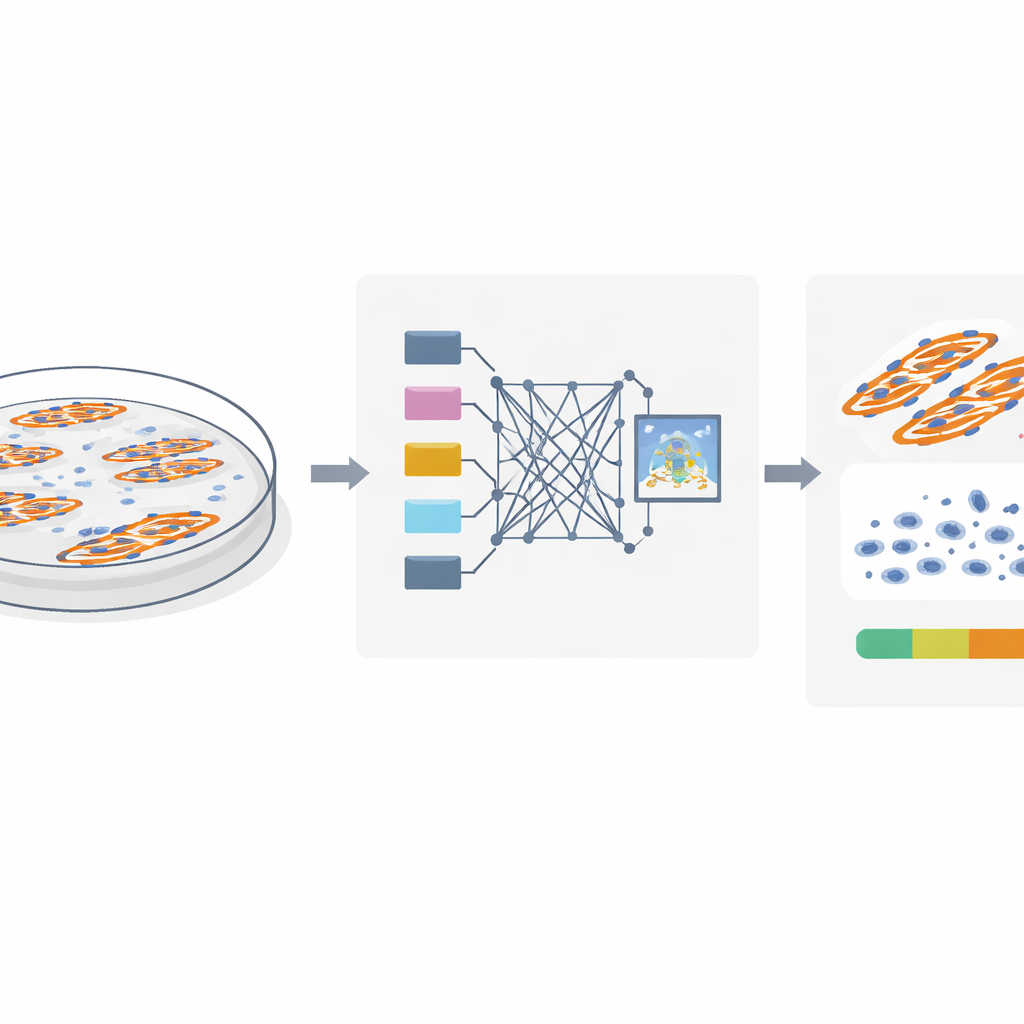
El reto de ver lo que realmente está ahí
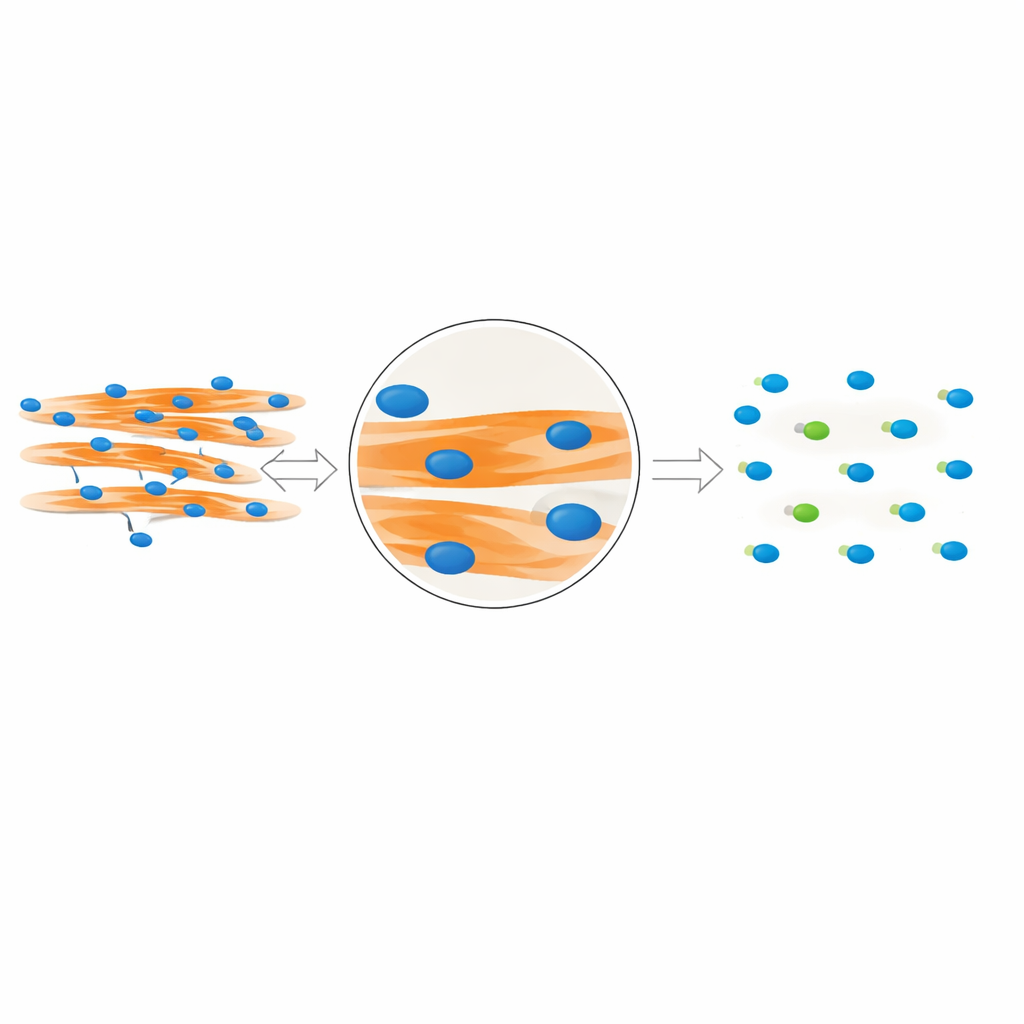
Para estudiar la fusión de células musculares, los investigadores tiñen los núcleos y las fibras musculares con colorantes fluorescentes y toman imágenes al microscopio. La pregunta clave es qué núcleos están realmente dentro de las fibras fusionadas y cuáles pertenecen a células no fusionadas que están cerca. Los métodos tradicionales asumen que si un núcleo se solapa con una fibra muscular en una imagen plana bidimensional, debe estar dentro de esa fibra. Sin embargo, las células crecen en tres dimensiones: un núcleo puede estar por encima o por debajo de una fibra y aun así parecer superponerse en la imagen. Los autores usan imágenes confocales detalladas en células musculares de ratón y humanas para mostrar que ese truco del solapamiento puede llevar a error, haciendo que muchos núcleos cercanos se cuenten equivocadamente como parte de fibras fusionadas e inflando el índice de fusión.
Una forma más inteligente de leer imágenes fluorescentes
El equipo se dio cuenta de que los núcleos verdaderamente “dentro de la fibra” dejan una huella visual distintiva. Porque esos núcleos ocupan físicamente espacio dentro de la fibra, crean pequeños huecos oscuros en la señal fluorescente que marca la proteína muscular MyHC. En contraste, los núcleos que están por encima o por debajo de una fibra no interrumpen esa señal. Partiendo de esta observación, los autores diseñaron MyoFuse, un flujo de trabajo de IA en dos pasos. Primero, un modelo de segmentación especializado (adaptado de la herramienta de código abierto Cellpose) delimita con precisión los núcleos individuales, incluso cuando están muy agrupados. Segundo, una red neuronal ligera clasifica, para cada núcleo, la señal de MyHC circundante y decide si el núcleo está dentro o fuera de una fibra, basándose únicamente en este patrón local en lugar del simple solapamiento.
Qué tan bien coincide la IA con expertos humanos
Los investigadores evaluaron rigurosamente MyoFuse en imágenes de células musculares C2C12 de ratón y en células musculares humanas primarias procedentes de distintos músculos. Para ambas especies, el recuento total de núcleos por parte de la IA y su índice de fusión calculado concordaron extremadamente bien con las anotaciones manuales cuidadosas de expertos, con correlaciones casi perfectas. A nivel de núcleos individuales, el clasificador distinguió correctamente núcleos dentro y fuera de las fibras en más del 90% de los casos en los distintos conjuntos de datos, con métricas de rendimiento que compiten con la discriminación a nivel humano. De forma importante, MyoFuse también funcionó bien en un conjunto separado de células humanas que nunca se había usado para entrenamiento, lo que sugiere que el enfoque puede generalizar a nuevas muestras en lugar de limitarse a memorizar las imágenes de entrenamiento.
Revelando un sesgo oculto en métodos comunes
Más allá de su precisión, MyoFuse puso de manifiesto problemas sistemáticos en métodos basados en máscaras ampliamente usados que dependen del solapamiento simple entre las señales nucleares y de fibra. Cuando los autores compararon los índices de fusión de MyoFuse con los de un enfoque de máscara refinado aplicado a las mismas imágenes, el método de máscara sobreestimó sistemáticamente la fusión, especialmente en áreas donde las fibras musculares ocupaban una mayor fracción de la placa. Ajustar los umbrales de detección cambiaba los números pero no eliminaba este sesgo subyacente; las mejoras aparentes a menudo provenían de errores que se cancelaban entre sí en lugar de reflejar mejor la biología. El equipo también mostró que las estimaciones de fusión pueden variar ampliamente entre diferentes regiones de un mismo pocillo, subrayando que analizar solo unos pocos campos seleccionados manualmente puede dar una visión distorsionada de qué tan bien se están fusionando las células.
Qué implica esto para la investigación muscular futura
MyoFuse ofrece a los biólogos musculares una forma de medir la fusión celular que es a la vez más rápida y más fiel a lo que realmente ocurre en la placa. Al combinar microscopía automatizada con una IA capaz de segmentar y clasificar cientos de miles de núcleos en minutos, el flujo de trabajo reduce la carga de trabajo humana, minimiza las decisiones subjetivas sobre dónde mirar y cómo establecer umbrales en las imágenes, y evita contar células cercanas como músculo fusionado. Los autores reconocen que condiciones extremas de imagen o protocolos de tinción muy diferentes pueden requerir reentrenamiento, pero el método es de acceso abierto y fue diseñado para ser adaptable. Para los laboratorios que estudian el desarrollo muscular, el envejecimiento, la regeneración o enfermedades metabólicas, MyoFuse promete mediciones de fusión más robustas y, con ello, conclusiones más fiables sobre cómo los músculos crecen y cambian.
Cita: Lair, B., Cazorla, C., Lobeto, A. et al. MyoFuse is a fully AI-based workflow for automated quantification of skeletal muscle cell fusion in vitro. Sci Rep 16, 9387 (2026). https://doi.org/10.1038/s41598-026-40047-y
Palabras clave: músculo esquelético, fusión celular, inteligencia artificial, análisis de imágenes, miogénesis